Im Kern ist das Bioreaktordesign die Praxis, eine präzise kontrollierte und sterile Umgebung zu schaffen, die den spezifischen metabolischen Bedürfnissen lebender Zellen oder Mikroorganismen entspricht. Der Erfolg hängt von einigen grundlegenden Prinzipien ab: Aufrechterhaltung der Sterilität (Asepsis), Ermöglichung eines effizienten Stoffaustauschs von Gasen und Nährstoffen, Wärmemanagement, Gewährleistung der Homogenität durch Mischung sowie Implementierung robuster Prozessüberwachung und -steuerung. Jede Designentscheidung, von der Form des Behälters bis zur Art des Laufrads, ist eine bewusste Entscheidung, um diese biologischen Anforderungen zu erfüllen.
Ein Bioreaktor ist nicht nur ein Behälter; er ist ein integriertes System, bei dem die Technik vollständig der Biologie untergeordnet sein muss. Die grundlegende Herausforderung besteht darin, konkurrierende Faktoren – wie Mischeffizienz gegenüber Zellschädigung – auszugleichen, um die optimalen Bedingungen für Ihren spezifischen Bioprozess zu schaffen.

Die Grundlage: Unterstützung des biologischen Prozesses
Jede Designüberlegung leitet sich aus der Notwendigkeit ab, eine stabile und produktive Umgebung für die Kultur zu schaffen. Die technischen Komponenten sind lediglich die Werkzeuge, mit denen diese biologischen Ziele erreicht werden.
Aufrechterhaltung einer reinen Kultur (Asepsis)
Kontamination ist die größte Bedrohung für einen erfolgreichen Bioprozess. Ein effektives Bioreaktordesign muss von Grund auf steril sein.
Dies wird durch Materialien erreicht, die einer Sterilisation standhalten (z. B. Autoklavieren oder Dampf-in-Place), und durch ein Design ohne Spalten, in denen sich Verunreinigungen verstecken können. Alle Verbindungen, Sonden und Probenahmestellen müssen über robuste Dichtungen verfügen, um das Eindringen von Mikroben während der langen Dauer einer Kultur zu verhindern.
Bereitstellung von Sauerstoff und Nährstoffen (Stoffaustausch)
Zellen benötigen eine konstante Versorgung mit Sauerstoff und Nährstoffen sowie eine konstante Entfernung von Abfallprodukten wie CO2. Die Fähigkeit des Designs, diesen Austausch zu erleichtern, ist ein Hauptbestimmungsfaktor für die Leistung.
Bei aeroben Kulturen muss die Sauerstofftransferrate (OTR) des Reaktors die Sauerstoffaufnahmerate (OUR) der Zellen erreichen oder übertreffen. Dies wird durch das Begasungssystem (das Gasblasen einbringt) und das Rührsystem (das Blasen zerteilt, um die Oberfläche für den Gasaustausch zu vergrößern) gesteuert.
Temperaturkontrolle (Wärmeübertragung)
Alle biologischen Prozesse erzeugen Wärme. Wenn diese Stoffwechselwärme nicht effizient abgeführt wird, steigt die Temperatur über den optimalen Bereich hinaus an, was die Zellen belastet oder abtötet.
Bioreaktoren regeln dies mit externen Mänteln oder internen Kühlschlangen, durch die eine Kühlflüssigkeit zirkuliert wird. Die Effizienz der Wärmeübertragung hängt von der verfügbaren Oberfläche für den Austausch und dem Gesamtdesign des Kühlsystems ab.
Homogenität erreichen (Mischen)
Das Kulturmedium muss perfekt gemischt sein, um sicherzustellen, dass jede Zelle gleichen Zugang zu Nährstoffen hat und keinen lokalen Ansammlungen toxischer Nebenprodukte ausgesetzt ist. Ein Mangel an Homogenität erzeugt leistungshemmende Gradienten in pH-Wert, gelöstem Sauerstoff und Substratkonzentration.
Eine ordnungsgemäße Durchmischung wird durch eine Kombination aus einem optimierten Rührsystem (Laufrad und Motor) und internen Behältermerkmalen wie Leitblechen erreicht, die die Bildung eines zentralen Wirbels verhindern und eine Bewegung der Flüssigkeit von oben nach unten fördern.
Wichtige technische Komponenten und ihre Auswirkungen
Nachdem die biologischen Ziele festgelegt sind, können wir die spezifische Hardware untersuchen, die zu deren Erreichung entwickelt wurde.
Der Behälter selbst: Geometrie und Materialien
Die Form und das Material des Reaktorgefäßes haben erhebliche Auswirkungen. Das Seitenverhältnis (Höhe zu Durchmesser) beeinflusst die Mischmuster und die Belüftungseffizienz, wobei oft höhere, schmälere Gefäße für die mikrobielle Fermentation verwendet werden.
Das Material ist typischerweise Edelstahl 316L wegen seiner Haltbarkeit und Reinigungsfähigkeit oder zunehmend Einweg-Kunststofffolien. Die Wahl zwischen ihnen stellt eine wichtige strategische Entscheidung in Bezug auf die Anlagengestaltung und die Betriebsphilosophie dar.
Das Rührwerk: Laufräder und Leitbleche
Das Laufrad ist das Herzstück des Mischsystems. Sein Design bestimmt das Gleichgewicht zwischen Flüssigkeitsbewegung und der physikalischen Kraft, der sogenannten Schubspannung (Shear), die auf die Zellen ausgeübt wird.
- Rushton-Turbinen erzeugen hohe Scherkräfte und eignen sich hervorragend zur Zerstreuung von Gasblasen in robusten mikrobiellen Kulturen.
- Schrägblatt- oder Schiffspropeller-Laufräder erzeugen eine sanfte, axiale Strömung, die ideal für empfindliche Säugetier- oder Insektenzellkulturen ist.
Das Belüftungssystem: Begaser und Gassteuerung
Der Begaser führt Gase in den Reaktor ein. Ein einfacher Ringbegaser oder ein Rohrbegaser mit Bohrungen setzt größere Blasen frei, die für viele Anwendungen geeignet sind.
Ein mikroporöser oder gesinterter Begaser erzeugt viel feinere Blasen, was die Oberfläche für den Sauerstofftransfer dramatisch erhöht, kann aber anfällig für Verstopfungen sein und Schaumbildung verursachen.
Das „Nervensystem“: Sensoren und Steuerung
Was man nicht messen kann, kann man nicht kontrollieren. Ein moderner Bioreaktor ist mit einer Reihe von Sensoren ausgestattet, um kritische Prozessparameter in Echtzeit zu überwachen.
Standard-Sonden umfassen solche für pH-Wert, gelösten Sauerstoff (DO) und Temperatur. Diese Daten werden an eine Steuereinheit übermittelt, die automatisch Eingaben anpasst – wie das Hinzufügen einer Base zur Korrektur des pH-Werts oder die Erhöhung des Gasflusses zur Anhebung des DO-Werts –, um den Prozess innerhalb seines optimalen Fensters zu halten.
Die Kompromisse verstehen
Das Bioreaktordesign ist eine Übung im Ausgleich konkurrierender Anforderungen. Das Verständnis dieser Kompromisse unterscheidet einen Anfänger von einem Experten.
Schubspannung vs. Mischeffizienz
Dies ist das klassische Dilemma. Die Erhöhung der Laufradgeschwindigkeit verbessert die Durchmischung und den Sauerstofftransfer, was für Kulturen mit hoher Zelldichte notwendig ist. Dies erhöht jedoch auch die Scherkräfte, die empfindliche Säugetierzellen schädigen oder abtöten können. Das Design muss gerade genug Energie für den Stoffaustausch liefern, ohne die Zellvitalität zu beeinträchtigen.
Edelstahl vs. Einwegsysteme
Edelstahlreaktoren sind eine langfristige Kapitalinvestition. Sie sind robust und können jahrzehntelang verwendet werden, erfordern jedoch erhebliche Infrastruktur für die Reinigung (Clean-In-Place) und Sterilisation (Steam-In-Place) sowie lange Validierungs- und Durchlaufzeiten.
Einweg-Bioreaktoren (SUBs) haben deutlich geringere Anschaffungskosten und bieten operative Flexibilität mit nahezu keiner Durchlaufzeit, da die gesamte produktberührende Komponente nach Gebrauch entsorgt wird. Sie verursachen jedoch wiederkehrende Verbrauchskosten und Bedenken hinsichtlich der Auslaugung von Verbindungen aus dem Kunststoff in das Medium.
Die Herausforderung der Maßstabsvergrößerung (Scale-Up)
Ein Prozess, der in einem 2-Liter-Benchtop-Reaktor perfekt funktioniert, kann in einem 2.000-Liter-Produktionsgefäß vollständig fehlschlagen. Dies liegt daran, dass die Beziehungen zwischen Volumen, Oberfläche und Mischdynamik nicht linear skalieren.
Ein erfolgreicher Scale-Up erfordert die Konstanz eines Schlüsselparameters, wie der Laufradspitzengeschwindigkeit (zur Kontrolle der Scherkräfte) oder der Leistung pro Volumeneinheit (zur Aufrechterhaltung der Durchmischung), was andere Designelemente zur Änderung zwingt.
Das Design auf Ihr Bioprozesziel abstimmen
Das richtige Design ist dasjenige, das Ihre spezifische Anwendung am besten unterstützt. Nutzen Sie diese Richtlinien, um Ihre Überlegungen zu leiten.
- Wenn Ihr Hauptaugenmerk auf der mikrobiellen Fermentation mit hoher Zelldichte liegt (z. B. E. coli): Priorisieren Sie ein robustes Design mit extrem hoher Sauerstoffübertragung und Wärmeabfuhrkapazität, wahrscheinlich unter Verwendung von Rushton-Turbinen und einem leistungsstarken Kühlmantel.
- Wenn Ihr Hauptaugenmerk auf der großtechnischen Säugetierzellkultur liegt (z. B. Antikörper): Wählen Sie ein System, das für niedrige Scherkräfte ausgelegt ist, unter Verwendung von Schrägblatt- oder anderen speziellen Laufrädern und hochentwickelten Gassteuerungsstrategien für eine präzise pH- und DO-Regelung.
- Wenn Ihr Hauptaugenmerk auf der Prozessentwicklung und Flexibilität liegt: Eine Einweg-Plattform ist oft überlegen, da sie es Ihnen ermöglicht, schnell verschiedene Prozesse und Zelllinien durchzuführen, ohne das Risiko einer Kreuzkontamination oder der Ausfallzeiten durch Reinigungszyklen.
- Wenn Ihr Hauptaugenmerk auf der Kultivierung scherempfindlicher oder adhäsionsabhängiger Zellen liegt: Ziehen Sie alternative Designs wie Festbettreaktoren, Hohlfasermembranreaktoren oder wellengemischte Bioreaktoren in Betracht, die eine große Oberfläche ohne mechanisches Rühren bieten.
Letztendlich ist ein gut konzipierter Bioreaktor eine elegante Lösung für eine komplexe biologische Herausforderung, die entwickelt wurde, um das volle Potenzial Ihres Prozesses auszuschöpfen.
Zusammenfassungstabelle:
| Design-Überlegung | Schlüsselfaktor | Auswirkung auf den Prozess |
|---|---|---|
| Sterilität (Asepsis) | Materialien, Dichtungen, Sterilisationsmethoden | Verhindert Kontamination, gewährleistet Kulturreinheit |
| Stoffaustausch | Begaser-Typ, Laufraddesign, OTR | Liefert Sauerstoff/Nährstoffe, entfernt Abfallstoffe |
| Mischen & Homogenität | Laufrad-Typ, Leitbleche, Rührgeschwindigkeit | Verhindert Gradienten, gewährleistet einheitliche Bedingungen |
| Wärmeübertragung | Kühlmäntel/-schlangen | Hält die optimale Temperatur für das Zellwachstum aufrecht |
| Scale-Up | Laufradspitzengeschwindigkeit, Leistung/Volumen | Gewährleistet Prozesskonsistenz vom Labor bis zur Produktion |
| Reaktortyp | Edelstahl vs. Einweg | Gleicht Kosten, Flexibilität und betriebliche Anforderungen aus |
Schöpfen Sie das volle Potenzial Ihres Bioprozesses mit KINTEK aus
Die Entwicklung des richtigen Bioreaktorsystems ist entscheidend für den Erfolg Ihrer Zellkultur, Fermentation oder Ihres Bioprocessing-Workflows. Das Gleichgewicht zwischen Sterilität, effizientem Stoffaustausch und sanfter Durchmischung ist komplex, und die falsche Ausrüstung kann zu kostspieligen Ausfällen und reduzierten Ausbeuten führen.
KINTEK ist spezialisiert auf die Bereitstellung hochwertiger Laborgeräte und Verbrauchsmaterialien, die auf die genauen Bedürfnisse moderner Labore zugeschnitten sind. Ob Sie einen mikrobiellen Fermentationsprozess skalieren oder empfindliche Säugetierzellen für die therapeutische Produktion kultivieren – wir verfügen über das Fachwissen und die Produkte, um Sie zu unterstützen.
- Fachkundige Beratung: Unser Team kann Ihnen helfen, die Kompromisse zwischen Edelstahl- und Einwegsystemen abzuwägen oder das ideale Laufrad- und Begaserdesign für Ihre spezifische Zelllinie auszuwählen.
- Zuverlässige Leistung: Verlassen Sie sich auf unsere Geräte für eine robuste Temperaturkontrolle, präzises Gasmanagement und konsistente, reproduzierbare Ergebnisse.
- Prozessflexibilität: Von der Laborforschung (R&D) bis zur Pilotproduktion finden Sie die richtige Bioreaktorerlösung, um Ihren Entwicklungszeitplan zu beschleunigen.
Lassen Sie nicht zu, dass Ausrüstungseinschränkungen Ihre Innovation behindern. Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie die Bioreaktorerlösungen von KINTEK die Effizienz, Zuverlässigkeit und Ausbeute Ihres Labors verbessern können.
Visuelle Anleitung
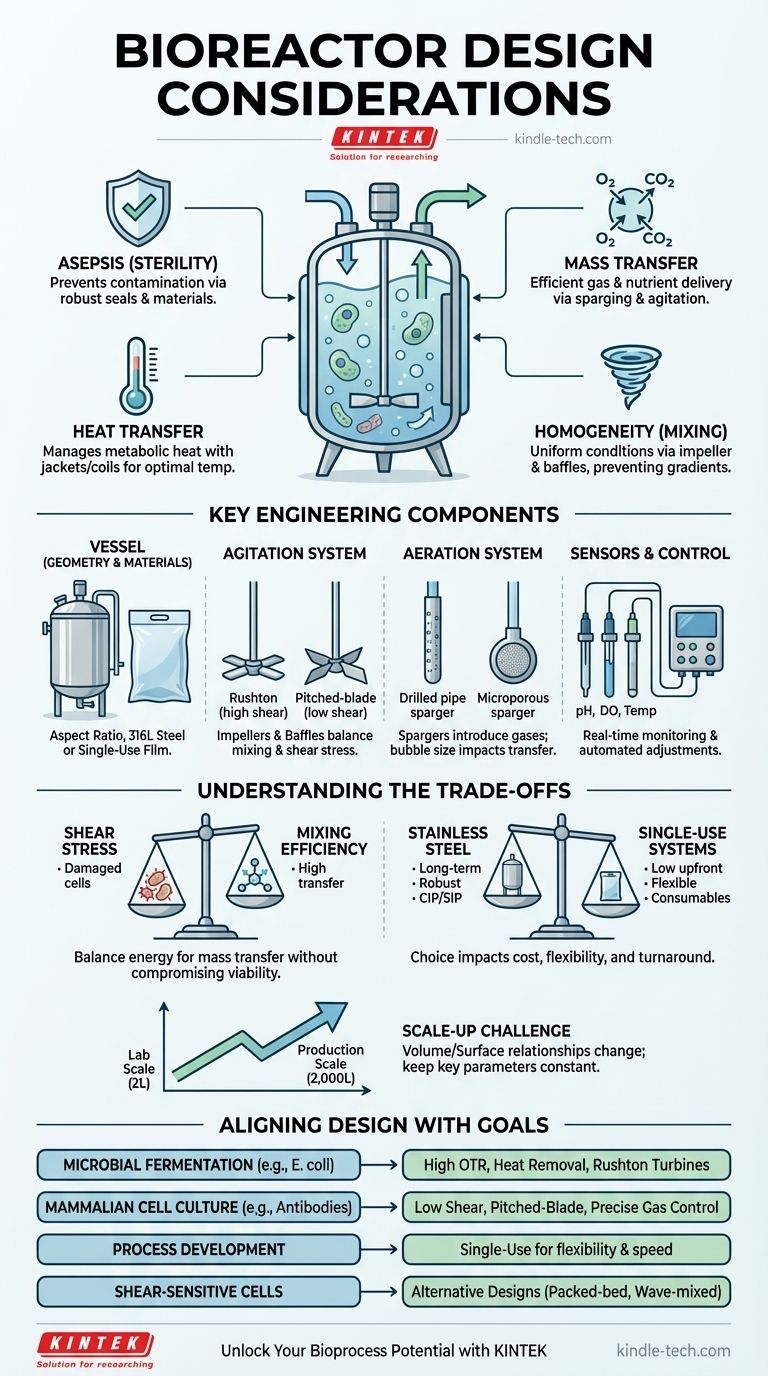
Ähnliche Produkte
- Anpassbare Labor-Hochtemperatur-Hochdruckreaktoren für vielfältige wissenschaftliche Anwendungen
- Viskoser Hochdruckreaktor zur In-situ-Beobachtung
- Anpassbare Hochdruckreaktoren für fortschrittliche wissenschaftliche und industrielle Anwendungen
- Edelstahl-Hochdruck-Autoklav-Reaktor Labor-Druckreaktor
- Hochdruck-Laborautoklav-Reaktor für Hydrothermalsynthese
Andere fragen auch
- Was ist die Bedeutung einer konstanten Temperaturumgebung bei Wasserstoffentwicklungsexperimenten mit Mg-2Ag-Legierungen?
- Welche experimentellen Bedingungen bietet ein HTHP-Reaktor für Coiled Tubing? Optimierung der Korrosionssimulation unter Tage
- Warum ist Pyrolyse teuer? Die hohen Kosten der fortschrittlichen Abfallumwandlung entschlüsselt
- Warum ist Argon besser als Stickstoff für eine inerte Atmosphäre? Absolute Reaktivität & Stabilität gewährleisten
- Wie steuern Sie hohen Druck in einem Reaktor? Ein Leitfaden für sicheren & stabilen Betrieb





