Ja, absolut. Eine einzelne chemische Reaktion kann oft gleichzeitig als mehrere Reaktionstypen klassifiziert werden. Dies ist ein häufiger Verwirrungspunkt, da die Einführungschemie Reaktionstypen oft als sich gegenseitig ausschließende Kategorien darstellt, aber ein fortgeschritteneres Verständnis zeigt, dass es sich lediglich um unterschiedliche Blickwinkel handelt, um dasselbe chemische Ereignis zu analysieren.
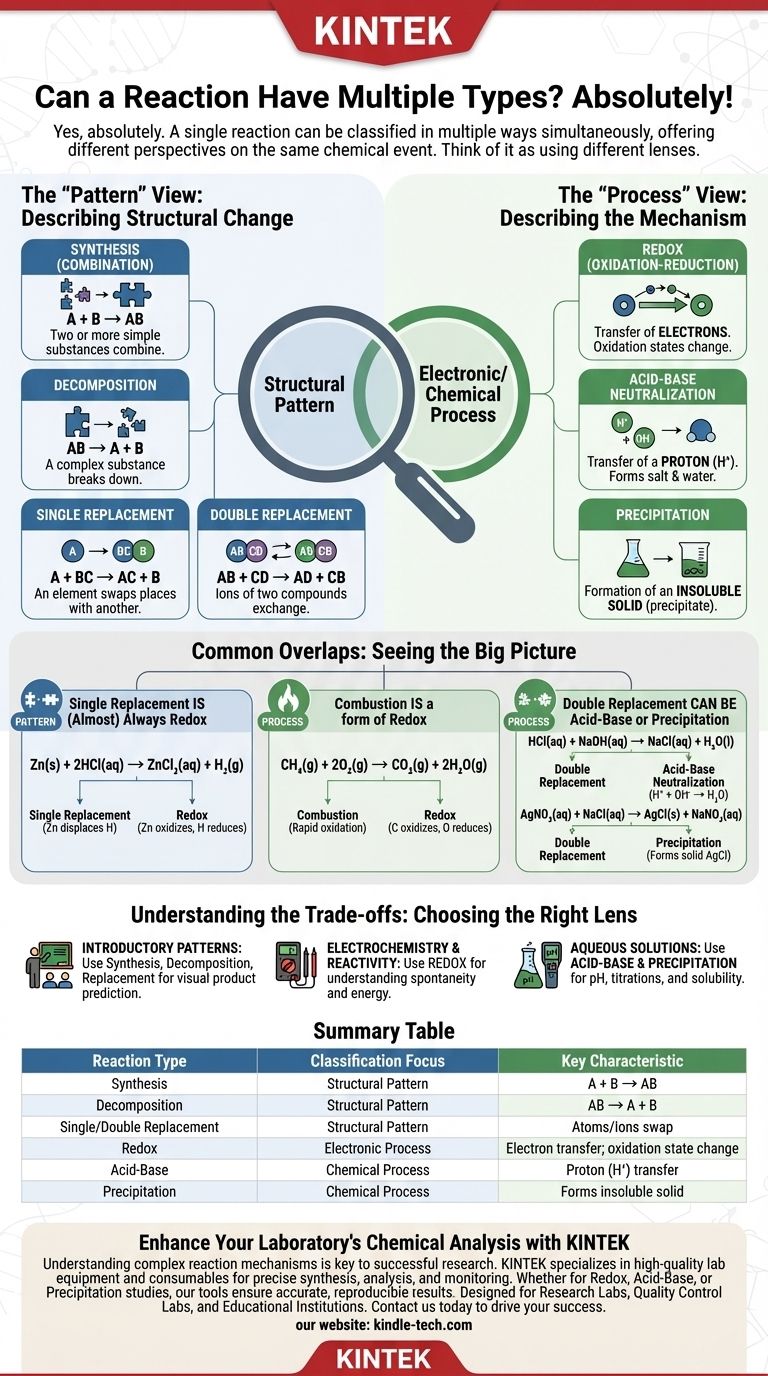
Der Schlüssel liegt darin zu verstehen, dass einige Reaktionstypen das strukturelle Muster beschreiben, wie sich Atome neu anordnen (wie Synthese oder Zersetzung), während andere den zugrunde liegenden elektronischen oder chemischen Prozess beschreiben (wie Redox oder Säure-Base). Eine einzelne Reaktion kann sowohl ein bestimmtes Muster als auch einen bestimmten Prozess aufweisen.

Warum einfache Bezeichnungen nicht ausreichen
Die Art und Weise, wie wir Reaktionen klassifizieren, hängt davon ab, was wir über sie verstehen wollen. Die einfachen Kategorien, die man zuerst lernt, sind nützlich, um visuelle Muster zu erkennen, aber sie erklären nicht immer die grundlegende chemische Veränderung.
Die „Muster“-Sichtweise: Beschreibung der strukturellen Veränderung
Früh in Ihrer chemischen Ausbildung lernen Sie, Reaktionen danach zu erkennen, wie die Reaktanten Produkte bilden. Diese Kategorien beschreiben die Gesamtform der Transformation.
Die wichtigsten musterbasierten Typen sind:
- Synthese (oder Kombination): Zwei oder mehr einfache Substanzen verbinden sich zu einem komplexeren Produkt (
A + B → AB). - Zersetzung: Eine komplexe Substanz zerfällt in einfachere (
AB → A + B). - Einfache Substitution (oder Verdrängung): Ein Element tauscht seinen Platz mit einem anderen in einer Verbindung (
A + BC → AC + B). - Doppelte Substitution (oder Metathese): Die Ionen zweier Verbindungen tauschen die Plätze, um zwei neue Verbindungen zu bilden (
AB + CD → AD + CB).
Diese Bezeichnungen sind hervorragend geeignet, um Produkte schnell anhand eines bekannten Musters vorherzusagen.
Die „Prozess“-Sichtweise: Beschreibung des Mechanismus
Anspruchsvollere Klassifizierungen beschreiben, wie die Transformation auf molekularer oder elektronischer Ebene abläuft. Sie konzentrieren sich auf den grundlegenden Prozess, der die Reaktion antreibt.
Die wichtigsten prozessbasierten Typen umfassen:
- Redox (Oxidations-Reduktion): Dieser Typ beinhaltet den Transfer von Elektronen. Die Oxidationszahlen eines oder mehrerer Elemente ändern sich während der Reaktion.
- Säure-Base-Neutralisation: Eine Säure und eine Base reagieren, typischerweise unter Übertragung eines Protons (H⁺-Ions), um ein Salz und Wasser zu bilden.
- Fällung: Zwei wässrige Lösungen werden gemischt und es bildet sich ein unlöslicher Feststoff (ein Niederschlag).
Diese Bezeichnungen sind unerlässlich, um die zugrunde liegenden treibenden Kräfte einer Reaktion zu verstehen.
Häufige Überschneidungen, denen Sie begegnen werden
Zu sehen, wie diese Kategorien sich überschneiden, ist der beste Weg, Ihr Verständnis zu festigen. Die meisten Reaktionen, denen Sie begegnen, haben mehr als eine gültige Bezeichnung.
Einfache Substitution ist (fast) immer Redox
Betrachten Sie die Reaktion von Zinkmetall mit Salzsäure:
Zn(s) + 2HCl(aq) → ZnCl₂(aq) + H₂(g)
Dies ist eine klassische einfache Substitutionsreaktion, da Zink Wasserstoff verdrängt. Es ist jedoch auch eine Redoxreaktion, da sich die Oxidationszahlen ändern: Zink wird oxidiert (0 auf +2) und Wasserstoff wird reduziert (+1 auf 0).
Verbrennung ist eine Form von Redox
Die Verbrennung von Methan ist ein gutes Beispiel:
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g)
Obwohl wir dies als Verbrennung bezeichnen, ist es im Grunde auch eine Redoxreaktion. Kohlenstoff wird oxidiert (-4 auf +4) und Sauerstoff wird reduziert (0 auf -2).
Doppelte Substitution kann Säure-Base oder Fällung sein
Betrachten Sie die Neutralisation von Salzsäure mit Natriumhydroxid:
HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)
Dies ist eine doppelte Substitutionsreaktion; Na⁺ und H⁺ tauschen die Plätze. Wichtiger noch, es ist das definitive Beispiel für eine Säure-Base-Neutralisation.
Ebenso beim Mischen von Silbernitrat und Natriumchlorid:
AgNO₃(aq) + NaCl(aq) → AgCl(s) + NaNO₃(aq)
Dies passt in das Muster der doppelten Substitution, aber sein bemerkenswertestes Merkmal ist die Bildung eines Feststoffs, was es zu einer Fällungsreaktion macht.
Die Abwägungen verstehen: Der Zweck der Klassifizierung
Die Wahl einer Bezeichnung ist nicht die Suche nach der einen „richtigen“ Antwort. Es geht darum, die beschreibendste und nützlichste Bezeichnung für Ihr spezifisches Ziel zu verwenden.
Die Begrenzung einfacher Muster
Die Klassifizierung einer Reaktion als „einfache Substitution“ sagt Ihnen, was mit den Atomen passiert ist, erklärt aber nicht, warum es passiert ist. Es erklärt nicht, warum Zink mit HCl reagiert, Kupfer aber nicht.
Die Stärke mechanistischer Bezeichnungen
Die Identifizierung derselben Reaktion als „Redox“ liefert viel tiefere Einblicke. Sie ermöglicht es Ihnen, Konzepte wie Aktivitätsreihen oder Standardelektrodenpotentiale zu verwenden, um vorherzusagen, ob die Reaktion spontan abläuft, und um die beteiligte Energie zu quantifizieren. Die Redox-Bezeichnung erklärt das „Warum“.
Die richtige Wahl für Ihr Ziel treffen
Verwenden Sie die Klassifizierung, die Ihrem Zweck am besten dient. Das Ziel ist nicht, eine einzige, ausschließliche Bezeichnung zu finden, sondern die relevanteste anzuwenden.
- Wenn Ihr Hauptaugenmerk auf der Erkennung grundlegender Muster in einem Einführungskurs liegt: Halten Sie sich an Synthese, Zersetzung und einfache/doppelte Substitution, um Produkte visuell vorherzusagen.
- Wenn Ihr Hauptaugenmerk auf Elektrochemie oder der Vorhersage der Reaktivität liegt: Die Klassifizierung als Redox ist die wichtigste Perspektive.
- Wenn Ihr Hauptaugenmerk auf der Arbeit mit wässrigen Lösungen, pH-Wert und Titrationen liegt: Die Klassifizierung von Reaktionen als Säure-Base oder Fällung ist der nützlichste Ansatz.
Letztendlich hängt die Verwendung der richtigen Bezeichnung von der spezifischen Frage ab, die Sie sich zur chemischen Umwandlung stellen.
Zusammenfassungstabelle:
| Reaktionstyp | Fokus der Klassifizierung | Schlüsselmerkmal |
|---|---|---|
| Synthese | Strukturelles Muster | Zwei oder mehr Reaktanten verbinden sich zu einem Produkt (A + B → AB) |
| Zersetzung | Strukturelles Muster | Eine Verbindung zerfällt in einfachere Substanzen (AB → A + B) |
| Einfache/Doppelte Substitution | Strukturelles Muster | Atome oder Ionen tauschen zwischen Verbindungen |
| Redox | Elektronischer Prozess | Beinhaltet Elektronentransfer; Oxidationszahlen ändern sich |
| Säure-Base | Chemischer Prozess | Beinhaltet Protonentransfer (H⁺) |
| Fällung | Chemischer Prozess | Bildung eines unlöslichen Feststoffs aus wässrigen Lösungen |
Verbessern Sie die chemische Analyse Ihres Labors mit KINTEK
Das Verständnis komplexer Reaktionsmechanismen ist der Schlüssel zu erfolgreicher Forschung und Entwicklung. Bei KINTEK sind wir darauf spezialisiert, qualitativ hochwertige Laborgeräte und Verbrauchsmaterialien anzubieten, die präzise chemische Synthese, Analyse und Prozessüberwachung unterstützen. Ob Sie an Redoxreaktionen, Säure-Base-Titrationen oder Fällungsstudien arbeiten, unsere zuverlässigen Werkzeuge helfen Ihnen, genaue und reproduzierbare Ergebnisse zu erzielen.
Unsere Produkte sind konzipiert für:
- Forschungslabore, die eine präzise Temperaturkontrolle für Synthese- und Zersetzungsreaktionen benötigen.
- Qualitätskontrolllabore, die konsistente Geräte für Säure-Base- und Fällungsanalysen benötigen.
- Bildungseinrichtungen, die langlebige und einfach zu bedienende Apparaturen zur Lehre grundlegender und fortgeschrittener Reaktionstypen suchen.
Lassen Sie KINTEK Ihr vertrauenswürdiger Partner bei der Erweiterung der Fähigkeiten Ihres Labors sein. Kontaktieren Sie uns noch heute, um Ihre spezifischen Anforderungen zu besprechen und herauszufinden, wie unsere Lösungen Ihren Erfolg vorantreiben können.
Visuelle Anleitung