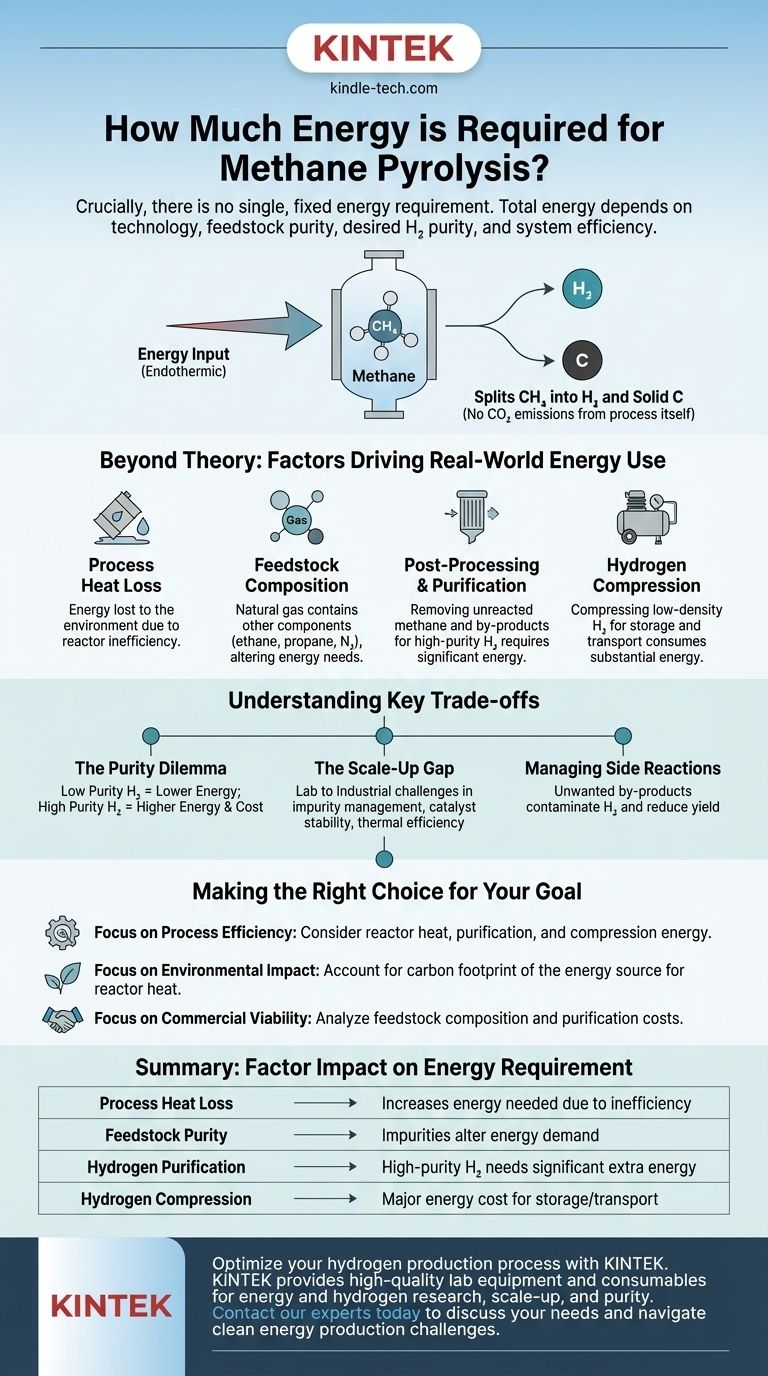
Entscheidend ist, dass es keinen einzigen, festen Energiebedarf für die Methanpyrolyse gibt. Die benötigte Gesamtenergie ist stark variabel und hängt von der spezifischen verwendeten Technologie, der Reinheit des Erdgas-Ausgangsmaterials, der gewünschten Reinheit des Endprodukts Wasserstoff und der Effizienz des Gesamtsystems ab.
Die theoretische Energie, die zur Spaltung der chemischen Bindungen von Methan erforderlich ist, ist nur der Ausgangspunkt. Die praktische, reale Energiekosten sind erheblich höher, angetrieben durch Prozesswärmeverluste, Gasreinigung und den energieintensiven Schritt der Wasserstoffkompression.

Der Kern der thermischen Nachfrage
Die Methanpyrolyse ist ein endothermer Prozess, was bedeutet, dass er eine kontinuierliche Energiezufuhr benötigt, um zu funktionieren. Diese Energie wird verwendet, um Methan (CH₄) auf hohe Temperaturen zu erhitzen, wodurch die starken chemischen Bindungen zwischen Kohlenstoff- und Wasserstoffatomen aufgebrochen werden.
Was die Energie bewirkt
Das Hauptziel der Energiezufuhr ist die Spaltung des Methanmoleküls in seine Bestandteile: Wasserstoffgas (H₂) und festen Kohlenstoff (C). Dies geschieht, ohne dass das Methan mit Sauerstoff reagiert, weshalb der Prozess selbst keine CO₂-Emissionen verursacht.
Jenseits der Theorie: Faktoren, die den realen Energieverbrauch bestimmen
Die grundlegende thermische Energie ist nur ein Teil des Puzzles. Bei jeder industriellen Anwendung kommen mehrere andere Faktoren hinzu, die erhebliche Energiekosten für den Gesamtprozess verursachen.
Prozesswärmeverluste
Kein industrieller Prozess ist perfekt isoliert. Ein Teil der dem Reaktor zugeführten thermischen Energie geht unweigerlich an die Umgebung verloren. Diese Ineffizienz bedeutet, dass mehr Energie zugeführt werden muss, als theoretisch für die Reaktion erforderlich ist.
Zusammensetzung des Ausgangsmaterials (Erdgas vs. Methan)
Während in der Forschung häufig reines Methan verwendet wird, setzen Industrieanlagen Erdgas ein. Erdgas enthält andere Bestandteile wie Ethan, Propan und Stickstoff. Diese zusätzlichen Substanzen können die Reaktion beeinflussen und möglicherweise unterschiedliche Betriebstemperaturen oder katalytische Prozesse erfordern, wodurch sich der Energiebedarf ändert.
Nachbearbeitung und Reinigung
Der Gasstrom, der den Reaktor verlässt, ist kein reiner Wasserstoff. Er enthält nicht umgesetztes Methan und andere Kohlenwasserstoff-Nebenprodukte. Wenn hochreiner Wasserstoff das Ziel ist (z. B. für Petrochemikalien), muss dieses Gemisch energieintensive Reinigungs- und Trennschritte durchlaufen.
Wasserstoffkompression
Wasserstoff ist das leichteste Element, was bedeutet, dass er eine sehr geringe Dichte aufweist. Um ihn effektiv zu speichern oder zu transportieren, muss das resultierende Wasserstoffgas stark komprimiert werden. Dieser mechanische Prozess verbraucht eine beträchtliche Menge an elektrischer Energie und ist ein Hauptbestandteil des gesamten Energiebudgets.
Verständnis der wichtigsten Kompromisse
Die Bewertung der Methanpyrolyse erfordert das Verständnis der praktischen Herausforderungen, die sich direkt auf ihre Energieeffizienz und wirtschaftliche Tragfähigkeit auswirken.
Das Reinheitsdilemma
Die Energie, die zur Erzeugung eines gemischten „unreinen“ Wasserstoffstroms erforderlich ist, ist weitaus geringer als die, die für 99,9 %+ reinen Wasserstoff benötigt wird. Die Entscheidung für höhere Reinheitsgrade bringt erhebliche Energie- und Kapitalkosten mit sich, die mit fortschrittlichen Gastrennungstechnologien verbunden sind.
Die Skalierungslücke
Es besteht eine deutliche Lücke zwischen kontrollierten Laborexperimenten und der industriellen Großserienrealität. Herausforderungen im Zusammenhang mit der Handhabung von Verunreinigungen im Erdgas, der Gewährleistung der Katalysatorstabilität und der Aufrechterhaltung der thermischen Effizienz werden im industriellen Maßstab weitaus ausgeprägter.
Umgang mit Nebenreaktionen
Unerwünschte Nebenreaktionen können andere Kohlenwasserstoffe oder aromatische Verbindungen erzeugen. Diese Nebenprodukte verunreinigen nicht nur den Wasserstoffstrom, was die Reinigung schwieriger und energieintensiver macht, sondern stellen auch einen Verlust an potenziellem Wasserstoffertrag aus dem Ausgangsmaterial dar.
Die richtige Wahl für Ihr Ziel treffen
Um den Energiebedarf für eine bestimmte Anwendung zu bewerten, müssen Sie über die Kernreaktion hinausblicken und das gesamte System berücksichtigen.
- Wenn Ihr Hauptaugenmerk auf der Prozesseffizienz liegt: Ihre Analyse muss die gesamte Energiezufuhr berücksichtigen, einschließlich Wärme für den Reaktor, Strom für die Reinigung und der erheblichen Energie, die durch die Wasserstoffkompression verbraucht wird.
- Wenn Ihr Hauptaugenmerk auf der Umweltauswirkung liegt: Obwohl die Pyrolyse-Reaktion CO₂-frei ist, müssen Sie den CO₂-Fußabdruck der Energiequelle berücksichtigen, die zum Heizen des Reaktors verwendet wird. Wenn zur Erzeugung dieser Wärme Erdgas verbrannt wird, entstehen dem Prozess immer noch Emissionen.
- Wenn Ihr Hauptaugenmerk auf der kommerziellen Tragfähigkeit liegt: Eine detaillierte Analyse Ihres Erdgas-Ausgangsmaterials ist von entscheidender Bedeutung. Seine spezifische Zusammensetzung bestimmt die Komplexität und die Energiekosten der Reinigungskette, die erforderlich ist, um die Wasserstoffreinheitsspezifikationen Ihres Kunden zu erfüllen.
Letztendlich erfordert das Verständnis der wahren Energiekosten der Methanpyrolyse eine ganzheitliche Betrachtung der gesamten Produktionskette, von der Erdgasquelle bis zum endgültigen komprimierten Wasserstoffprodukt.
Zusammenfassungstabelle:
| Faktor | Auswirkung auf den Energiebedarf |
|---|---|
| Prozesswärmeverluste | Erhöht den benötigten Energieaufwand aufgrund von Reaktorineffizienz |
| Reinheit des Ausgangsmaterials | Verunreinigungen im Erdgas können den Energiebedarf verändern |
| Wasserstoffreinigung | Hochreiner H₂ erfordert erhebliche zusätzliche Energie |
| Wasserstoffkompression | Ein Hauptenergiekostenfaktor für Lagerung und Transport |
Optimieren Sie Ihren Wasserstoffproduktionsprozess mit KINTEK.
Das Verständnis der komplexen Energiedynamik der Methanpyrolyse ist der Schlüssel zur Entwicklung eines effizienten und kostengünstigen Betriebs. Die richtige Laborausrüstung ist unerlässlich für genaue Forschung, Prozessentwicklung und Qualitätskontrolle.
KINTEK ist spezialisiert auf die Bereitstellung hochwertiger Laborgeräte und Verbrauchsmaterialien zur Unterstützung Ihrer Energie- und Wasserstoffforschung. Egal, ob Sie vom Labor in den Pilotbetrieb übergehen oder die Produktreinheit sicherstellen, unsere Lösungen helfen Ihnen, zuverlässige Ergebnisse zu erzielen und die Prozesseffizienz zu verbessern.
Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie KINTEK Ihre spezifischen Laboranforderungen unterstützen und Ihnen helfen kann, die Herausforderungen der sauberen Energieerzeugung zu meistern.
Visuelle Anleitung
Ähnliche Produkte
- Elektrischer Drehrohrofen Kleiner Drehrohrofen Biomasse-Pyrolyseanlage
- Elektrischer Drehrohrofen Kontinuierlicher Betrieb Kleine Drehrohrofen Heizpyrolyseanlage
- Elektrische Drehrohrofen-Pyrolyseofenanlage Kalzinator Kleiner Drehrohrofen Rotierender Ofen
- Anpassbare Labor-Hochtemperatur-Hochdruckreaktoren für vielfältige wissenschaftliche Anwendungen
- Mini-Edelstahl-Hochdruck-Autoklavenreaktor für den Laboreinsatz
Andere fragen auch
- Wie werden Drehrohröfen beheizt? Erklärung der direkten vs. indirekten Heizmethoden
- Bei welcher Temperatur findet die Pyrolyse statt? Ein Leitfaden zur Steuerung Ihres Produktausstoßes
- Was sind die Merkmale der Gleit-, Einsink- und Rollbewegungsmodi von Schüttgütern? Optimieren Sie Ihren Drehprozess
- Was sind die Reaktoren für die schnelle Pyrolyse? Auswahl des richtigen Systems für maximale Bioöl-Ausbeute
- Ist ein Drehrohrofen ein Ofen? Entdecken Sie die Hauptunterschiede für die industrielle Verarbeitung












