In der experimentellen Wissenschaft sind wir oft besessen von den Variablen, die wir einführen: die Spannung, der Katalysator, die Temperatur.
Wir denken selten genug über die Variablen nach, die wir nicht einführen wollen.
Ein Fingerabdruck auf einer Elektrode. Ein mikroskopischer Bruch im Quarz. Ein zufälliges Sauerstoffmolekül, das in der Lösung gelöst ist.
Das sind die stillen Killer von Daten. Sie verwandeln ein deterministisches Experiment in ein probabilistisches Durcheinander.
Die richtige Vorbereitung einer reinen Quarz-Elektrolysezelle ist keine bloße lästige Pflicht vor Beginn der "eigentlichen Arbeit". Sie ist das Fundament der Arbeit selbst. Wie der Chirurg Atul Gawande über den Operationssaal argumentieren würde: Erfolg wird selten durch einen einzigen genialen Schachzug definiert, sondern durch die unerbittliche Eliminierung von Fehlerquellen, bevor der Eingriff überhaupt beginnt.
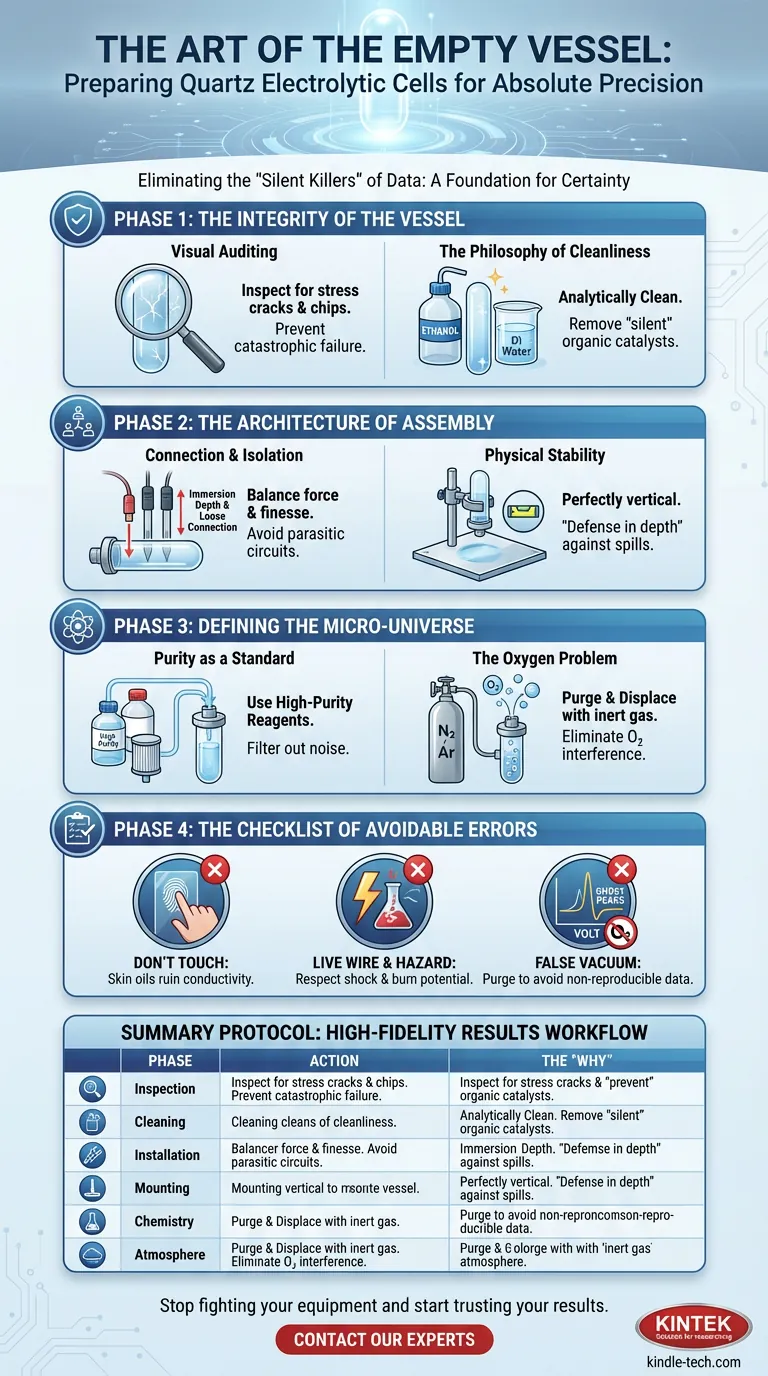
Hier erfahren Sie, wie Sie Ihrem elektrochemischen Aufbau Sicherheit verleihen.
Die Integrität des Gefäßes
Quarz ist ein Material, das Ingenieure lieben. Es bietet optische Klarheit, thermische Beständigkeit und chemische Inertheit. Aber es ist spröde und verzeiht keine mechanischen Belastungen.
Bevor Sie sich mit der Chemie befassen, müssen Sie die Physik Ihres Behälters überprüfen.
Visuelle Prüfung
Beginnen Sie mit einer sorgfältigen Inspektion. Achten Sie auf Spannungsrisse, Absplitterungen oder Brüche, insbesondere an den Verbindungsstellen und den Elektrodenanschlüssen.
Ein kompromittiertes Gefäß ist eine tickende Zeitbombe. Unter thermischer Schwankung oder mechanischer Belastung wird ein Haarriss zu einem Leck. Ein Leck wird zu einem katastrophalen Versagen.
Die Philosophie der Sauberkeit
"Sauber" ist ein relativer Begriff. In Ihrer Küche ist ein gewaschener Teller sauber. In der Elektrochemie ist derselbe Teller eine Katastrophenzone für organische Rückstände.
Sie benötigen eine analytisch saubere Oberfläche.
- Das Lösungsmittel: Waschen Sie mit hochreinem Ethanol, um organische Öle aufzulösen.
- Das Spülen: Spülen Sie anschließend mehrmals mit deionisiertem (DI) Wasser nach.
- Das Ziel: Sie entfernen unsichtbare Katalysatoren. Wenn ein Rückstand verbleibt, wird er zum Teilnehmer Ihrer Redoxreaktion.
Die Architektur der Montage
Sobald das Gefäß intakt ist, müssen Sie die Akteure einführen: die Elektroden.
Diese Phase erfordert ein Gleichgewicht zwischen Kraft und Finesse. Die Elektroden – Arbeits-, Referenz- und Gegenelektrode – müssen mit geometrischer Präzision in ihre vorgesehenen Anschlüsse eingebaut werden.
Verbindung und Isolierung
Die Verbindungen müssen dicht genug sein, um atmosphärische Lecks zu verhindern, aber locker genug, um die Quarzanschlüsse nicht zu belasten.
Achten Sie entscheidend auf die Eintauchtiefe. Der aktive Bereich muss eingetaucht sein, aber der Elektrolyt darf niemals die oberen Anschlussstifte berühren. Wenn die Flüssigkeit den Anschlusspunkt berührt, erzeugen Sie einen parasitären Stromkreis. Sie messen nicht mehr die Chemie; Sie messen die Korrosion eines Steckverbinders.
Physikalische Stabilität
Die Schwerkraft ist eine Variable, die Sie nicht kontrollieren können, also müssen Sie sie managen.
Befestigen Sie das Gefäß auf einem Laborständer. Es muss perfekt vertikal ausgerichtet sein. Wenn Sie mit korrosiven Elektrolyten arbeiten, legen Sie eine chemikalienbeständige Unterlage unter den Aufbau. Das ist "Tiefenverteidigung" – Planung für ein Versagen, das Sie hoffentlich nie erleben werden.
Das Mikrouniversum definieren
Nun führen Sie die Chemie ein. Hier verwandeln Sie sich vom Physiker zum Chemiker.
Sie gießen nicht einfach Flüssigkeit in ein Glas; Sie schaffen eine kontrollierte Atmosphäre – ein temporäres Universum, in dem nur bestimmte physikalische Gesetze gelten.
Reinheit als Standard
Verwenden Sie hochreine Reagenzien und DI-Wasser. Wenn Ihr Wasser Spuren von Metallionen enthält, wandern diese zu Ihrer Elektrode und erscheinen in Ihren Daten.
Filtern Sie die Lösung, um suspendierte Mikropartikel zu entfernen. Rauschen in der Lösung bedeutet Rauschen im Signal.
Das Sauerstoffproblem
Sauerstoff ist der ungebetene Gast bei jeder elektrochemischen Party. Er ist elektrochemisch aktiv und liebt es, Reduktionsreaktionen zu stören.
Wenn Ihr Experiment empfindlich ist (und die meisten sind es):
- Spülen: Spülen Sie das verschlossene Gefäß mit einem Inertgas wie hochreinem Stickstoff oder Argon.
- Verdrängen: Stellen Sie sicher, dass die Innenluft vollständig ersetzt ist, bevor das Experiment beginnt.
Die Checkliste vermeidbarer Fehler
Morgan Housel schreibt oft, dass reich werden bedeutet, nicht dumm zu sein. Ebenso bedeutet gute Daten oft, keine ungezwungenen Fehler zu machen.
Die meisten Fehler im Labor sind nicht auf komplexe theoretische Lücken zurückzuführen, sondern auf einfache Verfahrensmängel.
- Der Todesgriff: Berühren Sie niemals die Innenflächen oder aktiven Elektrodenbereiche mit bloßen Händen. Hautöle sind isolierende Schichten, die die Leitfähigkeit ruinieren.
- Der stromführende Draht: Elektrochemische Systeme sind stromführende Stromkreise. Respektieren Sie die Stromschlaggefahr und das Potenzial für chemische Verätzungen.
- Das falsche Vakuum: Das Versäumnis, Sauerstoff zu spülen, führt zu nicht reproduzierbaren "Geisterspitzen" in Ihren Voltamogrammen.
Zusammenfassendes Protokoll
Die folgende Tabelle skizziert den systematischen Arbeitsablauf, der für hochpräzise Ergebnisse erforderlich ist.
| Phase | Aktion | Das "Warum" |
|---|---|---|
| 1. Inspektion | Auf Absplitterungen und Spannungsrisse prüfen. | Verhindert mechanisches Versagen und Lecks. |
| 2. Reinigung | Ethanolwäsche + DI-Wasser-Spülung. | Entfernt "stille" organische Katalysatoren. |
| 3. Installation | Elektroden befestigen; Tiefe prüfen. | Verhindert Kurzschlüsse und parasitäre Korrosion. |
| 4. Montage | Vertikale Ausrichtung + Tropfschutz. | Gewährleistet physische Stabilität und Sicherheit. |
| 5. Chemie | Hochreine Reagenzien + Filterung. | Maximiert das Signal-Rausch-Verhältnis. |
| 6. Atmosphäre | Inertgas-Spülung (N₂/Ar). | Eliminiert Sauerstoffstörungen. |
Schlussfolgerung
Der Unterschied zwischen einem fehlgeschlagenen Lauf und einem veröffentlichungsfähigen Ergebnis liegt oft in der Vorbereitung. Indem Sie den Aufbau als Ritual und nicht als lästige Pflicht behandeln, stellen Sie sicher, dass die einzigen Überraschungen in Ihren Daten die wissenschaftlichen Durchbrüche sind, nach denen Sie gesucht haben.
Bei KINTEK verstehen wir, dass Ihre Ausrüstung die Bühne für Ihre Entdeckung ist. Wir sind spezialisiert auf hochreine Laborgeräte, von makellosen Quarzgefäßen bis hin zu Präzisionselektroden, die entwickelt wurden, um Hardware-Variablen zu eliminieren, damit Sie sich auf die Wissenschaft konzentrieren können.
Hören Sie auf, gegen Ihre Ausrüstung zu kämpfen, und fangen Sie an, Ihren Ergebnissen zu vertrauen. Kontaktieren Sie unsere Experten, um noch heute Ihre spezifischen experimentellen Bedürfnisse zu besprechen.
Visuelle Anleitung
Ähnliche Produkte
- Elektrochemische Quarz-Elektrolysezelle für elektrochemische Experimente
- Elektrochemische Elektrolysezelle mit fünf Anschlüssen
- PTFE Elektrolysezelle Elektrochemische Zelle Korrosionsbeständig Abgedichtet und Nicht Abgedichtet
- Elektrochemische Elektrolysezelle zur Beschichtungsbewertung
- Flache Korrosions-Elektrolysezelle
Ähnliche Artikel
- Die Architektur der Transparenz: Sicherheit und Präzision in der Quarz-Elektrolyse meistern
- Elektrochemie Die Wissenschaft hinter elektrochemischen Zellen
- Die Geometrie der Kontrolle: Warum Millimeter in der Elektrochemie entscheidend sind
- Die Architektur der Stille: Warum Quarz elektrochemische Präzision definiert
- Elektrochemische Zellen: Elektrizität erzeugen und Reaktionen antreiben




















