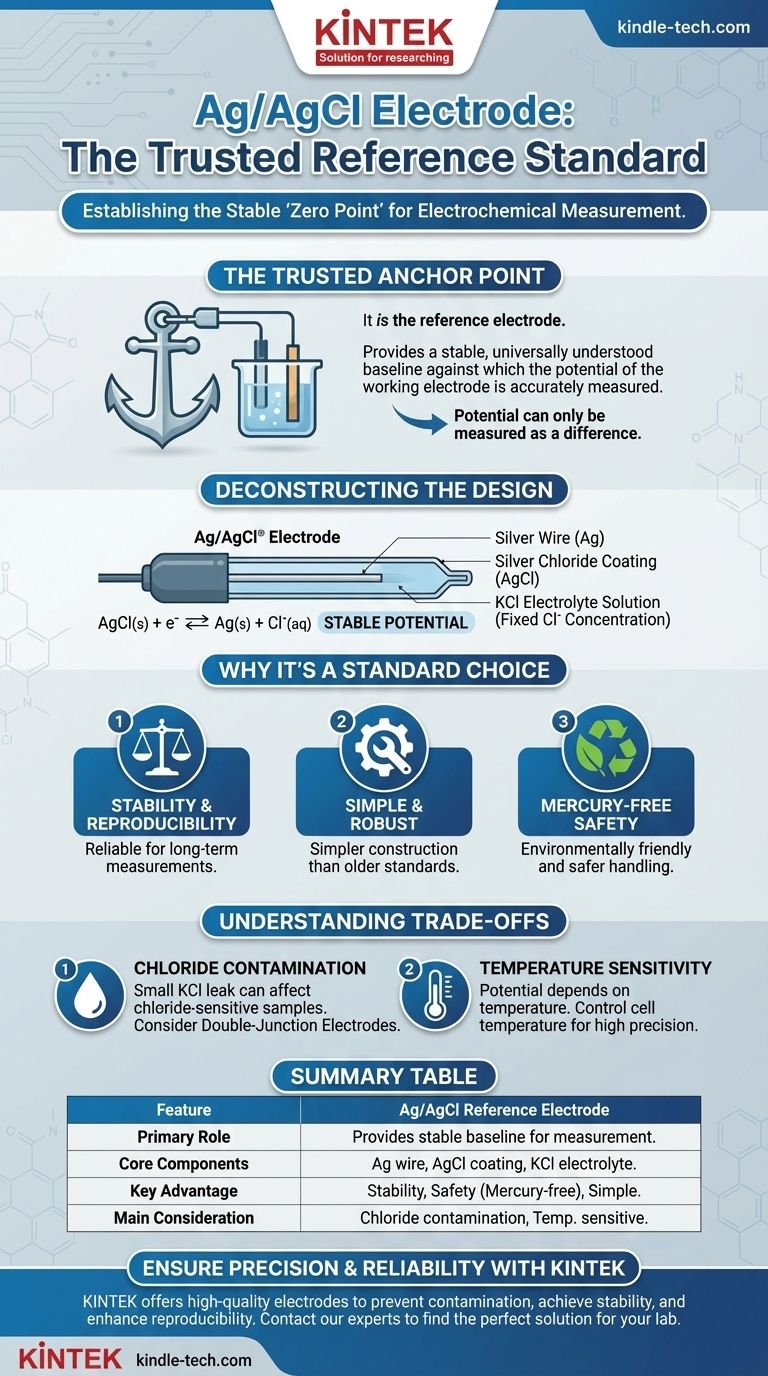
Kurz gesagt, die Silber/Silberchlorid (Ag/AgCl)-Elektrode wird nicht gegen eine Referenzelektrode gemessen; sie ist die Referenzelektrode. Sie fungiert als stabile, international anerkannte Standard-Halbzelle. Ihr Zweck ist es, eine konstante und zuverlässige Potenzial-Basislinie bereitzustellen, gegen die das Potenzial einer anderen Elektrode (der "Arbeitselektrode") genau gemessen werden kann.
Eine Referenzelektrode ist ein notwendiges Werkzeug in der Elektrochemie, da das Potenzial nur als Differenz zwischen zwei Punkten gemessen werden kann. Die Ag/AgCl-Elektrode bietet einen universell verständlichen, stabilen "Nullpunkt" für diese Messungen und gewährleistet, dass die Ergebnisse über verschiedene Experimente hinweg konsistent und vergleichbar sind.

Was macht eine Elektrode zu einer "Referenz"?
Um die Rolle der Ag/AgCl-Elektrode zu verstehen, ist es wichtig zu begreifen, warum überhaupt eine Referenz benötigt wird. Man kann das absolute Potenzial einer einzelnen Elektrode nicht messen; man kann nur die Spannungsdifferenz zwischen zwei Elektroden messen.
Die Notwendigkeit einer stabilen Basislinie
Bei jeder elektrochemischen Messung interessiert man sich für das sich ändernde Potenzial Ihrer Arbeitselektrode, wenn sie mit Ihrer Probe interagiert. Um diese Änderung genau zu messen, benötigen Sie eine zweite Elektrode, die ein konstantes, nicht schwankendes Potenzial aufweist. Dieser stabile Partner ist die Referenzelektrode.
Wie Stabilität erreicht wird
Die Stabilität einer Referenzelektrode beruht auf einem sorgfältig kontrollierten elektrochemischen Gleichgewicht. Es handelt sich um eine Halbzellenreaktion, deren Komponenten fixiert sind, was zu einem Potenzial führt, das sich nicht ändert, solange Bedingungen wie Temperatur und Konzentrationen der Komponenten aufrechterhalten werden.
Die Ag/AgCl-Elektrode im Detail
Die Ag/AgCl-Elektrode ist ein elegantes und robustes Design, das durch ein spezifisches chemisches Gleichgewicht ein hochstabiles Potenzial erreicht.
Kernkomponenten
Die Elektrode selbst ist bemerkenswert einfach. Sie besteht aus einem hochreinen Silberdraht (Ag), der mit einer Schicht aus Silberchlorid (AgCl) überzogen ist, einem in Wasser schwer löslichen Salz.
Der entscheidende Elektrolyt
Dieser beschichtete Draht wird dann in eine Lösung mit einer festen Konzentration von Chloridionen (Cl⁻) getaucht. Dies ist fast immer eine Kaliumchlorid (KCl)-Lösung, typischerweise in hoher Konzentration (z.B. 3M oder gesättigt).
Die reversible Reaktion
Das stabile Potenzial wird durch eine reversible chemische Reaktion an der Elektrodenoberfläche erzeugt:
AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq)
Da Silber und Silberchlorid fest sind und die Konzentration der Chloridionen in der Fülllösung festgelegt ist, bleibt das Potenzial dieser Halbreaktion konstant.
Warum Ag/AgCl eine Standardwahl ist
Die Ag/AgCl-Elektrode ist aus mehreren praktischen Gründen zur gebräuchlichsten Referenz in modernen Laboren geworden.
Stabilität und Reproduzierbarkeit
Die Elektrode liefert über lange Zeiträume ein hochstabiles und reproduzierbares Potenzial, was sie zu einem zuverlässigen Standard für Routine- und Forschungszwecke macht.
Einfache, robuste Konstruktion
Im Vergleich zu älteren Standards wie der gesättigten Kalomelelektrode (SCE) ist die Ag/AgCl-Elektrode einfacher herzustellen und weniger zerbrechlich, was zu ihrer weiten Verbreitung beiträgt.
Sicherheit und Umweltauswirkungen
Entscheidend ist, dass die Ag/AgCl-Elektrode quecksilberfrei ist. Dies macht sie wesentlich sicherer in der Handhabung und Entsorgung als quecksilberbasierte Elektroden, die in vielen Laboren aufgrund von Umwelt- und Gesundheitsbedenken inzwischen eingeschränkt sind.
Die Kompromisse verstehen
Obwohl sie der Industriestandard ist, ist keine Referenzelektrode für jede Situation perfekt. Es ist wichtig, sich ihrer Einschränkungen bewusst zu sein.
Chloridkontamination
Die Elektrode ist mit einem porösen Fritt ausgestattet, der den elektrischen Kontakt mit der Probenlösung ermöglicht. Mit der Zeit kann eine kleine Menge der KCl-Fülllösung in Ihre Probe gelangen. Dies ist problematisch, wenn Ihre Probe Spezies enthält, die mit Chlorid reagieren, wie z.B. Silberionen.
Temperaturempfindlichkeit
Das Potenzial der Ag/AgCl-Elektrode ist temperaturabhängig. Für hochpräzise Arbeiten muss die Temperatur der Zelle kontrolliert und angegeben werden, oder eine Temperaturkorrektur muss auf die Daten angewendet werden.
Die richtige Wahl für Ihre Messung treffen
Ihre Wahl der Referenzelektrode hängt vollständig von der chemischen Natur Ihres Experiments und dem erforderlichen Präzisionsgrad ab.
- Wenn Ihr Hauptaugenmerk auf der allgemeinen Laboranalyse liegt: Die Ag/AgCl-Elektrode ist die Standardwahl aufgrund ihres hervorragenden Gleichgewichts aus Stabilität, Sicherheit und Kosten.
- Wenn Ihre Probe empfindlich auf Chloridionen reagiert: Sie müssen eine "Doppelkammer"-Ag/AgCl-Elektrode oder eine Alternative wie die Quecksilber/Quecksilbersulfat (Hg/Hg₂SO₄)-Elektrode in Betracht ziehen, die eine chloridfreie Fülllösung verwendet.
- Wenn Sie höchste Präzision über einen Temperaturbereich hinweg benötigen: Sie müssen die Temperatur Ihrer elektrochemischen Zelle aktiv kontrollieren, unabhängig davon, welche Referenz Sie verwenden.
Letztendlich dient die Silber/Silberchlorid-Elektrode als der vertrauenswürdige, stabile Ankerpunkt, der für eine genaue und aussagekräftige elektrochemische Analyse unerlässlich ist.
Zusammenfassungstabelle:
| Merkmal | Ag/AgCl-Referenzelektrode |
|---|---|
| Primäre Rolle | Bietet eine stabile Potenzial-Basislinie zur Messung einer Arbeitselektrode. |
| Kernkomponenten | Silberdraht, beschichtet mit AgCl, getaucht in KCl-Elektrolytlösung. |
| Hauptvorteil | Hervorragende Stabilität, Sicherheit (quecksilberfrei) und einfache Konstruktion. |
| Hauptüberlegung | Potenzielle Chloridkontamination; temperaturempfindliches Potenzial. |
Stellen Sie sicher, dass Ihre elektrochemischen Messungen präzise und zuverlässig sind. Die richtige Referenzelektrode ist entscheidend für den Erfolg Ihres Labors. KINTEK ist spezialisiert auf hochwertige Laborgeräte und Verbrauchsmaterialien, einschließlich einer vollständigen Palette von Referenzelektroden, die auf Ihre spezifischen experimentellen Anforderungen zugeschnitten sind.
Unsere Experten können Ihnen helfen, die ideale Elektrode auszuwählen, um:
- Probenkontamination zu verhindern.
- Überlegene Messstabilität zu erreichen.
- Die Reproduzierbarkeit Ihrer Ergebnisse zu verbessern.
Kontaktieren Sie unser Team noch heute über unser sicheres Formular, um Ihre Anwendung zu besprechen und die perfekte Lösung für Ihr Labor zu finden.
Visuelle Anleitung
Ähnliche Produkte
- Referenzelektrode Kalomel Silberchlorid Quecksilbersulfat für Laborzwecke
- Kupfersulfat-Referenzelektrode für Laboranwendungen
- Goldplattierte Elektrode
- Gold-Elektrodenblech Gold-Elektrode
- Metall-Scheibenelektrode Elektrochemische Elektrode
Andere fragen auch
- Welche Art von Elektrode kann als Referenzpunkt verwendet werden? Wählen Sie die richtige für genaue Messungen
- Welche Elektrode wird als Referenzelektrode zur Messung von Halbzellenpotentialen verwendet? Das universelle Standardverständnis
- Was ist die Referenzelektrode in der Potentiometrie? Der Schlüssel zu stabilen & genauen Messungen
- Warum ist die Auswahl einer hochwertigen Referenzelektrode für die elektrochemische Synthese entscheidend? | KINTEK
- Was ist der Zweck der Referenzelektrode? Erreichen Sie stabile und genaue elektrochemische Messungen














