Die Illusion der Einfachheit
Im Labor konzentrieren wir uns oft auf die Komplexität des Elektrolyten. Wir messen Konzentrationen bis zum Mikrogramm. Wir sind besessen von Temperaturgradienten. Wir behandeln die chemische Lösung wie ein zartes Rezept, das die Berührung eines Meisterkochs erfordert.
Doch wir übersehen häufig die „Rohrleitungen“ des Experiments: die Drähte.
Das Anschließen einer Elektrolysezelle erscheint trivial. Roter Draht hier, schwarzer Draht dort. Es fühlt sich an, als würde man einen Toaster einstecken – spielt es wirklich eine Rolle, in welche Richtung er geht?
Bei der Elektrolyse ist das wichtiger als alles andere.
Die Elektrodenpolarität ist nicht nur ein Anschlussdetail. Sie ist das Kommando- und Kontrollzentrum Ihres Experiments. Sie ist der Unterschied zwischen der Schaffung eines Meisterwerks und der Auflösung Ihrer Ausrüstung.
Die Elektronenpumpe
Um die Polarität zu verstehen, müssen Sie aufhören, das Netzteil als Batterie zu betrachten, und anfangen, es als Pumpe zu betrachten.
Im Gegensatz zu einer galvanischen Zelle, bei der Chemie Elektrizität erzeugt, verwendet eine Elektrolysezelle Elektrizität, um Chemie gegen ihren Willen zu erzwingen. Die Reaktion ist nicht spontan. Sie braucht einen Anstoß.
Das Netzteil liefert diesen Anstoß, aber streng in einer Richtung:
- Es zieht Elektronen von einer Seite ab.
- Es drückt Elektronen zur anderen Seite.
Dieser Fluss bestimmt die Identität Ihrer Elektroden. Die Bezeichnungen „Anode“ und „Umpolung“ sind keine geografischen Orte in Ihrem Becherglas; es sind funktionale Rollen, die vollständig durch diesen Fluss definiert sind.
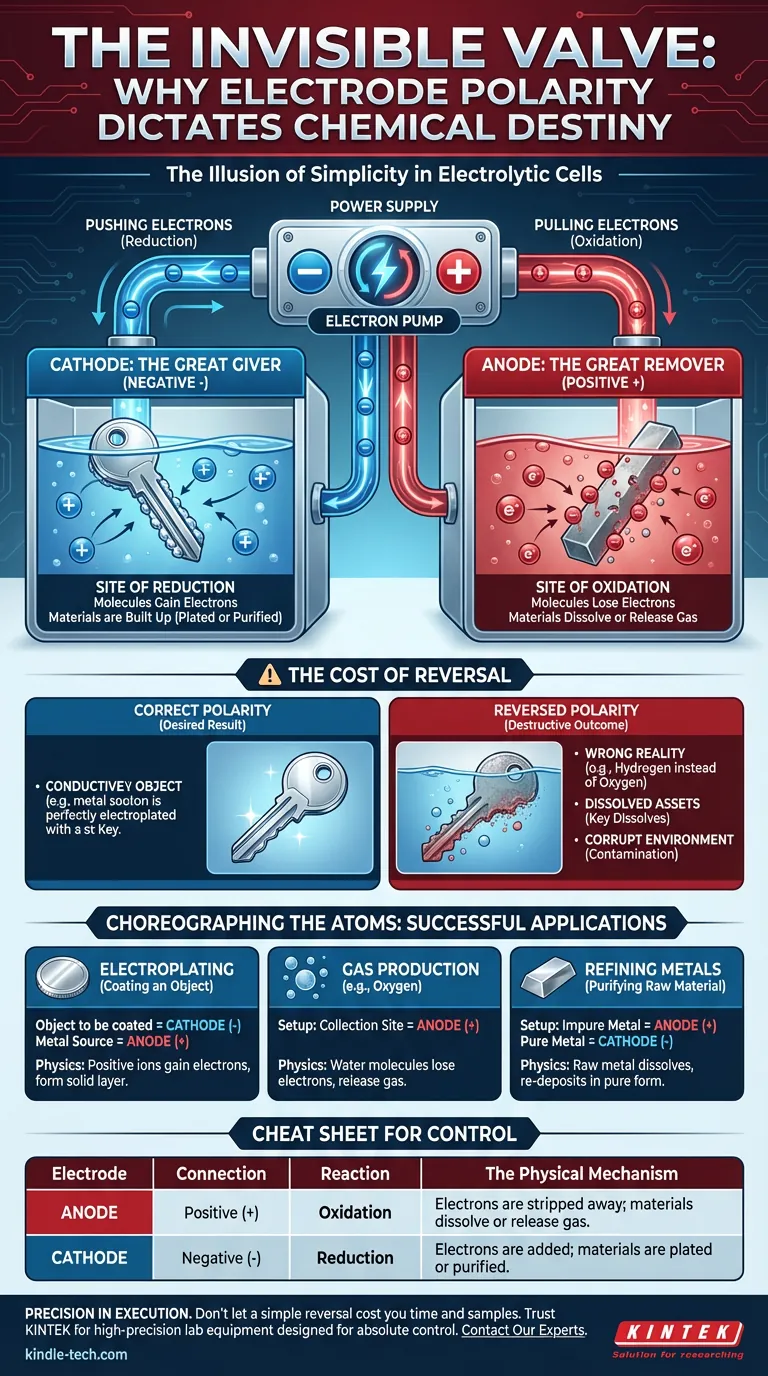
Die Anode: Der große Entferner
An den positiven (+) Pol angeschlossen, ist die Anode der Ort, an dem das Netzteil Elektronen von chemischen Spezies abreißt.
Dies ist der Ort der Oxidation. Moleküle in der Nähe dieser Oberfläche verlieren Elektronen. Sie werden abgebaut.
Die Kathode: Der große Geber
An den negativen (-) Pol angeschlossen, ist die Kathode der Ort, an dem das Netzteil einen Elektronenüberschuss auf die Oberfläche drückt.
Dies ist der Ort der Reduktion. Moleküle in der Nähe dieser Oberfläche gewinnen Elektronen. Sie werden aufgebaut.
Die Kosten der Umkehrung
Was passiert, wenn Sie die Drähte vertauschen?
In vielen Lebensbereichen bedeutet ein vertauschter Anschluss lediglich, dass das Gerät nicht eingeschaltet wird. In der Elektrolyse sind die Folgen weitaus aktiver – und oft zerstörerisch.
Wenn Sie die Polarität umkehren, pausieren Sie die Reaktion nicht. Sie invertieren das Universum Ihres Becherglases.
1. Sie produzieren die falsche Realität
Wenn Sie beabsichtigt hatten, Sauerstoff zu erzeugen, aber die Anschlüsse vertauscht haben, könnten Sie stattdessen Wasserstoff erzeugen. Die chemische Logik ist perfekt invertiert. Sie erhalten kein „Ergebnis“, sondern das „Anti-Ergebnis“.
2. Sie lösen Ihre Vermögenswerte auf
Stellen Sie sich vor, Sie beschichten einen antiken Schlüssel mit Kupfer. Sie möchten, dass die Kupferionen auf dem Schlüssel abgeschieden werden.
Wenn Sie die Polarität umkehren, wird der Schlüssel zur Anode (Ort der Oxidation). Anstatt eine glänzende Kupferschicht zu erhalten, beginnt der Schlüssel selbst, sich in der Lösung aufzulösen. Sie bewahren das Objekt nicht auf; Sie zerstören es aktiv.
3. Sie verderben die Umwelt
Das Erzwingen einer Oxidation an einer dafür nicht vorgesehenen Elektrode führt zu schneller Korrosion. Dies ruiniert nicht nur die Elektrode; es überschwemmt Ihren sorgfältig vorbereiteten Elektrolyten mit Verunreinigungen und macht das gesamte Experiment ungültig.
Choreografie der Atome
Erfolgreiche Elektrolyse erfordert, dass Sie ein Architekt der atomaren Bewegung sind. Sie müssen entscheiden, wohin die Elektronen fließen, bevor Sie den Schalter umlegen.
Verwenden Sie diese Logik, um Ihre Polarität zuzuweisen:
-
Das Ziel: Galvanisieren
- Der Aufbau: Das zu beschichtende Objekt muss die Kathode (-) sein.
- Die Physik: Sie benötigen positive Metallionen, die Elektronen aufnehmen und sich auf der Oberfläche des Objekts in festes Metall umwandeln.
-
Das Ziel: Gasproduktion (z. B. Sauerstoff)
- Der Aufbau: Der Sammelort muss die Anode (+) sein.
- Die Physik: Wassermoleküle müssen Elektronen verlieren (oxidieren), um Sauerstoffgas freizusetzen.
-
Das Ziel: Raffinieren von Metallen
- Der Aufbau: Das unreine Metall muss die Anode (+) sein.
- Die Physik: Das Rohmetall muss sich in der Lösung auflösen (oxidieren), damit es an anderer Stelle in reiner Form wieder abgeschieden werden kann.
Die Zusammenfassung der Kontrolle
Hier ist der Spickzettel zur Kontrolle Ihres chemischen Schicksals:
| Elektrode | Anschluss | Reaktion | Der physikalische Mechanismus |
|---|---|---|---|
| Anode | Positiv (+) | Oxidation | Elektronen werden abgerissen; Materialien lösen sich auf oder geben Gas ab. |
| Kathode | Negativ (-) | Reduktion | Elektronen werden hinzugefügt; Materialien werden beschichtet oder gereinigt. |
Präzision in der Ausführung
Es gibt eine gewisse Romantik in der Elektrolyse. Sie greifen in die molekulare Welt ein und zwingen Atome, in die von Ihnen gewählte Richtung zu marschieren.
Aber diese Kontrolle hängt von der Integrität Ihres Aufbaus ab. Selbst das beste theoretische Verständnis scheitert, wenn die Ausrüstung unzuverlässig ist oder die Anschlüsse schlecht sind.
Bei KINTEK verstehen wir, dass die Grenze zwischen einem Durchbruch und einem fehlgeschlagenen Experiment oft so dünn ist wie eine Drahtverbindung. Wir sind spezialisiert auf hochpräzise Laborgeräte und Verbrauchsmaterialien, die Ihnen absolute Kontrolle über Ihre elektrochemischen Prozesse geben.
Ob Sie Edelmetalle raffinieren oder empfindliche Forschung betreiben, unsere Werkzeuge stellen sicher, dass die Elektronen, wenn Sie sie zum Fließen befehlen, genau dorthin fließen, wo sie hingehören.
Lassen Sie nicht zu, dass eine einfache Umkehrung Sie Zeit und Proben kostet. Kontaktieren Sie unsere Experten
Visuelle Anleitung
Ähnliche Produkte
- PTFE Elektrolysezelle Elektrochemische Zelle Korrosionsbeständig Abgedichtet und Nicht Abgedichtet
- Super abgedichtete elektrochemische Elektrolysezelle
- Elektrochemische Elektrolysezelle mit fünf Anschlüssen
- H-Typ Elektrolysezelle Dreifache elektrochemische Zelle
- Elektrochemische Elektrolysezelle mit Gasdiffusion und Flüssigkeitsströmungsreaktionszelle
Ähnliche Artikel
- Die Architektur der Sicherheit: Beherrschen Sie die Kontrolle in multifunktionalen Elektrolysezellen
- Der stille Partner: Warum die Materialwahl in der Elektrochemie Vertrauenssache ist
- Elektrolytbatterien sind eine Lösung für den wachsenden Energiebedarf
- Die Kunst des Widerstands: Warum Ihre Elektrolysezelle Platz zum Atmen braucht
- Die Architektur der Unsichtbarkeit: Dekonstruktion der "Ganz-Quarz"-Zelle




















