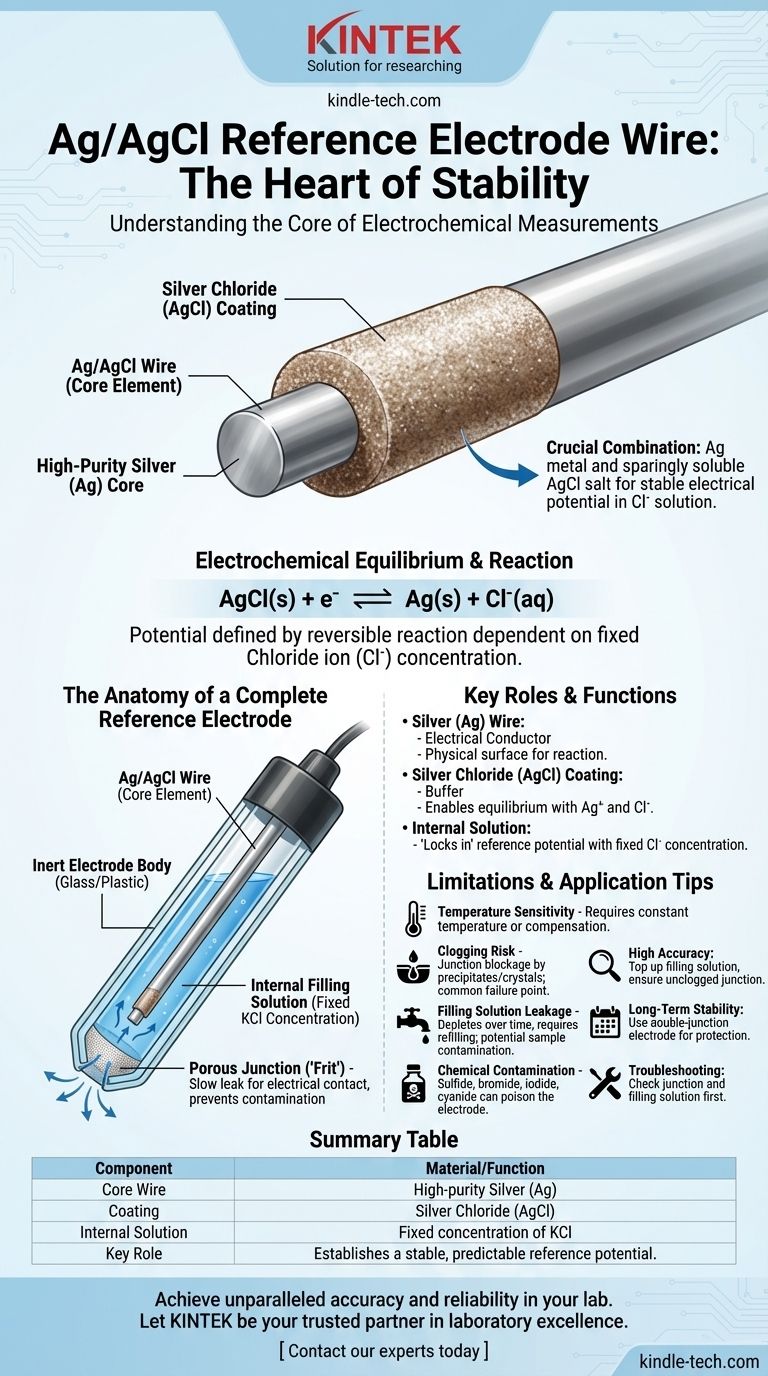
Der Draht im Kern einer Silber/Silberchlorid (Ag/AgCl)-Referenzelektrode ist ein hochreiner Silber (Ag)-Draht, der mit einer Schicht aus Silberchlorid (AgCl) beschichtet wurde. Diese spezifische Kombination aus einem Metall und seinem schwerlöslichen Salz ermöglicht es der Elektrode, ein stabiles, vorhersagbares elektrisches Potenzial aufrechtzuerhalten, wenn sie in eine chloridhaltige Lösung eingetaucht wird.
Die Stabilität einer Ag/AgCl-Elektrode kommt nicht allein vom Silberdraht. Sie entsteht durch das elektrochemische Gleichgewicht, das sich zwischen dem metallischen Silber, seiner Silberchloridbeschichtung und der konstanten Konzentration von Chloridionen in der die Elektrode füllenden Lösung einstellt.

Wie der Ag/AgCl-Draht eine stabile Referenz erzeugt
Um zu verstehen, warum dieser spezifische Draht verwendet wird, müssen wir ihn als einen Teil eines präzisen elektrochemischen Systems betrachten. Das Potenzial der Elektrode ist nicht willkürlich; es wird durch eine spezifische, reversible chemische Reaktion bestimmt.
Die Rolle des Silber (Ag)-Drahtes
Der reine Silberdraht dient als feste, metallische Phase in der Elektrode. Er ist ein ausgezeichneter elektrischer Leiter, der die physikalische Oberfläche bereitstellt, auf der die entscheidende elektrochemische Reaktion stattfindet.
Die kritische Silberchlorid (AgCl)-Beschichtung
Die Silberchloridschicht ist die kritischste Komponente. AgCl ist ein Salz, das in Wasser nur schwer löslich ist. Diese Beschichtung wirkt als Puffer und stellt sicher, dass der Silberdraht immer im Gleichgewicht mit einer Quelle von sowohl Silberionen (Ag⁺) als auch Chloridionen (Cl⁻) steht.
Die definierende elektrochemische Reaktion
Das stabile Potenzial der Elektrode wird durch die folgende reversible Reaktion definiert:
AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq)
Das Potenzial dieser Reaktion hängt direkt von der Konzentration der Chloridionen (Cl⁻) in der Lösung ab. Da die Elektrode mit einer Lösung von bekannter und fester Chloridkonzentration gefüllt ist, bleibt ihr Potenzial stabil und vorhersagbar.
Anatomie einer vollständigen Referenzelektrode
Der Ag/AgCl-Draht funktioniert nicht isoliert. Er ist in einem sorgfältig konstruierten Gehäuse untergebracht, das sicherstellt, dass sein Potenzial unabhängig von der Probenlösung, die er misst, konstant bleibt.
Die interne Fülllösung
Der Elektrodenkörper ist mit einer Elektrolytlösung gefüllt, die eine feste Konzentration von Chloridionen enthält, meist Kaliumchlorid (KCl). Diese Lösung stellt sicher, dass die Chloridionenkonzentration in der obigen Reaktion konstant bleibt, was das Referenzpotenzial der Elektrode "fixiert".
Der poröse Übergang (oder 'Fritte')
Ein poröser Stopfen, oft aus Keramik oder Teflon, befindet sich an der Spitze der Elektrode. Seine Aufgabe ist es, den elektrischen Kontakt (Ionenfluss) zwischen der internen Fülllösung und der externen Probenlösung zu ermöglichen. Er ist so konzipiert, dass er sehr langsam leckt, um eine Kontamination des Referenzelements zu verhindern.
Der Elektrodenkörper
Der Körper selbst besteht typischerweise aus inertem Glas- oder Kunststoffrohr. Er dient dazu, den Ag/AgCl-Draht und die interne Fülllösung aufzunehmen und sie vor der äußeren Umgebung zu schützen.
Verständnis der Kompromisse und Einschränkungen
Obwohl robust, sind Ag/AgCl-Elektroden nicht ohne ihre betrieblichen Einschränkungen. Das Verständnis dieser ist der Schlüssel zu genauen Messungen.
Temperaturempfindlichkeit
Das Potenzial einer Ag/AgCl-Elektrode ist temperaturabhängig. Für hochpräzise Arbeiten müssen Messungen bei einer konstanten, bekannten Temperatur durchgeführt oder die Temperaturschwankung berücksichtigt werden.
Verstopfungsgefahr
Der poröse Übergang ist der häufigste Fehlerpunkt. Wenn er durch Ausfällungen aus der Probenlösung oder durch getrocknete KCl-Kristalle verstopft wird, wird der elektrische Kreislauf unterbrochen, und die Elektrode funktioniert nicht mehr korrekt.
Leckage der Fülllösung
Der Übergang muss langsam lecken, um den ionischen Kontakt aufrechtzuerhalten. Das bedeutet, dass die Fülllösung mit der Zeit verbraucht wird und nachgefüllt werden muss. Diese Leckage kann auch geringe Mengen an Chlorid- und Kaliumionen in Ihre Probe einbringen, was bei bestimmten empfindlichen Analysen ein Problem darstellen kann.
Chemische Kontamination
Das Referenzpotenzial kann instabil werden, wenn die Elektrode Substanzen ausgesetzt wird, die mit Silber reagieren. Sulfid-, Bromid-, Iodid- und Cyanidionen sind besonders problematisch und können die Elektrodenoberfläche "vergiften".
Wie Sie dies auf Ihr Experiment anwenden können
Bei der Arbeit mit Ag/AgCl-Elektroden bestimmt Ihr primäres Ziel, wie Sie sie verwenden und warten sollten.
- Wenn Ihr Hauptaugenmerk auf hochgenauen Messungen liegt: Überprüfen Sie immer, ob die Fülllösung aufgefüllt und frei von Luftblasen oder Kristallen ist, und stellen Sie sicher, dass der poröse Übergang vor jedem Gebrauch frei ist.
- Wenn Ihr Hauptaugenmerk auf Langzeitstabilität liegt (z. B. in einer Überwachungseinrichtung): Verwenden Sie eine Doppelkammerelektrode, um das innere Ag/AgCl-Element vor potenziellen Verunreinigungen in Ihrer Probenlösung zu schützen.
- Wenn Ihr Hauptaugenmerk auf der Fehlerbehebung einer fehlerhaften Messung liegt: Vermuten Sie zuerst einen verstopften Übergang oder eine erschöpfte Fülllösung, da dies die häufigsten und am einfachsten zu behebenden Fehlerursachen für eine Referenzelektrode sind.
Das Verständnis, dass der Ag/AgCl-Draht das Herzstück eines vollständigen elektrochemischen Systems ist, ist der Schlüssel zu zuverlässigen und wiederholbaren Messungen.
Zusammenfassungstabelle:
| Komponente | Material/Funktion |
|---|---|
| Kerndraht | Hochreines Silber (Ag) |
| Beschichtung | Silberchlorid (AgCl) |
| Interne Lösung | Feste Konzentration von KCl |
| Schlüsselrolle | Stellt ein stabiles, vorhersagbares Referenzpotenzial her |
Erzielen Sie unübertroffene Genauigkeit und Zuverlässigkeit in Ihrem Labor.
Die Silber/Silberchlorid (Ag/AgCl)-Referenzelektrode ist grundlegend für präzise elektrochemische Messungen. Bei KINTEK verstehen wir, dass Ihre Forschung das höchste Maß an Konsistenz und Leistung von Ihrer Laborausrüstung verlangt.
Wir bieten hochwertige Referenzelektroden und Verbrauchsmaterialien, die auf Langlebigkeit und Genauigkeit ausgelegt sind, um sicherzustellen, dass Ihre Experimente niemals beeinträchtigt werden. Ob Sie empfindliche pH-Analysen, potentiometrische Titrationen oder Langzeitüberwachung durchführen, die richtige Ausrüstung ist entscheidend.
Lassen Sie KINTEK Ihr vertrauenswürdiger Partner für Labor-Exzellenz sein. Kontaktieren Sie noch heute unsere Experten, um die perfekten elektrochemischen Lösungen für Ihre spezifische Anwendung zu finden und sicherzustellen, dass Ihre Messungen immer präzise sind.
Visuelle Anleitung
Ähnliche Produkte
- Referenzelektrode Kalomel Silberchlorid Quecksilbersulfat für Laborzwecke
- Kupfersulfat-Referenzelektrode für Laboranwendungen
- Graphit-Scheiben-Stab- und Plattenelektrode Elektrochemische Graphitelektrode
- Elektrochemische Elektrode aus Glaskohlenstoff
- Gold-Elektrodenblech Gold-Elektrode
Andere fragen auch
- Welche Art von Elektrode kann als Referenzpunkt verwendet werden? Wählen Sie die richtige für genaue Messungen
- Welche Elektrode wird als Referenzelektrode zur Messung von Halbzellenpotentialen verwendet? Das universelle Standardverständnis
- Was ist die Referenzelektrode in der Potentiometrie? Der Schlüssel zu stabilen & genauen Messungen
- Was ist die Funktion einer Referenzelektrode? Präzision meistern bei der Rekonstruktion von Drei-Elektroden-Reaktoren
- Was ist der Zweck der Referenzelektrode? Erreichen Sie stabile und genaue elektrochemische Messungen








