Das häufigste Edelgas in der Erdatmosphäre ist Argon (Ar). Es macht etwa 0,93 % der Luft aus, die wir atmen, und ist damit nach Stickstoff und Sauerstoff das dritthäufigste Gas insgesamt.
Während Argon die definitive Antwort ist, liegt das tiefere Verständnis in der Unterscheidung zwischen der chemischen Definition eines „Edelgases“ und der praktischen Anwendung eines „inerten Gases“ in Wissenschaft und Industrie.
Was macht ein Gas „inert“?
Der Begriff „inert“ bezieht sich auf eine chemisch inaktive Substanz. Im Zusammenhang mit Gasen wird diese Eigenschaft am bekanntesten mit einer bestimmten Gruppe von Elementen im Periodensystem in Verbindung gebracht.
Die Edelgasfamilie
Die inerten Gase werden auch als Edelgase bezeichnet. Diese Gruppe umfasst Helium, Neon, Argon, Krypton, Xenon und Radon.
Ihr bestimmendes Merkmal ist eine volle Außenschale von Elektronen. Diese stabile Konfiguration macht sie extrem widerwillig, Elektronen zu teilen, aufzunehmen oder abzugeben.
Extreme chemische Stabilität
Da sie nicht leicht chemische Bindungen mit anderen Elementen eingehen, sind Edelgase hochgradig nicht-reaktiv. Sie existieren als einzelne Atome, nicht als Moleküle wie Sauerstoff (O₂) oder Stickstoff (N₂).
Warum diese Eigenschaft wichtig ist
Diese Nicht-Reaktivität ist unglaublich nützlich. Inertgase werden verwendet, um eine stabile Umgebung für Prozesse wie das Schweißen zu schaffen, um zu verhindern, dass Glühfäden in Glühlampen durchbrennen, und um empfindliche Materialien zu konservieren.
Ein genauerer Blick auf die Erdatmosphäre
Um Argons Platz zu verstehen, ist es entscheidend, das Gesamtbild der Zusammensetzung unserer Atmosphäre zu sehen.
Die zwei dominanten Gase
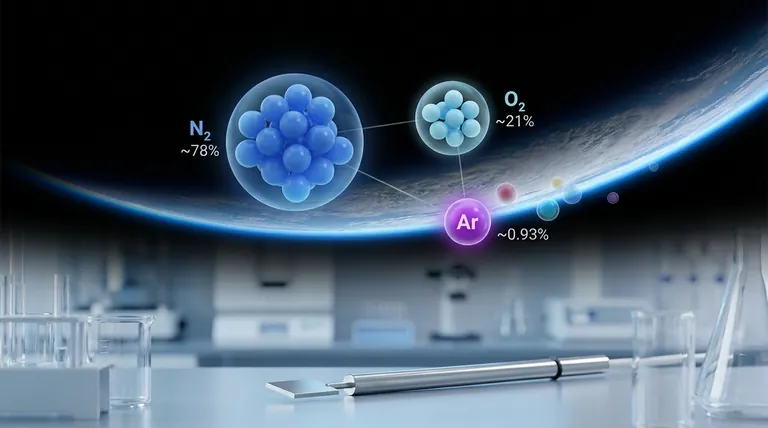
Die Luft besteht überwiegend aus zwei Gasen: Stickstoff (N₂) mit etwa 78 % und Sauerstoff (O₂) mit etwa 21 %. Diese beiden Elemente machen 99 % der Luft aus.
Argons Position
Das restliche 1 % ist der Bereich, in dem wir Argon finden. Mit etwa 0,93 % ist es bei weitem das bedeutendste vorhandene Edelgas.
Spuren anderer Edelgase
Die anderen Edelgase existieren in weitaus geringeren Mengen. Zum Vergleich: Neon ist zu etwa 0,0018 % vorhanden, während Helium, Krypton und Xenon in noch geringeren Spurenmengen gefunden werden.
Die Nuancen verstehen
Die Begriffe „inert“ und „Edelgas“ werden oft synonym verwendet, aber es gibt wichtige Unterschiede zu verstehen.
Ist „inert“ wirklich inert?
Obwohl Edelgase sehr stabil sind, sind sie nicht unter allen Bedingungen vollständig inert. Wissenschaftler haben Edelgase wie Xenon und Krypton dazu gebracht, chemische Verbindungen in einer Laborumgebung unter extremem Druck und extremen Temperaturen zu bilden.
Stickstoff: Das „fast“ inerte Gas
Stickstoffgas (N₂) ist kein Edelgas. Die starke Dreifachbindung, die seine beiden Atome zusammenhält, macht es jedoch unter vielen Bedingungen sehr stabil und nicht-reaktiv.
Da es weitaus häufiger und billiger als Argon ist, wird Stickstoff häufig als „inertes“ Gas für industrielle Anwendungen wie Lebensmittelverpackungen und Elektronikfertigung verwendet, wo extreme Nicht-Reaktivität nicht erforderlich ist.
Alles ins rechte Licht rücken
Die Wahl oder Identifizierung eines inerten Gases hängt vollständig vom Kontext Ihrer Frage ab – konzentrieren Sie sich auf die chemische Reinheit oder die praktische Anwendung?
- Wenn Ihr Hauptaugenmerk auf der Chemie liegt: Argon ist das häufigste Edelgas, definiert durch seine Atomstruktur und volle Elektronenschale.
- Wenn Ihr Hauptaugenmerk auf der atmosphärischen Zusammensetzung liegt: Argon ist das dritthäufigste Gas in der Luft, aber es liegt weit hinter Stickstoff und Sauerstoff.
- Wenn Ihr Hauptaugenmerk auf der industriellen Nutzung liegt: Die Wahl zwischen Argon und Stickstoff hängt oft vom erforderlichen Grad der Nicht-Reaktivität im Verhältnis zu den Kosten ab, wobei Stickstoff ein häufiger Ersatz ist.
Das Verständnis der Unterscheidung zwischen der elementaren Natur eines Gases und seinem praktischen Verhalten ist der Schlüssel zur Beherrschung des Themas.
Zusammenfassungstabelle:
| Gas | Typ | Häufigkeit in der Atmosphäre | Hauptmerkmal |
|---|---|---|---|
| Argon (Ar) | Edelgas (inert) | ~0,93% | Häufigstes Edelgas; volle Elektronenschale |
| Stickstoff (N₂) | Diatomares Gas | ~78% | Wird oft als praktisches, kostengünstiges inertes Gas verwendet |
| Helium (He) | Edelgas (inert) | Spuren | Sehr geringe Häufigkeit, aber hoch inert |
| Neon (Ne) | Edelgas (inert) | ~0,0018% | Geringe Häufigkeit; in Beleuchtung verwendet |
Benötigen Sie eine zuverlässige Inertgasversorgung für Ihr Labor?
Das Verständnis der Eigenschaften von Gasen wie Argon ist entscheidend für präzise Laborarbeiten. Ob Sie hochreine Inertgase für empfindliche Experimente oder zuverlässige Gasversorgungssysteme benötigen, KINTEK verfügt über das Fachwissen und die Ausrüstung, um Ihre Forschung zu unterstützen. Wir sind spezialisiert auf die Bereitstellung hochwertiger Laborgeräte und Verbrauchsmaterialien, um sicherzustellen, dass Ihre Prozesse effizient und kontaminationsfrei sind.
Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie wir Ihre spezifischen Anforderungen an Laborgase erfüllen können!
Visuelle Anleitung
