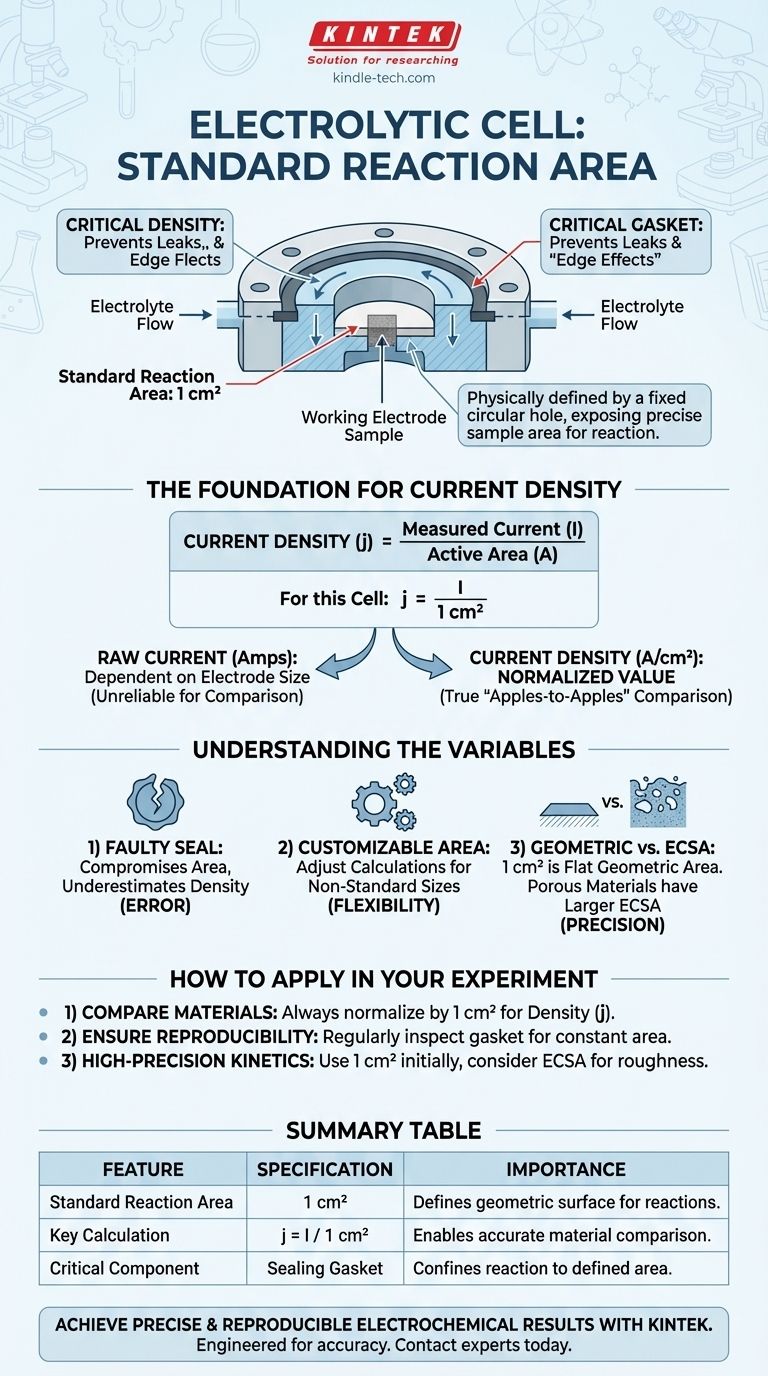
Basierend auf den bereitgestellten Spezifikationen beträgt die Standard-Reaktionsfläche der Arbeitselektrode in dieser Elektrolysezelle 1 Quadratzentimeter (1 cm²). Diese Fläche wird physisch durch ein festes kreisförmiges Loch am Boden der Zelle definiert, durch das die Arbeitselektrodenprobe dem Elektrolyten ausgesetzt wird.
Die Frage nach der Elektrodenfläche weist auf ein grundlegenderes Bedürfnis hin: die Sicherstellung, dass experimentelle Ergebnisse genau und vergleichbar sind. Die feste Fläche von 1 cm² ist nicht nur eine Dimension; sie ist die Grundlage für die Berechnung der Stromdichte, der universellen Metrik zur Bewertung der elektrochemischen Leistung.

Die Rolle der festen Reaktionsfläche
Das physikalische Design der Zelle ist bewusst so konstruiert, dass die Variablen Ihres Experiments kontrolliert werden. Die definierte Öffnung für die Arbeitselektrode ist wohl das kritischste Merkmal.
Definition der aktiven Oberfläche
Das 1 cm² große Loch fungiert als Maske, die nur eine präzise und bekannte Fläche Ihres Probenmaterials (der Arbeitselektrode) dem Elektrolyten aussetzt. Alle elektrochemischen Reaktionen sind auf diese spezifische Oberfläche beschränkt.
Dieses Design stellt sicher, dass die geometrische Oberfläche, die an der Reaktion beteiligt ist, von einem Experiment zum nächsten konstant ist, was für die Reproduzierbarkeit unerlässlich ist.
Die kritische Funktion der Dichtung
Eine Dichtung wird verwendet, um eine dichte Abdichtung um den Umfang dieses 1 cm² großen Lochs herum zu schaffen. Ihr Zweck ist zweifach: das Austreten des Elektrolyten zu verhindern und die Ausbreitung der Reaktion über den definierten Bereich hinaus zu stoppen.
Ohne eine ordnungsgemäße Abdichtung können "Spaltkorrosion" oder "Randeffekte" auftreten, die zu einer undefinierten Reaktionsfläche führen und Ihre Messungen ungenau machen.
Von der Fläche zur Stromdichte: Die wahre Metrik
Die Kenntnis der Reaktionsfläche ist der erste Schritt. Das ultimative Ziel ist es, sie zu verwenden, um einen weitaus aufschlussreicheren Wert zu berechnen: die Stromdichte.
Was ist Stromdichte?
Die Stromdichte ist der gesamte in einem Experiment gemessene elektrische Strom, geteilt durch die aktive Fläche der Elektrode. Sie wird typischerweise in Ampere pro Quadratzentimeter (A/cm²) oder Milliampere pro Quadratzentimeter (mA/cm²) ausgedrückt.
Für diese Zelle ist die Berechnung einfach: Stromdichte (j) = Gemessener Strom (I) / 1 cm².
Warum sie wichtiger ist als der Rohstrom
Das bloße Messen des Gesamtstroms (in Ampere) ist für den Vergleich unzureichend, da dieser Wert bei einer größeren Elektrode natürlich größer sein wird. Er spiegelt nicht die intrinsische Effizienz oder Aktivität des Elektrodenmaterials selbst wider.
Durch die Normierung des Stroms auf die Fläche erhalten Sie einen Wert – die Stromdichte –, der einen echten direkten Vergleich zwischen verschiedenen Materialien, Katalysatoren oder experimentellen Bedingungen ermöglicht, unabhängig von geringfügigen Abweichungen in der Probengröße.
Abwägungen und Überlegungen verstehen
Obwohl das Design einen Standard bietet, müssen mehrere Faktoren berücksichtigt werden, um die Integrität Ihrer Ergebnisse zu gewährleisten.
Die Auswirkungen einer fehlerhaften Dichtung
Eine verschlissene, unsachgemäß sitzende oder chemisch degradierte Dichtung ist eine Hauptursache für experimentelle Fehler. Wenn die Dichtung beeinträchtigt ist, kann die tatsächliche Reaktionsfläche größer sein als die angenommene 1 cm², was dazu führt, dass Sie die wahre Stromdichte unterschätzen.
Die Option für eine "anpassbare" Fläche
Der Hinweis besagt, dass die Lochgröße angepasst werden kann. Während 1 cm² ein praktischer Standard ist, kann für bestimmte Anwendungen eine andere Fläche erforderlich sein.
Zum Beispiel könnte eine kleinere Fläche für sehr teure oder knappe Materialien verwendet werden, während eine größere Fläche für Materialien mit sehr geringer Leitfähigkeit erforderlich sein könnte. Wenn Sie eine benutzerdefinierte Fläche verwenden, müssen alle Stromdichteberechnungen entsprechend angepasst werden.
Geometrische vs. elektrochemische Oberfläche (ECSA)
Es ist entscheidend, zwischen der geometrischen Fläche (dem 1 cm² großen flachen Kreis) und der elektrochemischen Oberfläche (ECSA) zu unterscheiden. Wenn Ihr Elektrodenmaterial porös, rau oder nanostrukturiert ist, ist seine wahre Oberfläche auf mikroskopischer Ebene viel größer als 1 cm².
Für die meisten routinemäßigen Vergleiche reicht die Normierung nach der geometrischen Fläche aus. Für fortgeschrittene kinetische Studien verwenden Forscher jedoch häufig Techniken wie Kapazitätsmessungen, um die ECSA für ein präziseres Verständnis der katalytischen Aktivität abzuschätzen.
So wenden Sie dies auf Ihr Experiment an
Verwenden Sie die Standardfläche als Ihre Basislinie für die Erzeugung zuverlässiger und aussagekräftiger Daten.
- Wenn Ihr Hauptaugenmerk auf dem Vergleich verschiedener Materialien liegt: Normieren Sie Ihren gemessenen Strom immer auf die 1 cm² Fläche, um die Stromdichte (j) zu berechnen und anzugeben.
- Wenn Ihr Hauptaugenmerk auf der Sicherstellung der Reproduzierbarkeit liegt: Überprüfen Sie die Dichtung regelmäßig auf Verschleiß und stellen Sie sicher, dass sie vor jedem Experiment korrekt sitzt, um eine konstante Reaktionsfläche von 1 cm² zu gewährleisten.
- Wenn Ihr Hauptaugenmerk auf hochpräziser Kinetik liegt: Verwenden Sie die geometrische Fläche von 1 cm² für erste Berechnungen, ziehen Sie jedoch die Messung der wahren elektrochemischen Oberfläche (ECSA) in Betracht, wenn Ihr Material einen hohen Grad an Oberflächenrauheit aufweist.
Letztendlich ist die Verwendung der definierten Reaktionsfläche zur Berechnung der Stromdichte der Schlüssel zur Erzeugung wiederholbarer und vergleichbarer elektrochemischer Daten.
Zusammenfassungstabelle:
| Merkmal | Spezifikation | Bedeutung |
|---|---|---|
| Standard-Reaktionsfläche | 1 cm² | Definiert die geometrische Oberfläche für alle Reaktionen. |
| Schlüsselberechnung | Stromdichte (j) = Gemessener Strom (I) / 1 cm² | Ermöglicht den genauen Vergleich verschiedener Materialien. |
| Kritische Komponente | Dichtung | Verhindert Leckagen und stellt sicher, dass die Reaktion auf die 1 cm² Fläche beschränkt ist. |
Erzielen Sie präzise und reproduzierbare elektrochemische Ergebnisse mit KINTEK.
Unsere Elektrolysezellen sind mit einer präzise definierten Reaktionsfläche von 1 cm² konstruiert, um Variablen zu eliminieren und die Grundlage für genaue Stromdichteberechnungen zu schaffen. Dies gewährleistet, dass Ihre Daten zur Katalysatorleistung, Materialeffizienz und Reaktionskinetik zuverlässig und vergleichbar sind.
KINTEK ist spezialisiert auf hochwertige Laborgeräte und Verbrauchsmaterialien für alle Ihre Laborbedürfnisse. Lassen Sie sich von unserem Fachwissen bei Ihrer Forschung unterstützen.
Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie unsere Geräte Ihren elektrochemischen Arbeitsablauf verbessern können.
Visuelle Anleitung
Ähnliche Produkte
- Elektrochemische Elektrolysezelle mit Gasdiffusion und Flüssigkeitsströmungsreaktionszelle
- H-Typ Elektrolysezelle Dreifache elektrochemische Zelle
- Elektrochemische Elektrolysezelle mit fünf Anschlüssen
- Flache Korrosions-Elektrolysezelle
- Elektrochemische Quarz-Elektrolysezelle für elektrochemische Experimente
Andere fragen auch
- Was sind die drei wesentlichen Bestandteile einer elektrolytischen Zelle? Schlüsselelemente der chemischen Synthese
- Wie beeinflusst das Design einer Elektrolysezelle die Produktionsausbeute von Ferrat(VI)? Effizienz & Reinheit optimieren
- Warum sind Elektrolysezellen für die Titanproduktion unerlässlich? Energie für Kreislaufeffizienz und Kosteneinsparungen
- Wie können Kurzschlüsse in der Elektrolysezellen-Anordnung verhindert werden? Wesentliche Tipps für Sicherheit & Leistung
- Wie beeinflusst das Design einer elektrochemischen Elektrolysezelle die Beschichtungsuniformität? Optimieren Sie Ihre Katalysatoren



















