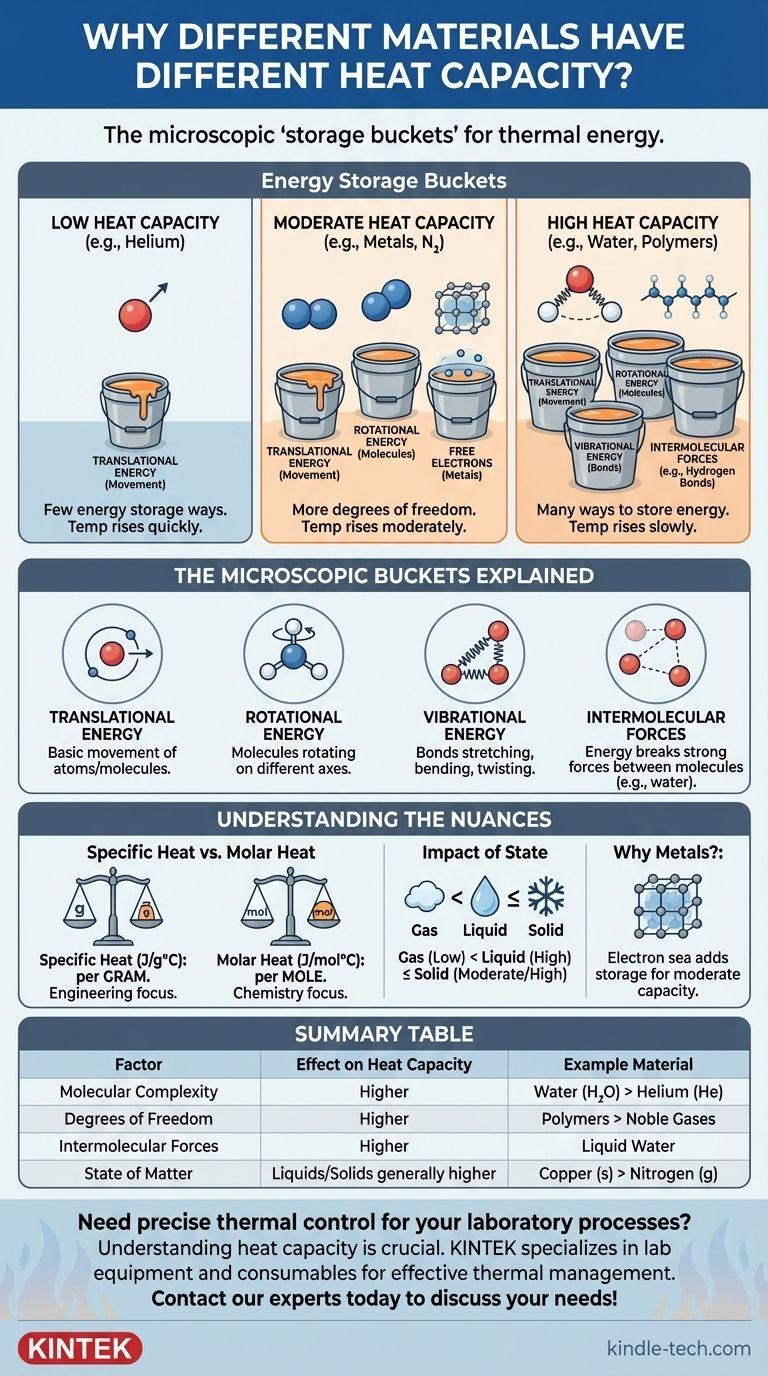
Im Kern wird die Wärmekapazität eines Materials durch die Anzahl der Möglichkeiten bestimmt, wie es Wärmeenergie auf mikroskopischer Ebene speichern kann. Wenn Sie Wärme hinzufügen, lässt diese Energie die Atome nicht nur schneller bewegen; sie wird in verschiedene „Speicherbehälter“ verteilt, wie molekulare Rotationen und Vibrationen. Materialien mit komplexeren Strukturen haben mehr dieser Speicherbehälter, sodass sie mehr Energie benötigen, um den gleichen Temperaturanstieg zu erreichen.
Die zentrale Erkenntnis ist diese: Wärmekapazität ist ein Maß für molekulare Komplexität und Freiheit. Materialien mit einfachen Atomen (wie Edelgase) haben eine geringe Wärmekapazität, während Materialien mit komplexen Molekülen und starken intermolekularen Kräften (wie Wasser) eine hohe Wärmekapazität haben, weil sie viel mehr Möglichkeiten haben, Energie über die einfache Bewegung hinaus aufzunehmen.

Was ist Wärmekapazität wirklich?
Um die Unterschiede zwischen Materialien zu verstehen, müssen wir zunächst die Konzepte von Wärme und Temperatur trennen.
Temperatur vs. Wärme
Temperatur ist ein Maß für die durchschnittliche kinetische Energie der Teilchen in einer Substanz. Stellen Sie es sich als die durchschnittliche Geschwindigkeit der Atome oder Moleküle vor, während sie sich bewegen, wackeln und zittern.
Wärme hingegen ist die gesamte thermische Energie, die in oder aus einer Substanz übertragen wird. Wenn Sie Wärme hinzufügen, fügen Sie Energie hinzu. Die Aufgabe dieser Energie ist es, die gesamte innere Energie der Substanz zu erhöhen.
Die Analogie der „Energiespeicherung“
Stellen Sie sich vor, Sie haben mehrere leere Eimer. Wärme hinzuzufügen ist wie Wasser hineinzuschütten. Die Temperatur ist wie der Wasser-Pegel in nur einem dieser Eimer, dem mit der Aufschrift „Bewegung“ (kinetische Energie).
Die Wärmekapazität eines Materials wird durch die Gesamtzahl der Eimer bestimmt, die es hat. Wenn ein Material nur einen Eimer („Bewegung“) hat, fließt das gesamte Wasser, das Sie hineinschütten, dorthin, und der Pegel steigt schnell. Wenn ein Material viele Eimer hat, müssen Sie viel mehr Wasser hineinschütten, um den Pegel in diesem einen spezifischen „Bewegungs“-Eimer zu erhöhen.
Die mikroskopischen Eimer: Wo Energie gespeichert wird
Verschiedene Materialien haben verschiedene Arten von mikroskopischen „Eimern“, die formal als Freiheitsgrade bezeichnet werden. Jeder bietet eine andere Möglichkeit, Wärmeenergie zu speichern.
1. Translationsenergie (Der Basiseimer)
Dies ist die Energie eines Atoms oder Moleküls, das sich von einem Ort zum anderen bewegt. Alle Materialien haben dies. Es ist der Hauptbeitrag zu dem, was wir als Temperatur messen.
Für eine einfache Substanz wie Heliumgas, dessen Atome einzelne Kugeln sind, ist dies fast die einzige Möglichkeit, Energie zu speichern. Seine Wärmekapazität ist sehr gering.
2. Rotationsenergie (Für Moleküle)
Ein einzelnes Atom kann sich nicht sinnvoll drehen, um Energie zu speichern, aber ein Molekül kann es. Ein einfaches zweiatomiges Molekül wie Stickstoff (N₂) kann sich um zwei verschiedene Achsen drehen, wie ein wirbelnder Stab.
Ein komplexeres, nicht-lineares Molekül wie Wasser (H₂O) kann sich um drei verschiedene Achsen drehen. Jede Rotationsachse ist ein weiterer „Eimer“ zur Energiespeicherung, was seine Wärmekapazität erhöht.
3. Vibrationsenergie (Ein wichtiges Unterscheidungsmerkmal)
Die Bindungen, die Atome in einem Molekül zusammenhalten, sind keine starren Stäbe; sie sind eher wie Federn. Sie können sich dehnen, biegen und verdrehen. Jede dieser Schwingungsmoden ist ein weiterer hochwirksamer Energieeimer.
Ein einfaches zweiatomiges Molekül hat eine Schwingungsmodus. Ein komplexes Molekül mit vielen Atomen und Bindungen hat Dutzende. Dies ist ein Hauptgrund, warum komplexe Substanzen wie Öle und Polymere höhere Wärmekapazitäten haben als einfache Gase.
4. Intermolekulare Kräfte (Das Wasserbeispiel)
In Flüssigkeiten und Feststoffen wird Energie auch dazu verwendet, den Kräften zwischen den Molekülen entgegenzuwirken. Wasser ist das ultimative Beispiel dafür. Seine Moleküle sind durch starke Wasserstoffbrückenbindungen miteinander verbunden.
Bevor sich die Wassermoleküle signifikant beschleunigen können (Temperaturanstieg), muss ein großer Teil der zugeführten Wärmeenergie zunächst in das Rütteln und Brechen dieser starken Bindungen fließen. Dies wirkt als massive Energiesenke und verleiht Wasser eine der höchsten spezifischen Wärmekapazitäten aller gängigen Substanzen.
Die Nuancen verstehen
Beim Vergleich von Materialien ist der Kontext entscheidend. Das bloße Betrachten einer Zahl kann irreführend sein, ohne zu verstehen, was sie darstellt.
Spezifische Wärme vs. molare Wärmekapazität
Die spezifische Wärmekapazität ist die Energie, die benötigt wird, um ein Gramm einer Substanz um ein Grad Celsius zu erhöhen (J/g°C). Dies ist nützlich für Ingenieurwesen und reale Anwendungen, wo die Masse das Hauptanliegen ist.
Die molare Wärmekapazität ist die Energie, die benötigt wird, um ein Mol einer Substanz um ein Grad zu erhöhen (J/mol°C). Dies ist oft nützlicher für Physiker und Chemiker, da es eine gleiche Anzahl von Molekülen vergleicht und einen faireren Vergleich der molekularen Komplexität ermöglicht. Zum Beispiel ist die spezifische Wärme von Wasser über viermal so hoch wie die von Kupfer, aber seine molare Wärmekapazität ist nur etwa dreimal größer.
Der Einfluss des Zustands (Gas, Flüssigkeit, Feststoff)
Die Wärmekapazität einer Substanz ändert sich je nach ihrem Zustand.
- Gase haben geringere Wärmekapazitäten, da ihre Moleküle weit voneinander entfernt sind und kaum interagieren.
- Flüssigkeiten haben höhere Kapazitäten aufgrund der Energie, die benötigt wird, um intermolekulare Kräfte zu überwinden.
- Feststoffe speichern Energie in einem kollektiven Gitter von Schwingungen (sogenannte Phononen). Ihre Kapazität ist oft ähnlich wie in ihrer flüssigen Form, kann aber bei sehr kalten Temperaturen niedriger sein.
Warum Metalle eine moderate Wärmekapazität haben
Man könnte erwarten, dass Metalle, da sie einfache Atome sind, eine geringe Wärmekapazität haben. Ihre Kapazität ist moderat aufgrund ihrer einzigartigen Struktur: ein starres Gitter von Ionen innerhalb eines „Meeres“ von frei beweglichen Elektronen. Dieses Elektronenmeer kann auch Wärmeenergie absorbieren und fungiert als zusätzlicher Energiespeicherbehälter, der einfachen atomaren Gasen fehlt.
Die richtige Wahl für Ihr Ziel treffen
Wie Sie Wärmekapazitätsdaten interpretieren, hängt ganz von Ihrem Ziel ab.
- Wenn Ihr Hauptaugenmerk auf Ingenieurwesen oder Wärmemanagement liegt: Verwenden Sie die spezifische Wärmekapazität (pro Gramm), da sie direkt darüber Auskunft gibt, wie stark sich eine gegebene Materialmasse in einem realen Design erwärmt.
- Wenn Ihr Hauptaugenmerk auf grundlegender Chemie oder Physik liegt: Vergleichen Sie die molare Wärmekapazität (pro Mol), um die Auswirkungen von Molekülstruktur, Freiheitsgraden und Bindungen auf die Energiespeicherung zu isolieren.
- Wenn Ihr Hauptaugenmerk auf Klimawissenschaft oder Biologie liegt: Erkennen Sie, dass die außergewöhnlich hohe spezifische Wärmekapazität von Wasser, angetrieben durch Wasserstoffbrückenbindungen, der wichtigste Faktor zur Stabilisierung des Erdklimas und zur Moderation der Körpertemperatur in lebenden Organismen ist.
Letztendlich ist die Wärmekapazität eines Materials die makroskopische Signatur seiner mikroskopischen Welt.
Zusammenfassungstabelle:
| Faktor | Auswirkung auf die Wärmekapazität | Beispielmaterial |
|---|---|---|
| Molekulare Komplexität | Komplexere Moleküle = höhere Kapazität | Wasser (H₂O) vs. Helium (He) |
| Freiheitsgrade | Mehr Möglichkeiten zur Energiespeicherung (Rotation, Vibration) = höhere Kapazität | Polymere vs. Edelgase |
| Intermolekulare Kräfte | Stärkere Kräfte (z.B. Wasserstoffbrücken) = höhere Kapazität | Flüssiges Wasser |
| Aggregatzustand | Flüssigkeiten/Feststoffe generell höher als Gase | Kupfer (fest) vs. Stickstoff (Gas) |
| Freie Elektronen | Elektronenmeer in Metallen fügt moderate Kapazität hinzu | Metalle wie Aluminium |
Benötigen Sie präzise thermische Kontrolle für Ihre Laborprozesse? Das Verständnis der Wärmekapazität ist entscheidend für Anwendungen wie chemische Synthese, Materialprüfung und thermische Analyse. KINTEK ist auf Laborgeräte und Verbrauchsmaterialien spezialisiert und bietet die Werkzeuge, die Sie zur effektiven Steuerung der Wärmeenergie benötigen. Ob Sie Öfen, Heizgeräte oder Temperaturüberwachungssysteme benötigen, unsere Lösungen sind auf Genauigkeit und Zuverlässigkeit ausgelegt. Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie wir Ihre spezifischen Laboranforderungen unterstützen und Ihre Forschungsergebnisse verbessern können.
Visuelle Anleitung