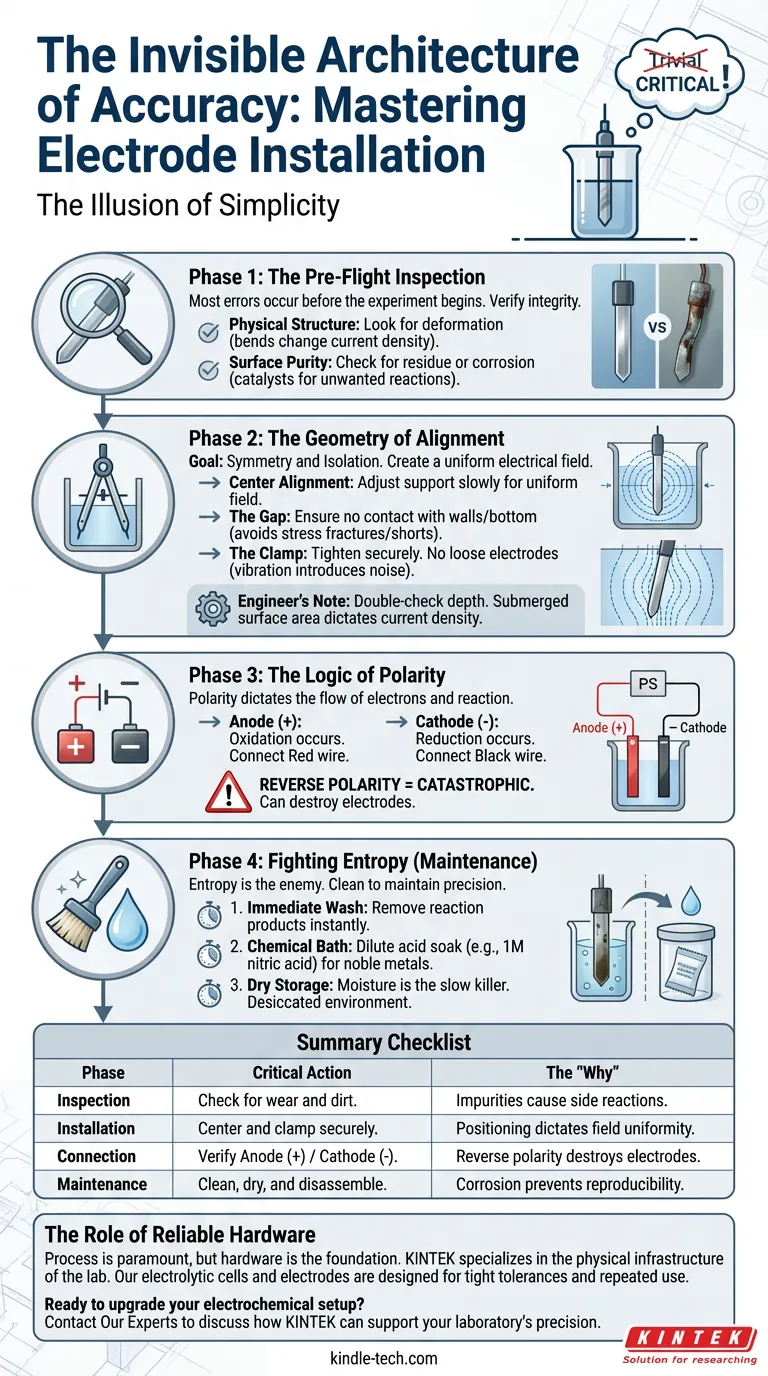
Die Illusion der Einfachheit
Im Labor sind die kritischsten Momente oft die ruhigsten.
Wir neigen dazu, uns auf die komplexe Chemie zu konzentrieren – die exotischen Reagenzien, die präzise Spannung, die theoretische Ausbeute. Aber in der Elektrochemie hängt das gesamte Experiment von einem mechanischen Vorgang ab, der weniger als fünf Minuten dauert: der Installation der Elektroden.
Es scheint trivial. Man steckt das Metall ins Glas. Man schaltet den Strom ein.
Aber diese Sichtweise ist gefährlich.
Eine Elektrolysezelle ist nicht nur ein Behälter; sie ist ein Stromkreis. Die Elektrode ist die Schnittstelle, an der die physische Welt auf die chemische Welt trifft. Wenn diese Schnittstelle fehlerhaft ist – auch nur um einen Millimeter –, sind die Daten nicht nur leicht daneben. Sie sind Fiktion.
Hier erfahren Sie, wie Sie den Installationsprozess mit der Präzision eines Ingenieurs und der Disziplin eines Chirurgen angehen.
Phase 1: Die Vorflugkontrolle
Die meisten Fehler treten auf, bevor das Experiment beginnt.
Wir gehen oft davon aus, dass eine Elektrode funktionsfähig ist, nur weil sie solide aussieht. Dies ist eine kognitive Verzerrung, bekannt als „Was man sieht, ist alles, was es gibt“. In der Elektrochemie ist jedoch die Oberflächenchemie alles.
Bevor die Elektrode die Zelle berührt, müssen Sie ihre Integrität überprüfen:
- Physische Struktur: Achten Sie auf Verformungen. Eine verbogene Elektrode verändert die Stromdichteverteilung.
- Oberflächenreinheit: Prüfen Sie auf Rückstände oder Korrosion. Ein Staubkorn ist nicht nur Staub; es ist ein Katalysator für unerwünschte Nebenreaktionen.
Wenn die Oberfläche beeinträchtigt ist, ist das Experiment bereits vor dem Start zum Scheitern verurteilt. Saubere Oberflächen sind kein Luxus; sie sind eine Voraussetzung.
Phase 2: Die Geometrie der Ausrichtung
Sobald die Inspektion abgeschlossen ist, gehen wir zur physischen Installation über.
Dies ist ein Spiel der Geometrie. Das Ziel ist Symmetrie und Isolation.
Wenn Sie die Elektroden in die Zelle absenken, versuchen Sie, ein gleichmäßiges elektrisches Feld zu erzeugen. Wenn eine Elektrode schief sitzt, verzerrt sich das Feld. Reaktionsraten verschieben sich. Reproduzierbarkeit verschwindet.
Die Regeln der Platzierung
- Zentrische Ausrichtung: Passen Sie den Stützmechanismus langsam an. Die Elektrode sollte die Achse sein, um die sich die Zelle dreht.
- Der Spalt: Stellen Sie sicher, dass die Elektrode niemals den Boden oder die Wände der Zelle berührt. Kontakt mit dem Glas kann Spannungsrisse verursachen. Kontakt mit der anderen Elektrode verursacht einen Kurzschluss.
- Die Klemme: Sobald die Position festgelegt ist, ziehen Sie die Stützklemmen fest. Verlassen Sie sich nicht auf Schwerkraft oder Reibung. Eine lose Elektrode vibriert, und Vibrationen führen Rauschen in Ihre Daten ein.
Anmerkung des Ingenieurs: Überprüfen Sie die Tiefe doppelt. Die eingetauchte Oberfläche bestimmt die Stromdichte. Wenn sich die Tiefe verschiebt, brechen Ihre Berechnungen.
Phase 3: Die Logik der Polarität
Chemie hat eine Richtung.
Das Anschließen des Netzteils ist nicht wie das Einstecken eines Toasters. Die Polarität bestimmt den Elektronenfluss und damit den Fluss der Reaktion.
- Anode (+): Hier findet die Oxidation statt.
- Kathode (-): Hier findet die Reduktion statt.
Eine Umkehrung hier ist katastrophal. Sie stoppt nicht nur das Experiment; sie zerstört oft die Elektroden, indem sie Oxidation auf ein für die Reduktion bestimmtes Material erzwingt.
Verfolgen Sie immer das Kabel von der Quelle zur Zelle. Rot zur Anode. Schwarz zur Kathode. Vertrauen Sie nicht Ihrem Gedächtnis. Vertrauen Sie dem Kabel.
Phase 4: Kampf gegen die Entropie (Wartung)
Das Experiment endet nicht, wenn der Strom abgeschaltet wird.
Entropie ist der Feind von Laborgeräten. Wenn Sie eine Elektrode feucht mit Elektrolyt zurücklassen, beginnt sofort die Korrosion. Die Salze kristallisieren. Das Metall zersetzt sich.
Um die „Romantik“ präziser Maschinen zu erhalten, müssen Sie sie reinigen.
- Sofortiges Abspülen: Entfernen Sie Reaktionsprodukte sofort.
- Chemisches Bad: Bei Edelmetallen wie Platin stellt ein Bad in verdünnter Säure (z. B. 1M Salpetersäure) die Oberfläche wieder her.
- Trockene Lagerung: Feuchtigkeit ist der langsame Killer. Lagern Sie Komponenten in einer trockenen Umgebung.
Wenn Sie die Zelle langfristig lagern, zerlegen Sie sie. Einen Elektrolyten in einer versiegelten Zelle zu lassen, lädt zur Zersetzung ein.
Zusammenfassende Checkliste
Ein Profi behandelt diesen Prozess als System, nicht als lästige Pflicht.
| Phase | Kritische Aktion | Das „Warum“ |
|---|---|---|
| Inspektion | Auf Verschleiß und Schmutz prüfen. | Verunreinigungen verursachen Nebenreaktionen. |
| Installation | Zentrieren und sicher klemmen. | Die Positionierung bestimmt die Feldgleichmäßigkeit. |
| Anschluss | Anode (+) / Kathode (-) überprüfen. | Umgekehrte Polarität zerstört Elektroden. |
| Wartung | Reinigen, trocknen und zerlegen. | Korrosion verhindert Reproduzierbarkeit. |
Die Rolle zuverlässiger Hardware
Der Prozess ist von größter Bedeutung, aber die Hardware ist das Fundament.
Sie können keine präzise Arbeit mit instabilen Klemmen oder unreinen Metallen leisten. Das beste Protokoll der Welt kann keine Elektrode kompensieren, die unvorhersehbar abgebaut wird, oder eine Zelle, die sich unter thermischer Belastung verzieht.
Hier kommt KINTEK ins Spiel.
Wir sind auf die physische Infrastruktur des Labors spezialisiert. Unsere Elektrolysezellen und Platin- oder Graphitelektroden sind so konzipiert, dass sie den Strapazen wiederholter Nutzung standhalten. Wir bauen unsere Geräte mit den engen Toleranzen, die Ingenieure schätzen, und stellen sicher, dass eine Elektrode, wenn Sie sie zentrieren, zentriert bleibt.
Ihre Forschung verdient Geräte, die so diszipliniert sind wie Sie.
Bereit, Ihr elektrochemisches Setup aufzurüsten?
Kontaktieren Sie unsere Experten, um zu besprechen, wie KINTEK die Präzision Ihres Labors unterstützen kann.
Visuelle Anleitung
Ähnliche Produkte
- Referenzelektrode Kalomel Silberchlorid Quecksilbersulfat für Laborzwecke
- Metall-Scheibenelektrode Elektrochemische Elektrode
- RRDE-Rotations-Scheiben (Ring-Scheiben)-Elektrode / Kompatibel mit PINE, japanischem ALS, Schweizer Metrohm Glaskohlenstoff-Platin
- Rotierende Platindisk-Elektrode für elektrochemische Anwendungen
- Platinblechelektrode für Laboranwendungen in der Batterieforschung
Ähnliche Artikel
- Verwendung und Pflege von Referenzelektroden
- Umfassender Leitfaden für Referenzelektroden: Typen, Anwendungen und Auswahlkriterien
- Pseudo-Referenzelektroden, wann und wie man sie verwendet
- Referenzelektroden: Kalomel, Silberchlorid und Quecksilbersulfat - ein umfassender Leitfaden
- Ein umfassender Leitfaden zu Referenzelektroden




















