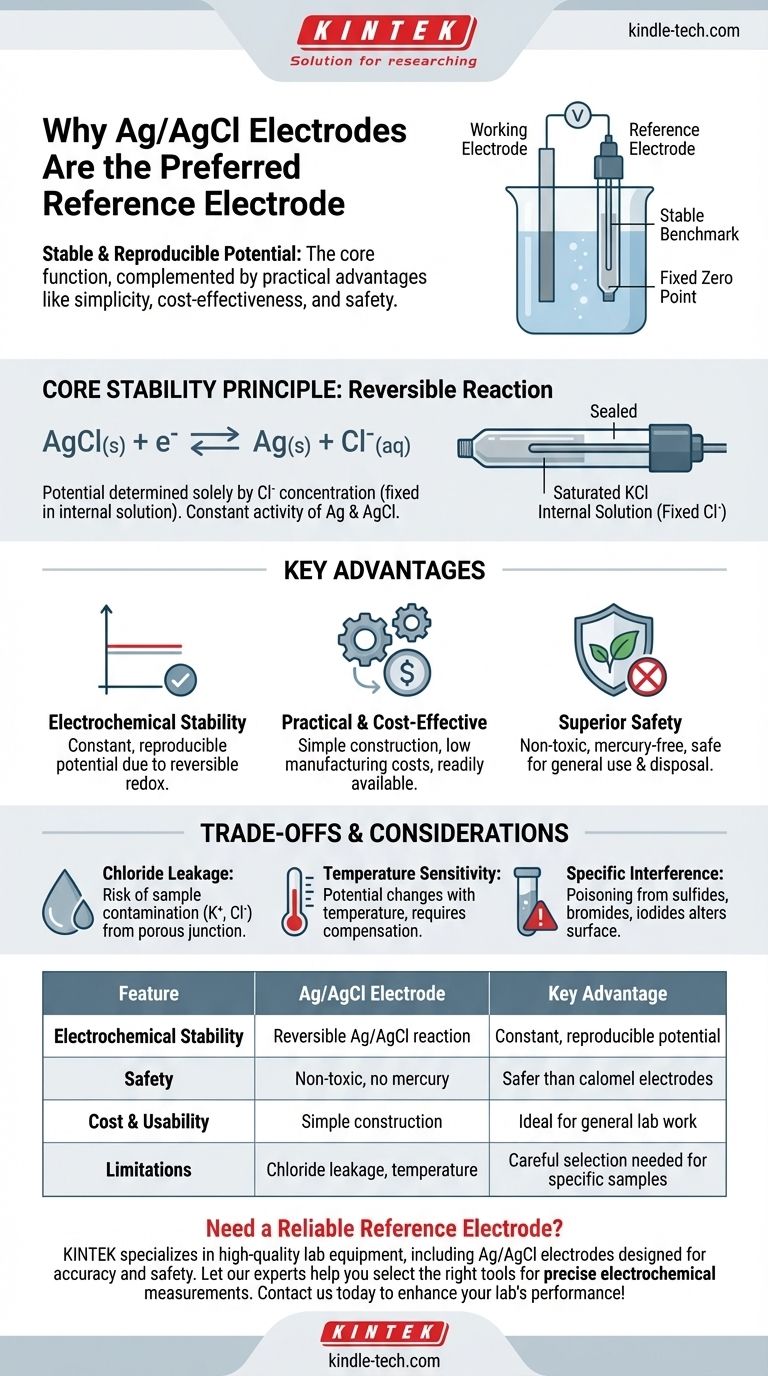
Kurz gesagt, die Silber/Silberchlorid-Elektrode (Ag/AgCl) wird als Referenzelektrode verwendet, weil sie ein hochstabiles und reproduzierbares elektrisches Potenzial liefert. Diese Kernfunktion wird durch ihre praktischen Vorteile ergänzt, darunter die einfache Konstruktion, die Kostengünstigkeit und die deutlich geringere Toxizität im Vergleich zu älteren Alternativen wie der Kalomelelektrode.
Die Hauptaufgabe einer Referenzelektrode ist es, ein stabiler, unveränderlicher Referenzpunkt zu sein. Die Ag/AgCl-Elektrode zeichnet sich bei dieser elektrochemischen Aufgabe aus und ist gleichzeitig sicher, erschwinglich und einfach zu bedienen, was sie zur dominierenden Wahl in der modernen Elektrochemie macht.

Warum Stabilität der Grundstein einer Referenzelektrode ist
Die Kernanforderung: Ein konstantes Potenzial
Eine Referenzelektrode fungiert als fester „Nullpunkt“ in einer elektrochemischen Zelle. Alle anderen Potenzialänderungen der Arbeitselektrode werden gegen diese stabile Basislinie gemessen.
Damit eine Messung genau ist, darf das Potenzial der Referenzelektrode während des Experiments nicht driften oder sich ändern. Sie muss unempfindlich gegenüber der Zusammensetzung der Probenlösung sein, die sie misst.
Das Prinzip einer reversiblen Reaktion
Diese Stabilität wird durch eine gut definierte und reversible elektrochemische Reaktion erreicht. Bei der Ag/AgCl-Elektrode wird das Potenzial ausschließlich durch die Konzentration der Chloridionen (Cl⁻) in ihrer internen Fülllösung bestimmt.
Da diese interne Lösung versiegelt ist und eine feste Konzentration (typischerweise gesättigtes Kaliumchlorid) aufweist, ist das resultierende Elektrodenpotenzial außergewöhnlich konstant und reproduzierbar.
Wie die Ag/AgCl-Elektrode die Schlüsselkriterien erfüllt
Elektrochemische Stabilität
Die Ag/AgCl-Elektrode basiert auf einer einfachen, schnellen und reversiblen Redoxreaktion:
AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq)
Da die Aktivitäten des festen Silbers (Ag) und Silberchlorids (AgCl) konstant sind, hängt das Potenzial nur von der Aktivität des Chloridions ab, die im Elektrodenkörper konstant gehalten wird.
Praktische Vorteile gegenüber Alternativen
Die weite Verbreitung der Ag/AgCl-Elektrode ist auch auf ihre erheblichen praktischen Vorteile zurückzuführen. Sie ist einfach herzustellen, was zu niedrigen Kosten für kommerzielle Elektroden führt.
Überlegenes Sicherheitsprofil
Entscheidend ist, dass sie ungiftig ist. Dies verschafft ihr einen großen Vorteil gegenüber der einst gebräuchlichen gesättigten Kalomelelektrode (SCE), die hochgiftiges Quecksilber enthält und Entsorgungs- und Sicherheitsrisiken birgt. Aus diesem Grund hat die Ag/AgCl-Elektrode die Kalomelelektroden im allgemeinen Laborgebrauch weitgehend ersetzt.
Verständnis der Kompromisse und Einschränkungen
Keine Elektrode ist für jede Situation perfekt. Das Verständnis der Einschränkungen der Ag/AgCl-Elektrode ist entscheidend, um genaue Messungen zu gewährleisten.
Kontamination durch Chloridleckage
Das häufigste Problem ist das langsame Austreten der KCl-Fülllösung aus dem porösen Diaphragma der Elektrode in die Probe. Dies kann Proben kontaminieren, die empfindlich auf Kalium- (K⁺) oder Chloridionen (Cl⁻) reagieren.
Beispielsweise würde die Messung von Chlorid in einer Wasserprobe mit einer Standard-Ag/AgCl-Elektrode aufgrund dieser Leckage künstlich hohe Ergebnisse liefern.
Temperaturempfindlichkeit
Das Potenzial einer Ag/AgCl-Elektrode ist temperaturabhängig. Obwohl diese Beziehung vorhersehbar ist, bedeutet dies, dass für hochpräzise Arbeiten die Temperatur kontrolliert oder ihr Effekt in Berechnungen kompensiert werden muss.
Interferenz in spezifischen Proben
Die Elektrode kann „vergiftet“ werden, wenn die Probe Substanzen enthält, die mit Silber reagieren, wie Proteine mit Sulfidgruppen, Bromidionen oder Iodidionen. Diese Reaktion verändert die Oberfläche der Elektrode und führt zu einem unvorhersehbaren Driften des Potenzials.
Die richtige Wahl für Ihr Ziel treffen
Bei der Auswahl einer Referenzelektrode bestimmt Ihr primäres Ziel die beste Wahl.
- Wenn Ihr Hauptaugenmerk auf allgemeiner Laborarbeit liegt (z. B. pH-Messungen): Die Standard-Ag/AgCl-Elektrode ist aufgrund ihrer hervorragenden Balance aus Stabilität, geringen Kosten und Sicherheit die ideale Standardwahl.
- Wenn Ihr Hauptaugenmerk auf der Analyse von Proben liegt, die empfindlich auf Chlorid oder Kalium reagieren: Sie müssen eine Doppel-Diaphragma-Referenzelektrode verwenden, die eine zweite äußere Kammer besitzt, um zu verhindern, dass die KCl-Lösung Ihre Probe kontaminiert.
- Wenn Ihr Hauptaugenmerk auf der Arbeit in nicht-wässrigen Lösungsmitteln oder bei hohen Temperaturen liegt: Die Leistung einer Standard-Ag/AgCl-Elektrode kann beeinträchtigt sein, und Sie müssen möglicherweise spezialisierte Referenzelektroden untersuchen, die für diese spezifischen Bedingungen entwickelt wurden.
Das Verständnis dieser Kernprinzipien befähigt Sie, nicht nur eine Elektrode, sondern das richtige Werkzeug auszuwählen, um genaue und zuverlässige Messungen zu gewährleisten.
Zusammenfassungstabelle:
| Merkmal | Ag/AgCl-Elektrode | Hauptvorteil |
|---|---|---|
| Elektrochemische Stabilität | Basiert auf einer reversiblen Ag/AgCl-Reaktion | Bietet ein konstantes, reproduzierbares Potenzial |
| Sicherheit | Ungiftig, kein Quecksilber | Sicherer als Kalomelelektroden |
| Kosten & Benutzerfreundlichkeit | Einfach zu konstruieren und kostengünstig | Ideal für allgemeine Laborarbeiten |
| Einschränkungen | Risiko der Chloridleckage, Temperaturempfindlichkeit | Erfordert sorgfältige Auswahl für spezifische Proben |
Benötigen Sie eine zuverlässige Referenzelektrode für Ihr Labor? KINTEK ist spezialisiert auf hochwertige Laborgeräte und Verbrauchsmaterialien, einschließlich Ag/AgCl-Elektroden, die für Genauigkeit und Sicherheit entwickelt wurden. Lassen Sie sich von unseren Experten bei der Auswahl der richtigen Werkzeuge für präzise elektrochemische Messungen unterstützen. Kontaktieren Sie uns noch heute, um die Leistung Ihres Labors zu verbessern!
Visuelle Anleitung
Ähnliche Produkte
- Referenzelektrode Kalomel Silberchlorid Quecksilbersulfat für Laborzwecke
- Goldplattierte Elektrode
- Rotierende Platindisk-Elektrode für elektrochemische Anwendungen
- Platinblechelektrode für Labor- und Industrieanwendungen
- Gold-Elektrodenblech Gold-Elektrode
Andere fragen auch
- Welche Elektrode wird als Erdreferenz verwendet? Beherrschen Sie den Schlüssel zu genauen elektrochemischen Messungen
- Wie korreliert die Wahl von Referenzelektroden wie Ag/AgCl oder Hg/HgO mit dem Elektrolyt-pH bei Wasserstoffentwicklungsreaktions (HER)-Tests?
- Welche Art von Elektrode kann als Referenzpunkt verwendet werden? Wählen Sie die richtige für genaue Messungen
- Warum ist die Auswahl einer hochwertigen Referenzelektrode für die elektrochemische Synthese entscheidend? | KINTEK
- Welche Elektrode wird als Referenz verwendet? Ein Leitfaden für genaue elektrochemische Messungen












