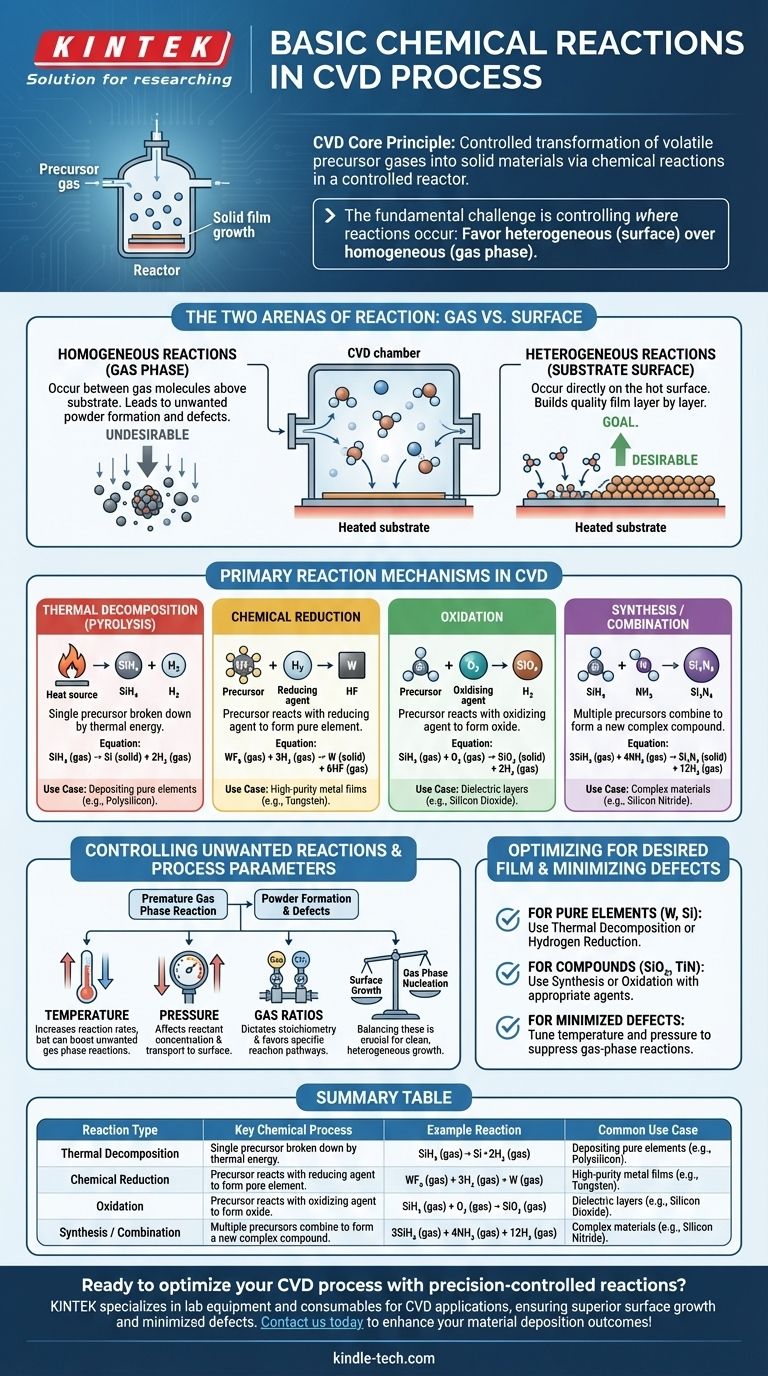
Im Kern ist die chemische Gasphasenabscheidung (CVD) ein Prozess kontrollierter chemischer Reaktionen. Diese Reaktionen sind darauf ausgelegt, stabile, flüchtige Precursor-Gase in ein festes, nichtflüchtiges Material direkt auf einem Substrat umzuwandeln. Die häufigsten Mechanismen, die diese Umwandlung antreiben, sind die thermische Zersetzung (Pyrolyse), chemische Reduktion, Oxidation und Synthesereaktionen, die alle in einer hochkontrollierten Reaktor-Umgebung stattfinden.
Die grundlegende Herausforderung bei jedem CVD-Prozess besteht nicht nur darin, chemische Reaktionen einzuleiten, sondern präzise zu steuern, wo sie stattfinden. Ziel ist es, heterogene Reaktionen auf der Substratoberfläche zu begünstigen, um einen qualitativ hochwertigen Film aufzubauen, während homogene Reaktionen in der Gasphase, die unerwünschte Partikel erzeugen, minimiert werden.

Die zwei Reaktionsbereiche: Gas vs. Oberfläche
Jede chemische Reaktion in einer CVD-Kammer findet an einem von zwei Orten statt. Das Gleichgewicht zwischen ihnen bestimmt die Qualität und Struktur des Endmaterials.
Homogene Reaktionen (In der Gasphase)
Diese Reaktionen treten zwischen Gasmolekülen selbst auf, die im Raum über dem Substrat suspendiert sind.
Während eine gewisse Gasphasenchemie notwendig ist, um reaktive Zwischenspezies zu erzeugen, sind übermäßige homogene Reaktionen oft unerwünscht. Sie können zur Bildung von festen Partikeln oder "Pulvern" führen, die dann auf das Substrat herabregnen, Defekte verursachen und die Filmqualität beeinträchtigen.
Heterogene Reaktionen (Auf der Substratoberfläche)
Dies sind die Reaktionen, die den Film aufbauen. Sie finden direkt auf oder in einer sehr dünnen Schicht angrenzend an die erhitzte Substratoberfläche statt.
Das Ziel eines gut konzipierten CVD-Prozesses ist es, die Rate heterogener Reaktionen zu maximieren. Precursor-Gase adsorbieren auf der heißen Oberfläche, zersetzen sich oder reagieren mit anderen adsorbierten Spezies und bilden den stabilen festen Film Schicht für Schicht.
Primäre Reaktionsmechanismen in CVD
Obwohl sie in einem der beiden oben genannten "Bereiche" stattfinden, können die Reaktionen selbst basierend auf der beteiligten chemischen Umwandlung in mehrere Schlüsseltypen eingeteilt werden.
Thermische Zersetzung (Pyrolyse)
Dies ist der einfachste und häufigste CVD-Reaktionstyp. Ein einzelnes Precursor-Gas wird allein durch thermische Energie in seine Bestandteile zerlegt.
Die Wärme vom Substrat liefert die Energie, die zum Brechen der chemischen Bindungen des Precursor-Moleküls benötigt wird, wodurch das gewünschte feste Element auf der Oberfläche abgeschieden wird. Ein klassisches Beispiel ist die Abscheidung von Polysilizium aus Silan-Gas.
SiH₄ (Gas) → Si (Feststoff) + 2H₂ (Gas)
Chemische Reduktion
Bei diesem Prozess reagiert ein Precursor-Gas (oft ein Metallhalogenid) mit einem Reduktionsmittel, typischerweise Wasserstoff (H₂), um einen reinen elementaren Film zu bilden.
Dies ist eine gängige Methode zur Abscheidung hochreiner Metallfilme wie Wolfram. Der Wasserstoff entfernt die Halogenatome vom Metall-Precursor, wodurch das reine Metall abgeschieden werden kann.
WF₆ (Gas) + 3H₂ (Gas) → W (Feststoff) + 6HF (Gas)
Oxidation
Diese Reaktion beinhaltet ein Precursor-Gas, das mit einem Oxidationsmittel wie Sauerstoff (O₂), Lachgas (N₂O) oder Wasserdampf (H₂O) reagiert, um einen festen Oxidfilm zu bilden.
Dies ist der grundlegende Prozess zur Herstellung isolierender dielektrischer Schichten wie Siliziumdioxid (SiO₂), einem kritischen Bestandteil in nahezu allen modernen Mikroelektronik.
SiH₄ (Gas) + O₂ (Gas) → SiO₂ (Feststoff) + 2H₂ (Gas)
Synthese oder Kombination
Hier werden zwei oder mehr Precursor-Gase eingeführt, um sich zu einem neuen Verbundmaterial auf dem Substrat zu verbinden. Dies ermöglicht die Herstellung komplexer Materialien, die nicht durch einfache Zersetzung gebildet werden können.
Zum Beispiel wird Siliziumnitrid (Si₃N₄), ein hartes und chemisch beständiges Material, durch die Reaktion einer Siliziumquelle mit einer Stickstoffquelle, wie Ammoniak, gebildet.
3SiH₄ (Gas) + 4NH₃ (Gas) → Si₃N₄ (Feststoff) + 12H₂ (Gas)
Die Kompromisse verstehen: Unerwünschte Reaktionen kontrollieren
Der Erfolg eines CVD-Prozesses hängt vollständig von der Kontrolle der Reaktionsumgebung ab, um die gewünschten chemischen Wege zu begünstigen.
Das Problem der Pulverbildung
Die Hauptfalle bei CVD ist die unbeabsichtigte Gasphasennukleation. Wenn die Reaktortemperatur zu hoch oder der Druck zu groß ist, können Precursor-Gase vorzeitig in der Gasphase (homogene Reaktion) reagieren, bevor sie das Substrat erreichen. Dies erzeugt Partikel, die Defekte verursachen oder einen Film mit geringer Dichte, pulvrig statt einer hochwertigen, dichten Schicht bilden können.
Die Rolle der Prozessparameter
Ingenieure verwenden mehrere Schlüsselparameter als Hebel, um die Reaktionskinetik und den Ort zu steuern:
- Temperatur: Erhöht die Reaktionsraten, kann aber auch unerwünschte Gasphasenreaktionen verstärken.
- Druck: Beeinflusst die Konzentration der Reaktanten und wie schnell sie zur Oberfläche gelangen.
- Gasverhältnisse: Bestimmt die Stöchiometrie und steuert, welcher Reaktionsweg bevorzugt wird.
Das Ausbalancieren dieser Faktoren ist entscheidend für die Förderung eines sauberen, heterogenen Wachstums auf der Substratoberfläche.
Reaktionen für Ihren gewünschten Film optimieren
Der spezifische chemische Reaktionsweg, den Sie anwenden, wird vollständig durch das Material bestimmt, das Sie erzeugen möchten.
- Wenn Ihr Hauptaugenmerk auf der Abscheidung eines reinen Elements liegt (z. B. Wolfram, Silizium): Sie werden wahrscheinlich auf thermische Zersetzung oder eine Wasserstoffreduktionsreaktion unter Verwendung eines einzelnen Precursors und möglicherweise eines Reduktionsmittels zurückgreifen.
- Wenn Ihr Hauptaugenmerk auf der Erzeugung eines Oxid- oder Nitrid-Verbundmaterials liegt (z. B. SiO₂, TiN): Sie werden eine Synthese- oder Oxidationsreaktion verwenden, indem Sie ein oxidierendes oder nitrierendes Mittel neben Ihrem Haupt-Precursor einführen.
- Wenn Ihr Hauptaugenmerk auf der Minimierung von Defekten und der Erzielung eines hochwertigen Films liegt: Ihre Hauptaufgabe besteht darin, Temperatur und Druck so einzustellen, dass homogene Gasphasenreaktionen unterdrückt und ein sauberes, heterogenes Wachstum auf dem Substrat gefördert wird.
Letztendlich ist die Beherrschung von CVD die Beherrschung der Kunst, die Chemie so zu steuern, dass sie zu einer bestimmten Zeit und an einem bestimmten Ort stattfindet.
Zusammenfassungstabelle:
| Reaktionstyp | Wichtiger chemischer Prozess | Beispielreaktion | Häufiger Anwendungsfall |
|---|---|---|---|
| Thermische Zersetzung (Pyrolyse) | Einzelner Precursor zerfällt durch Wärme | SiH₄ (Gas) → Si (Feststoff) + 2H₂ (Gas) | Abscheidung reiner Elemente wie Polysilizium |
| Chemische Reduktion | Precursor reagiert mit einem Reduktionsmittel (z. B. H₂) | WF₆ (Gas) + 3H₂ (Gas) → W (Feststoff) + 6HF (Gas) | Hochreine Metallfilme (z. B. Wolfram) |
| Oxidation | Precursor reagiert mit einem Oxidationsmittel (z. B. O₂) | SiH₄ (Gas) + O₂ (Gas) → SiO₂ (Feststoff) + 2H₂ (Gas) | Dielektrische Schichten wie Siliziumdioxid |
| Synthese/Kombination | Mehrere Precursoren verbinden sich zu einer Verbindung | 3SiH₄ (Gas) + 4NH₃ (Gas) → Si₃N₄ (Feststoff) + 12H₂ (Gas) | Komplexe Materialien wie Siliziumnitrid |
Bereit, Ihren CVD-Prozess mit präzisionsgesteuerten Reaktionen zu optimieren? KINTEK ist spezialisiert auf Laborgeräte und Verbrauchsmaterialien für CVD-Anwendungen und hilft Ihnen, defektfreie Dünnschichten durch maßgeschneiderte Reaktorlösungen zu erzielen. Egal, ob Sie Metalle, Oxide oder Nitride abscheiden, unser Fachwissen gewährleistet überlegenes Oberflächenwachstum und minimierte Gasphasendefekte. Kontaktieren Sie uns noch heute, um zu besprechen, wie unsere CVD-Systeme Ihre Materialabscheidungsergebnisse verbessern können!
Visuelle Anleitung
Ähnliche Produkte
- Kundenspezifische vielseitige CVD-Rohröfen-Systemausrüstung für die chemische Gasphasenabscheidung
- Chemische Gasphasenabscheidung CVD-Anlagensystem Kammer-Schiebe-PECVD-Rohroofen mit Flüssigkeitsvergaser PECVD-Maschine
- CVD-Diamant für Wärmemanagementanwendungen
- HFCVD-Maschinensystemausrüstung für Ziehstein-Nanodiamantbeschichtung
- Kundenspezifische CVD-Diamantbeschichtung für Laboranwendungen
Andere fragen auch
- Was ist ein CVD-Röhrenofen? Ein vollständiger Leitfaden zur Dünnschichtabscheidung
- Was ist die Funktion eines Rohrofens bei der CVD-SiC-Synthese? Herstellung von ultrareinem Siliziumkarbidpulver
- Was ist die Anwendung von CVD in der Nanotechnologie? Nutzen Sie atomare Präzision für Materialien der nächsten Generation
- Welche Auswirkung hat die Temperatur auf Graphenoxid? Beherrschen Sie die thermische Reduktion für präzise Materialeigenschaften
- Was ist die Bedeutung der Synthese von Graphen? Ein Leitfaden zu Top-Down- vs. Bottom-Up-Methoden