Die grundlegende Vorsichtsmaßnahme bei der Verwendung einer Platinscheibenelektrode besteht darin, einen Elektrolyten zu wählen, der die Elektrodenoberfläche chemisch nicht angreift oder physikalisch verunreinigt. Platin ist weniger inert, als oft angenommen wird, und bestimmte Ionen können irreversible Korrosion oder Verschmutzung verursachen, was die Integrität Ihrer Daten und die Langlebigkeit der Elektrode beeinträchtigt. Insbesondere müssen Sie jeglichen Kontakt mit Lithiumionen vermeiden und bei Halogenidionen wie Chlorid äußerst vorsichtig sein.
Die Leistung Ihrer Platinelektrode hängt vollständig vom Zustand ihrer Oberfläche ab. Das primäre Ziel ist es, einen Elektrolyten zu wählen, der Leitfähigkeit bietet, ohne zu stören, und sicherzustellen, dass das gemessene elektrochemische Verhalten von Ihrem Experiment stammt und nicht von unbeabsichtigten Nebenreaktionen oder Elektrodenabbau.

Der Mythos der "inerten" Elektrode
Viele halten Platin für ein völlig inertes Material, doch in der Elektrochemie ist dies eine gefährliche Vereinfachung. Die Oberfläche ist hochaktiv und empfindlich gegenüber ihrer chemischen Umgebung.
Katalytische Natur von Platin
Eine Platinelektrodenoberfläche ist nicht nur ein passiver Elektronenleiter. Sie ist eine hochaktive katalytische Stelle, an der elektrochemische Reaktionen stattfinden. Der genaue Zustand dieser Oberfläche bestimmt die Geschwindigkeit und den Weg dieser Reaktionen.
Wie Elektrolyte die Leistung beeinträchtigen
Wenn ein Elektrolyt korrosive Ionen oder adsorbierende Verunreinigungen enthält, verändert er direkt die aktive Oberfläche der Elektrode. Dies verursacht nicht nur physische Schäden; es verändert grundlegend die Kinetik der Reaktion, die Sie untersuchen möchten, was zu ungenauen und nicht reproduzierbaren Ergebnissen führt.
Zu vermeidende Schlüsselkomponenten des Elektrolyten
Um die Integrität der Platinoberfläche zu erhalten, müssen bestimmte chemische Spezies in Ihrer Elektrolytlösung streng kontrolliert oder eliminiert werden.
Das Verbot von Lithiumionen
Die Referenzen sind explizit: Lithiumionen (Li⁺) sind korrosiv für Platin. Ihre Verwendung ist oft von Elektrodenherstellern untersagt. Es kann zu einer Legierungsbildung zwischen Lithium und Platin kommen, die die Elektrodenstruktur dauerhaft schädigt.
Die Gefahr von Halogenidionen (Cl⁻, Br⁻)
Halogenidionen, insbesondere Chlorid, sind berüchtigt dafür, Korrosion von Platin zu verursachen, besonders bei positiven (anodischen) Potentialen. Sie können stabile, lösliche Platin-Halogenid-Komplexe bilden, die im Laufe der Zeit Platinatome von der Elektrodenoberfläche effektiv ablösen.
Verunreinigung durch organische Substanzen
Viele organische Moleküle können stark an der Platinoberfläche adsorbieren. Dieser Prozess, bekannt als Fouling (Verschmutzung), blockiert die aktiven Stellen, die für Ihre gewünschte Reaktion benötigt werden, was den elektrochemischen Prozess, den Sie messen, dramatisch verlangsamen oder stoppen kann.
Die Kompromisse und Best Practices verstehen
Die Wahl des richtigen Elektrolyten beinhaltet mehr als nur das Vermeiden schädlicher Substanzen. Sie erfordert einen proaktiven Ansatz zur Aufrechterhaltung einer makellosen elektrochemischen Umgebung.
Die Rolle eines "Träger"-Elektrolyten
Die Hauptfunktion des Elektrolyten besteht darin, die Leitfähigkeit der Lösung zu gewährleisten. Ein idealer Trägerelektrolyt enthält Ionen, die in Ihrem Potentialfenster elektrochemisch inaktiv sind und nicht mit der Elektrodenoberfläche interagieren. Aus diesem Grund werden oft nicht-koordinierende Elektrolyte auf Basis von Salzen wie Perchloraten (z. B. NaClO₄) oder Tetrafluoroboraten (z. B. KBF₄) bevorzugt.
Die entscheidende Bedeutung der Reinheit
Spurenverunreinigungen in Ihrem Lösungsmittel oder Elektrolytsalz können eine Hauptquelle für Kontaminationen sein. Verwenden Sie immer hochreine Reagenzien in Elektrochemie-Qualität, wann immer möglich, um das Risiko der Einführung unbekannter Spezies zu minimieren, die Ihre Elektrode verschmutzen oder korrodieren könnten.
Mechanische vs. chemische Beschädigung
Denken Sie daran, dass Platin ein weiches Metall ist. Mechanische Beschädigungen durch Kratzer oder Stöße erzeugen energiereiche Oberflächenstellen. Diese beschädigten Bereiche sind oft anfälliger für chemische Angriffe und Korrosion durch den Elektrolyten als eine glatte, polierte Oberfläche.
Die richtige Wahl für Ihr Ziel treffen
Ihr experimentelles Ziel sollte Ihr Vorsichtsniveau und Ihre Materialwahl leiten.
- Wenn Ihr Hauptaugenmerk auf Genauigkeit und Wiederholbarkeit liegt: Priorisieren Sie hochreine, nicht-koordinierende Elektrolyte und reinigen Sie Ihre Glaswaren sorgfältig, um jegliche Quellen von Halogenid- oder organischer Kontamination zu vermeiden.
- Wenn Sie neue chemische Systeme untersuchen: Führen Sie immer einen Hintergrundscan (z. B. ein leeres zyklisches Voltamogramm) nur mit Ihrer Elektrode und dem neuen Elektrolyten durch, um unerwartete Reaktionen zu überprüfen, bevor Sie Ihren Analyten hinzufügen.
- Wenn Ihr Ziel die langfristige Gesundheit der Elektrode ist: Erstellen Sie eine Checkliste verbotener Substanzen für Ihr Labor und implementieren Sie ein strenges Protokoll zur Reinigung und Inspektion der Elektrodenoberfläche nach jeder Verwendung.
Letztendlich ist ein gut gewählter Elektrolyt die Grundlage für die Erzeugung zuverlässiger und vertrauenswürdiger elektrochemischer Daten.
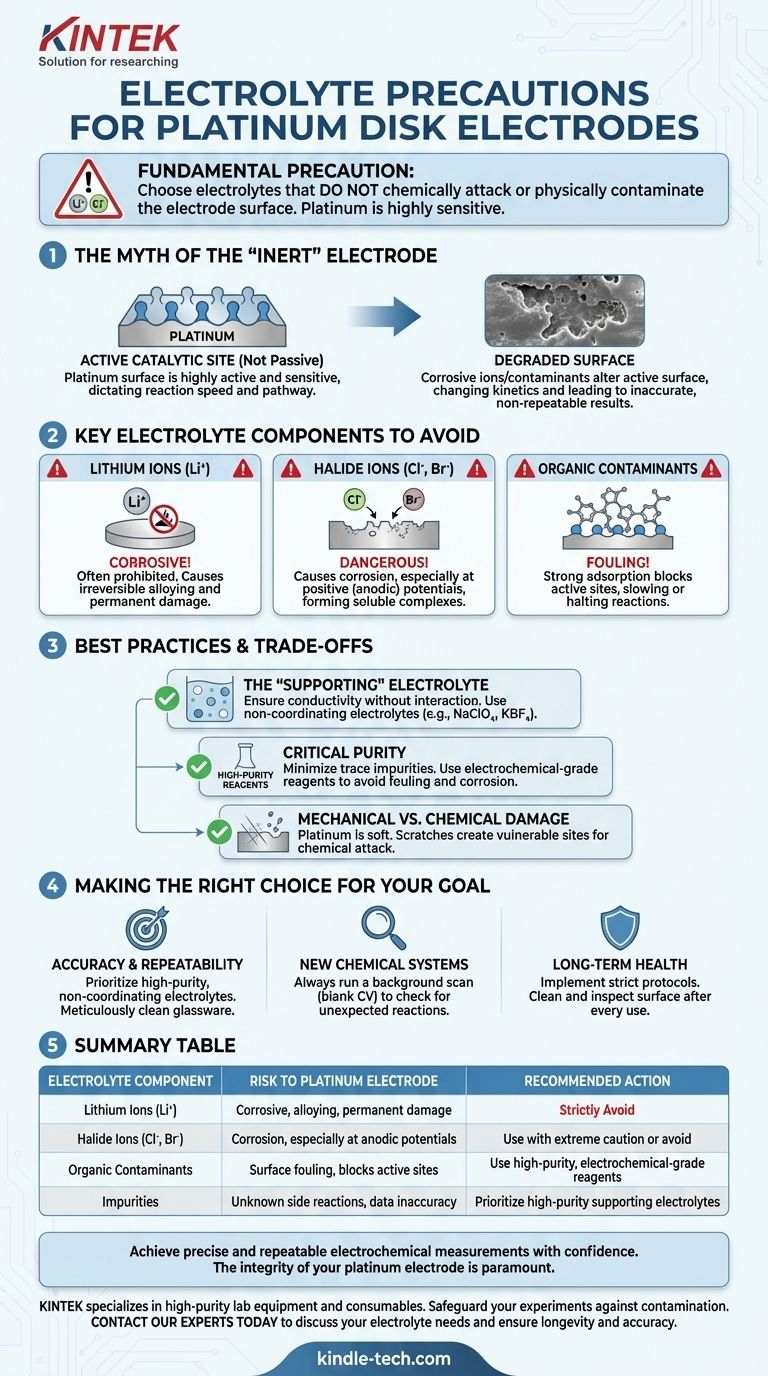
Zusammenfassungstabelle:
| Elektrolytkomponente | Risiko für Platinelektrode | Empfohlene Maßnahme |
|---|---|---|
| Lithiumionen (Li⁺) | Korrosiv, kann Legierungsbildung und dauerhafte Schäden verursachen | Streng vermeiden |
| Halogenidionen (Cl⁻, Br⁻) | Korrosion, besonders bei anodischen Potentialen | Mit äußerster Vorsicht verwenden oder vermeiden |
| Organische Verunreinigungen | Oberflächenverschmutzung, blockiert aktive Stellen | Hochreine Reagenzien in Elektrochemie-Qualität verwenden |
| Verunreinigungen | Unbekannte Nebenreaktionen, Datenungenauigkeit | Hochreine Trägerelektrolyte (z. B. Perchlorate) priorisieren |
Erzielen Sie präzise und wiederholbare elektrochemische Messungen mit Zuversicht. Die Integrität Ihrer Platinelektrode ist für Ihre Forschung von größter Bedeutung. KINTEK ist spezialisiert auf die Bereitstellung hochwertiger Laborgeräte und Verbrauchsmaterialien, einschließlich elektrochemischer Reagenzien und zuverlässiger Elektroden, um Ihre Experimente vor Kontamination und Korrosion zu schützen. Kontaktieren Sie noch heute unsere Experten, um Ihre spezifischen Elektrolytanforderungen zu besprechen und die Langlebigkeit und Genauigkeit Ihres elektrochemischen Aufbaus zu gewährleisten.
Visuelle Anleitung
Ähnliche Produkte
- Rotierende Platindisk-Elektrode für elektrochemische Anwendungen
- RRDE-Rotations-Scheiben (Ring-Scheiben)-Elektrode / Kompatibel mit PINE, japanischem ALS, Schweizer Metrohm Glaskohlenstoff-Platin
- Platinblechelektrode für Labor- und Industrieanwendungen
- Platinblechelektrode für Laboranwendungen in der Batterieforschung
- Platin-Hilfselektrode für Laboranwendungen
Andere fragen auch
- Was kann eine Vergiftung einer Platinscheibenelektrode verursachen und wie kann sie verhindert werden? Sorgen Sie für zuverlässige elektrochemische Daten
- Welche Temperaturgrenzen gelten für eine Platinscheibenelektrode? Der kritische Faktor ist der Isolierkörper
- Wie kann die Oberfläche einer abgenutzten oder zerkratzten Platinelektrode wiederhergestellt werden? Erreichen Sie ein spiegelglattes Finish für zuverlässige Daten
- Wie lautet das korrekte Nachbehandlungsverfahren für eine Platinelektrode? Bewahren Sie Ihre Elektrode für genaue Ergebnisse
- Welche Rolle spielt eine Platindrahtelektrode üblicherweise? Ein Leitfaden zu ihrer primären Verwendung als Arbeitselektrode









