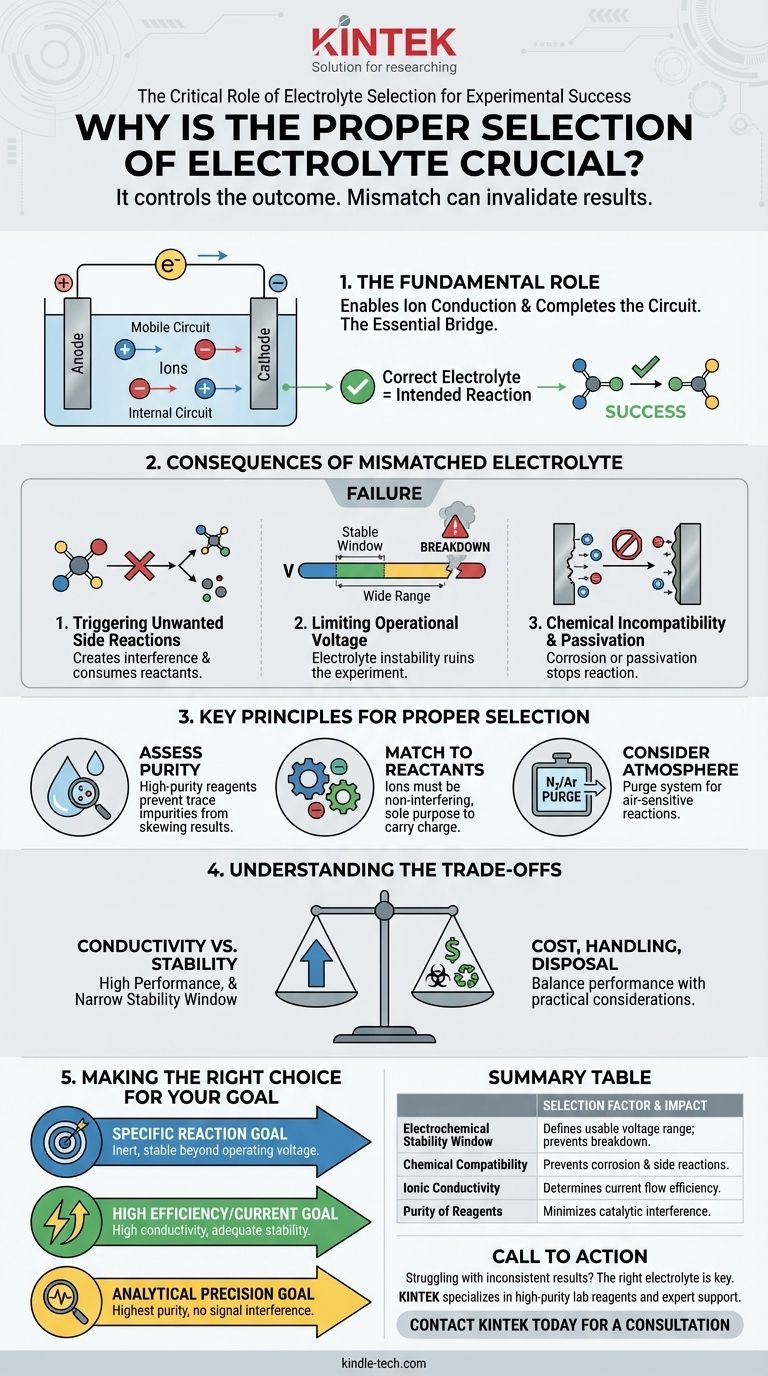
Die Wahl des richtigen Elektrolyten ist entscheidend, da sie das Ergebnis Ihres Experiments direkt beeinflusst. Der Elektrolyt ist kein passives Hintergrundmedium; er ist eine aktive Komponente, die sorgfältig ausgewählt werden muss, um sicherzustellen, dass Ihre beabsichtigte Reaktion korrekt abläuft und unerwünschte Nebenreaktionen verhindert werden, die Ihre Ergebnisse ungültig machen könnten.
Die Kernfunktion eines Elektrolyten besteht darin, den Stromkreis durch Ionenleitung zu schließen, aber seine chemischen Eigenschaften bestimmen, welche Reaktionen möglich sind. Eine Diskrepanz zwischen dem Elektrolyten und dem experimentellen System kann zu völlig unterschiedlichen und unbeabsichtigten chemischen Umwandlungen führen.

Die grundlegende Rolle eines Elektrolyten
Ein Elektrolyt ist die wesentliche Brücke in jeder elektrochemischen Zelle. Seine Hauptaufgabe ist der Ladungstransport in Form von Ionen, wodurch der Stromkreis zwischen den beiden Elektroden geschlossen werden kann.
Ermöglichung der Ionenleitung
Der Elektrolyt enthält bewegliche Ionen (Kationen und Anionen), die sich als Reaktion auf das elektrische Feld bewegen. Diese Bewegung geladener Teilchen stellt den Stromfluss innerhalb der Zelle dar.
Schließen des Stromkreises
Elektronen fließen durch den externen Draht, aber Ionen müssen durch den Elektrolyten fließen. Ohne diesen internen ionischen Pfad wäre der Stromkreis unterbrochen, und es könnte keine elektrochemische Reaktion stattfinden.
Warum ein unpassender Elektrolyt Ergebnisse ungültig macht
Die Wahl des falschen Elektrolyten ist eine der häufigsten Ursachen, um ein Experiment zum Scheitern zu bringen. Sie kann Variablen einführen, die den Prozess, den Sie untersuchen möchten, vollständig verschleiern.
Auslösen unerwünschter Nebenreaktionen
Die Bestandteile des Elektrolyten können mit Ihren Elektroden, Ihrem Lösungsmittel oder der Substanz, die Sie analysieren, reagieren. Dies erzeugt Nebenprodukte, die Reaktanten verbrauchen und Messungen stören.
Begrenzung der Betriebsspannung
Jeder Elektrolyt hat ein elektrochemisches Stabilitätsfenster. Dies ist der Spannungsbereich, in dem er inert bleibt. Wenn Ihr Experiment eine Spannung außerhalb dieses Fensters erfordert, zerfällt der Elektrolyt selbst (oxidiert oder reduziert), was das Experiment ruiniert.
Chemische Inkompatibilität und Passivierung
Ein Elektrolyt kann chemisch aggressiv gegenüber Ihren Elektrodenmaterialien sein und diese korrodieren oder auflösen. Er kann auch eine Passivierungsschicht – einen nichtleitenden Film – auf der Elektrodenoberfläche bilden, die die Reaktion vollständig stoppt.
Schlüsselprinzipien für die richtige Auswahl
Eine bewusste Wahl erfordert das Verständnis der Eigenschaften, die einen geeigneten Elektrolyten für Ihr spezifisches Ziel definieren.
Beurteilung der Reinheit der Reagenzien
Die Reinheit der Bestandteile Ihres Elektrolyten ist von größter Bedeutung. Selbst Spurenverunreinigungen können als Katalysatoren für Nebenreaktionen wirken oder sich auf den Elektroden ablagern, was Ihre Ergebnisse verfälscht. Verwenden Sie immer hochreine Reagenzien und deionisiertes oder destilliertes Wasser.
Anpassung des Elektrolyten an die Reaktanten
Die Ionen innerhalb des Elektrolyten müssen nicht störend sein. Sie sollten nicht an der primären elektrochemischen Reaktion teilnehmen, die Sie antreiben möchten. Ihr einziger Zweck sollte der Ladungstransport sein.
Berücksichtigung der erforderlichen Atmosphäre
Einige Experimente sind sehr empfindlich gegenüber Luft. Wenn Ihr System eine inerte Atmosphäre (wie Stickstoff oder Argon) erfordert, müssen Sie die Zelle vor Zugabe des Elektrolyten spülen, um zu verhindern, dass Sauerstoff oder Feuchtigkeit parasitäre Reaktionen verursachen.
Verständnis der Kompromisse
Die Wahl eines Elektrolyten beinhaltet oft das Abwägen konkurrierender Faktoren. Es gibt selten eine einzige "perfekte" Option.
Leitfähigkeit vs. Stabilität
Ein Elektrolyt mit sehr hoher Ionenleitfähigkeit bietet möglicherweise eine hervorragende Leistung, hat aber möglicherweise ein enges Stabilitätsfenster. Möglicherweise müssen Sie etwas Leistung opfern, um einen Elektrolyten zu erhalten, der bei Ihren erforderlichen Spannungen stabil bleibt.
Kosten und Handhabung
Praktische Überlegungen sind wichtig. Einige Hochleistungselektrolyte können teuer, hochgiftig sein oder spezielle Handhabungsverfahren (z. B. in einer Handschuhbox) erfordern. Diese Faktoren müssen gegen die experimentellen Anforderungen abgewogen werden.
Entsorgung nach dem Experiment
Der Auswahlprozess endet nicht mit dem Experiment. Sie müssen einen Elektrolyten wählen, für den Sie einen klaren und sicheren Entsorgungsplan haben, sei es Neutralisation, Recycling oder spezielle chemische Abfallentsorgung.
Die richtige Wahl für Ihr Ziel treffen
Ihr experimentelles Ziel sollte die ultimative Richtschnur für Ihre Auswahl sein.
- Wenn Ihr Hauptaugenmerk auf der Erzielung einer spezifischen Reaktion liegt: Wählen Sie einen Elektrolyten, der gegenüber allen Komponenten in Ihrem System völlig inert und weit über Ihre Betriebsspannung hinaus stabil ist.
- Wenn Ihr Hauptaugenmerk auf hoher Effizienz oder Strom liegt: Priorisieren Sie einen Elektrolyten mit hoher Ionenleitfähigkeit und stellen Sie sicher, dass sein Stabilitätsfenster für Ihre Bedürfnisse immer noch ausreichend ist.
- Wenn Ihr Hauptaugenmerk auf analytischer Präzision liegt: Verwenden Sie die reinsten verfügbaren Reagenzien und stellen Sie sicher, dass die Elektrolytionen das Signal, das Sie messen möchten, nicht stören.
Letztendlich stellt ein gut gewählter Elektrolyt sicher, dass die von Ihnen gesammelten Daten den Prozess widerspiegeln, den Sie untersuchen wollten.
Zusammenfassungstabelle:
| Auswahlfaktor | Auswirkung auf das Experiment |
|---|---|
| Elektrochemisches Stabilitätsfenster | Definiert den nutzbaren Spannungsbereich; eine Diskrepanz führt zum Elektrolytzerfall. |
| Chemische Kompatibilität | Verhindert Korrosion, Passivierung und unerwünschte Nebenreaktionen mit Elektroden/Lösungsmitteln. |
| Ionenleitfähigkeit | Bestimmt die Effizienz des Stromflusses innerhalb der Zelle. |
| Reinheit der Reagenzien | Spurenverunreinigungen können Nebenreaktionen katalysieren und Ergebnisse verfälschen. |
Haben Sie Probleme mit inkonsistenten elektrochemischen Ergebnissen? Der richtige Elektrolyt ist entscheidend. KINTEK ist spezialisiert auf hochreine Laborreagenzien und Verbrauchsmaterialien und bietet die zuverlässigen Elektrolyte und die fachkundige Unterstützung, die Ihr Labor benötigt, um experimentelle Genauigkeit und Effizienz zu gewährleisten.
Lassen Sie sich von unseren Experten bei der Auswahl des perfekten Elektrolyten für Ihre Anwendung helfen.
Kontaktieren Sie KINTEK noch heute für eine Beratung, um Ihre spezifischen Anforderungen zu besprechen und die Leistung Ihres Labors zu verbessern.
Visuelle Anleitung