Anforderungen für die Verwendung von Referenzelektroden
Ideale nichtpolarisierte Elektrode
Eine ideale nicht polarisierte Elektrode dient als Eckpfeiler bei elektrochemischen Messungen, da sie einen stabilen und zuverlässigen Bezugspunkt bietet.Dieser Elektrodentyp zeichnet sich durch seine hervorragende Reversibilität aus, die gewährleistet, dass das Elektrodenpotenzial unabhängig von der Richtung des Stromflusses konstant bleibt.Ein stabiles Potenzial ist von entscheidender Bedeutung, da es Schwankungen und Fehler bei den Messungen minimiert und so die Genauigkeit und Zuverlässigkeit der gewonnenen Daten erhöht.
Darüber hinaus ist die Reproduzierbarkeit des Potenzials einer idealen nicht polarisierten Elektrode von größter Bedeutung.Das bedeutet, dass die Elektrode unter identischen Bedingungen stets das gleiche Potenzial erzeugen sollte, um Diskrepanzen bei wiederholten Experimenten auszuschließen.Eine solche Reproduzierbarkeit ist für die wissenschaftliche Strenge und die zuverlässige Vergleichbarkeit und Reproduzierbarkeit von Versuchsergebnissen unerlässlich.
Zur Veranschaulichung dieser Eigenschaften werden in der folgenden Tabelle die Merkmale idealer und nicht idealer Bezugselektroden verglichen:
| Charakteristisch | Ideale Bezugselektrode | Nicht-ideale Referenzelektrode |
|---|---|---|
| Elektrode Umkehrbarkeit | Hoch | Niedrig |
| Potenzielle Stabilität | Hoch | Variabel |
| Potenzial Reproduzierbarkeit | Hoch | Niedrig |
Zusammenfassend lässt sich sagen, dass eine ideale nicht polarisierte Elektrode eine hohe Reversibilität der Elektrode, ein stabiles Potenzial und eine ausgezeichnete Reproduzierbarkeit des Potenzials aufweisen muss, um effektiv als Referenz in elektrochemischen Studien zu dienen.
Temperaturkoeffizient und Wartung
Der Temperaturkoeffizient einer Referenzelektrode ist ein entscheidender Parameter, der ihre Leistung und Zuverlässigkeit beeinflusst.Im Idealfall sollte die Elektrode einen minimalen Temperaturkoeffizienten aufweisen, um sicherzustellen, dass ihr Potenzial unter verschiedenen Umgebungsbedingungen stabil bleibt.Diese Stabilität ist entscheidend für genaue Messungen bei elektrochemischen Experimenten, bei denen schon geringe Schwankungen des Potenzials zu erheblichen Fehlern führen können.
Neben einem geringen Temperaturkoeffizienten muss die Elektrode auch in Bezug auf Herstellung, Betrieb und Wartung benutzerfreundlich sein.Die einfache Herstellung gewährleistet gleichbleibende Qualität und Verfügbarkeit, während die unkomplizierte Verwendung den Versuchsaufbau vereinfacht und die Wahrscheinlichkeit von Bedienungsfehlern verringert.Der Wartungsaufwand sollte minimal sein, so dass eine langfristige Nutzung ohne häufige Kalibrierung oder Austausch möglich ist.
| Aspekt | Ideale Merkmale | Bedeutung |
|---|---|---|
| Temperaturkoeffizient | Klein | Gewährleistet ein stabiles Potenzial bei unterschiedlichen Temperaturen |
| Fabrikation | Einfach zu produzieren | Gewährleistet gleichbleibende Qualität und Verfügbarkeit |
| Nutzung | Einfach und intuitiv | Vereinfacht den Versuchsaufbau und reduziert Fehler |
| Wartung | Minimale | Ermöglicht eine langfristige Verwendung ohne häufige Eingriffe |
Durch die Berücksichtigung dieser Aspekte können Forscher Referenzelektroden auswählen und pflegen, die zuverlässige und genaue Daten liefern und so zum Erfolg ihrer elektrochemischen Studien beitragen.
Einsatzbedingungen für verschiedene Referenzelektroden
Klassifizierung anhand des pH-Werts
Bei der Auswahl einer Referenzelektrode für elektrochemische Experimente ist der pH-Wert des Elektrolyten ein entscheidender Faktor.Verschiedene Bezugselektroden sind speziell dafür ausgelegt, unter verschiedenen pH-Bedingungen optimal zu funktionieren und genaue und stabile Messungen zu gewährleisten.
Saure Bedingungen
Für Umgebungen mit niedrigem pH-Wert, Kalomel-Elektroden werden in der Regel verwendet.Diese Elektroden sind in sauren Umgebungen aufgrund ihrer Stabilität und der Tatsache, dass sie nicht mit sauren Lösungen reagieren, zuverlässig.Die Kalomel-Elektrode besteht aus Quecksilber in Kontakt mit einer Paste aus Quecksilber(I)-chlorid (Kalomel) und einer Kaliumchloridlösung, die ein stabiles Potenzial liefert.

Neutrale Bedingungen
In neutralen pH-Umgebungen, Silberchlorid-Elektroden sind die bevorzugte Wahl.Diese Art von Elektrode besteht aus einem mit Silberchlorid beschichteten Silberdraht, der in eine Kaliumchlorid- oder Natriumchloridlösung getaucht wird.Die Silberchlorid-Elektrode bietet eine ausgezeichnete Stabilität und einen niedrigen Temperaturkoeffizienten, wodurch sie sich für eine Vielzahl von Anwendungen eignet.
Alkalische Bedingungen
Für Umgebungen mit hohem pH-Wert, Quecksilber-Quecksilberoxid-Elektroden werden verwendet.Diese Elektroden bestehen aus Quecksilber in Kontakt mit einer Paste aus Quecksilberoxid und Kaliumhydroxidlösung.Die Quecksilber-Quecksilberoxid-Elektrode ist unter alkalischen Bedingungen stabil und liefert ein gleichmäßiges Potenzial, was für genaue Messungen in solchen Umgebungen entscheidend ist.
| Elektroden-Typ | Optimaler pH-Bereich | Bestandteile |
|---|---|---|
| Kalomel-Elektrode | sauer (niedriger pH-Wert) | Quecksilber, Quecksilber(I)-chloridpaste, Kaliumchloridlösung |
| Silberchlorid-Elektrode | Neutral (mittlerer pH-Wert) | Silberdraht, beschichtet mit Silberchlorid, Kaliumchlorid oder Natriumchloridlösung |
| Quecksilber-Quecksilber-Oxid-Elektrode | Alkalisch (hoher pH-Wert) | Quecksilber, Quecksilberoxidpaste, Kaliumhydroxidlösung |
Die Kenntnis der spezifischen pH-Anforderungen für jede Art von Referenzelektrode stellt sicher, dass die am besten geeignete Elektrode gewählt wird, wodurch die Genauigkeit und Zuverlässigkeit der elektrochemischen Messungen verbessert wird.
Sonderfälle und organische Elektrolyte
In speziellen Fällen, z. B. bei Schwefelsäure- oder Sulfatlösungen, werden Quecksilber-Quecksilbersulfat-Elektroden eingesetzt, da sie mit diesen rauen Umgebungen kompatibel sind.Diese Elektroden sind besonders effektiv bei der Aufrechterhaltung stabiler Potenziale und gewährleisten genaue Messungen unter solch aggressiven Bedingungen.
Im Bereich der Batterietechnologie sind Cadmiumhydroxid-Elektroden weit verbreitet.Diese Elektroden werden aufgrund ihrer Fähigkeit ausgewählt, den zyklischen Anforderungen des Batteriebetriebs standzuhalten und über längere Zeiträume eine zuverlässige Leistung zu erbringen.
Für Anwendungen mit organischen Elektrolyten sind Silber- und Ferrocen-Elektroden oft die bevorzugte Wahl.Silberelektroden werden wegen ihrer Stabilität und geringen Reaktivität mit organischen Verbindungen geschätzt, während Ferrocen-Elektroden einzigartige Vorteile in Bezug auf ihre Redox-Eigenschaften und ihre Kompatibilität mit organischen Medien bieten.
| Elektrolyt-Typ | Bevorzugte Elektrode | Wichtige Vorteile |
|---|---|---|
| Schwefelsäure-Lösungen | Quecksilber Quecksilbersulfat | Kompatibilität mit aggressiven Umgebungen, stabiles Potenzial |
| Batterie-Industrie | Kadmiumhydroxid | Ausdauer im zyklischen Batteriebetrieb, zuverlässige Leistung |
| Organische Elektrolyte | Silber und Ferrocen | Stabilität mit organischen Verbindungen, einzigartige Redox-Eigenschaften |
Diese Tabelle fasst die bevorzugten Elektroden für verschiedene Elektrolyttypen zusammen und hebt ihre wichtigsten Vorteile für verschiedene Anwendungen hervor.
Warum unterschiedliche Referenzelektroden für unterschiedliche Bedingungen gelten
Elektrodenreaktion und Nernst-Gleichung
Verschiedene Elektroden werden auf der Grundlage ihrer einzigartigen Elektrodenreaktionen und der sich daraus ergebenden Standard-Gleichgewichtselektrodenpotentiale, die mit Hilfe der Nernst-Gleichung sorgfältig berechnet werden, auf bestimmte Bedingungen zugeschnitten.Diese Gleichung, benannt nach dem deutschen Chemiker Walther Nernst, ist in der Elektrochemie von grundlegender Bedeutung, da sie das Reduktionspotenzial einer elektrochemischen Reaktion mit dem Standardelektrodenpotenzial und den Aktivitäten der reagierenden Spezies in Beziehung setzt.
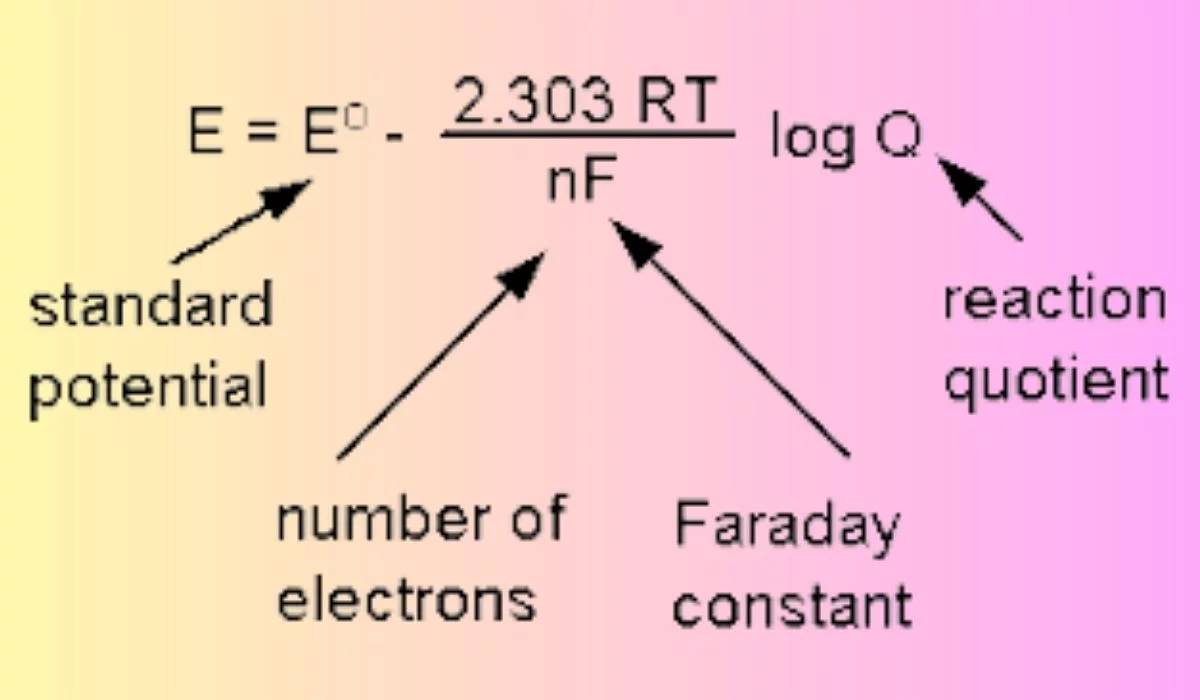
So wird beispielsweise das Standard-Gleichgewichtselektrodenpotenzial einer Silberchloridelektrode, die häufig in neutralen Umgebungen verwendet wird, von der Konzentration der Chloridionen und dem Partialdruck des Wasserstoffgases beeinflusst.Im Gegensatz dazu arbeitet eine Kalomelelektrode, die in sauren Umgebungen bevorzugt wird, nach anderen thermodynamischen Prinzipien, die Stabilität und Genauigkeit in der vorgesehenen Umgebung gewährleisten.
| Elektrodentyp | Geeignete Bedingungen | Schlüsselreaktion | Standard-Gleichgewichtspotential (V) |
|---|---|---|---|
| Silberchlorid | Neutral | AgCl + e- → Ag + Cl- | 0.2223 |
| Kalomel | Säuerlich | Hg₂Cl₂ + 2e- → 2Hg + 2Cl- | 0.2682 |
| Quecksilber-Quecksilber-Oxid | Alkalisch | HgO + H₂O + 2e- → Hg + 2OH- | 0.0977 |
Die Auswahl einer geeigneten Elektrode ist entscheidend, da sie sich direkt auf die Genauigkeit und Zuverlässigkeit elektrochemischer Messungen auswirkt.Die Eignung jeder Elektrode wird durch ihre Fähigkeit bestimmt, ein stabiles Potenzial unter wechselnden Bedingungen aufrechtzuerhalten, um sicherzustellen, dass die Nernst-Gleichung das Verhalten der Elektrode genau vorhersagt.Diese Präzision ist für Anwendungen von der Umweltüberwachung bis hin zur Batterietechnologie von entscheidender Bedeutung, bei denen schon geringe Abweichungen zu erheblichen Fehlern führen können.
Zusammenfassend lässt sich sagen, dass die Nernst-Gleichung nicht nur die Beziehung zwischen Elektrodenpotenzial und Reaktionsbedingungen quantifiziert, sondern auch die Bedeutung der Auswahl der richtigen Elektrode für bestimmte Anwendungen unterstreicht.Dadurch wird sichergestellt, dass elektrochemische Experimente präzise und reproduzierbare Ergebnisse liefern, die mit den allgemeinen Zielen der wissenschaftlichen Forschung und der industriellen Praxis übereinstimmen.
Stabilität und Nachteile
Die Silberchlorid-Elektrode ist ein gutes Beispiel dafür, wie sich bestimmte Bedingungen auf die Stabilität und Genauigkeit von Referenzelektroden auswirken können.Unter alkalischen Bedingungen kann ein längerer Gebrauch dieser Elektrode zur Bildung von Silberoxid führen.Diese Reaktion beeinträchtigt nicht nur die Stabilität der Elektrode, sondern auch ihre Genauigkeit, wodurch die Zuverlässigkeit der Messungen beeinträchtigt wird.
In alkalischen Umgebungen lässt sich die chemische Reaktion wie folgt zusammenfassen:
- Silberchlorid (AgCl) + Hydroxid (OH-) → Silberoxid (Ag₂O) + Chlorid (Cl-)
Durch diese Umwandlung ändert sich das Potenzial der Elektrode erheblich, was sie weniger vorhersehbar und fehleranfälliger macht.Die Instabilität, die durch die Bildung von Silberoxid entsteht, erfordert eine sorgfältige Abwägung bei der Auswahl und Verwendung von Referenzelektroden unter solchen Bedingungen.
Um diese Nachteile abzumildern, wird häufig der Einsatz eines Doppelsalzbrückensystems empfohlen.Diese Methode trägt dazu bei, die Stabilität der Silberchloridelektrode unter alkalischen Bedingungen aufrechtzuerhalten und sorgt für genauere und zuverlässigere Messwerte.
Abschwächung von Nachteilen durch Salzbrücken
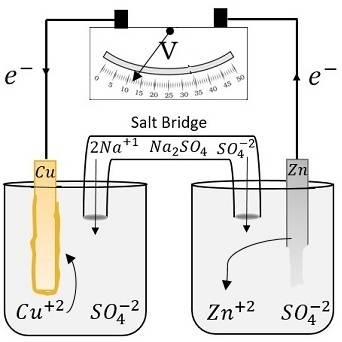
Unter alkalischen Bedingungen kann es bei Silberchloridelektroden zu Stabilitätsproblemen kommen, da sich im Laufe der Zeit Silberoxid bildet, das die Genauigkeit und Zuverlässigkeit der Messungen beeinträchtigt.Um diesen Nachteilen entgegenzuwirken, ist der Einsatz eines doppelten Salzbrückensystems eine wirksame Strategie.
Ein Doppelsalzbrückensystem beinhaltet die Verwendung von zwei separaten Salzbrücken, die jeweils mit einem geeigneten Elektrolyten gefüllt sind.Dieser Aufbau trägt dazu bei, die Referenzelektrode von der Prüflösung zu isolieren, wodurch das Risiko einer Kontamination verringert und die Wechselwirkung, die zur Bildung von Silberoxid führen könnte, minimiert wird.Durch die Schaffung einer Pufferzone sorgt das Doppelsalzbrückensystem dafür, dass die Referenzelektrode auch in schwierigen alkalischen Umgebungen stabil bleibt.
Diese Methode bewahrt nicht nur die Integrität der Silberchloridelektrode, sondern verbessert auch die Gesamtgenauigkeit der elektrochemischen Messungen.Die doppelte Isolierung durch die Salzbrücken wirkt wie eine Schutzbarriere und ermöglicht eine konsistentere und zuverlässigere Datenerfassung unter alkalischen Bedingungen.
Ähnliche Produkte
- Referenzelektrode Kalomel Silberchlorid Quecksilbersulfat für Laborzwecke
- Kupfersulfat-Referenzelektrode für Laboranwendungen
- Metall-Scheibenelektrode Elektrochemische Elektrode
- Graphit-Scheiben-Stab- und Plattenelektrode Elektrochemische Graphitelektrode
- Elektrochemische Elektrode aus Glaskohlenstoff
Ähnliche Artikel
- Verwendung und Pflege von Referenzelektroden
- Ein Leitfaden für Anfänger zum Verständnis von Referenzelektroden in der Elektrochemie
- Umfassender Leitfaden für Referenzelektroden: Typen, Anwendungen und Auswahlkriterien
- Referenzelektroden: Kalomel, Silberchlorid und Quecksilbersulfat - ein umfassender Leitfaden
- Ein umfassender Leitfaden zu Referenzelektroden



















