Der grundlegende Unterschied liegt nicht in der Substanz, sondern in der Struktur. Graphen ist kein anderes Material als Kohlenstoff; es ist eine spezifische, zweidimensionale Form des Elements Kohlenstoff. Während Kohlenstoff das Basiselement ist, ist Graphen eine einzelne, eine Atomlage dicke Schicht von Kohlenstoffatomen, die in einem präzisen Wabengitter angeordnet sind, und diese einzigartige Anordnung ist die Quelle all seiner außergewöhnlichen Eigenschaften.
Die wesentliche Unterscheidung, die man sich merken sollte, ist, dass "Kohlenstoff" das Element ist – der Baustein – während "Graphen" eine spezifische, hochgeordnete Struktur ist, die ausschließlich aus diesen Bausteinen besteht. Stellen Sie es sich vor wie Diamant und Graphit: Beide sind reiner Kohlenstoff, aber ihre unterschiedlichen Atomanordnungen verleihen ihnen völlig unterschiedliche Eigenschaften.

Vom Element zum Allotrop: Die Grundlage des Kohlenstoffs
Um die Rolle von Graphen zu verstehen, müssen wir zunächst die Vielseitigkeit seines Ausgangselements, des Kohlenstoffs, begreifen. Dieser Kontext ist unerlässlich, um zu würdigen, warum eine einfache strukturelle Veränderung ein revolutionäres Material schaffen kann.
Kohlenstoff: Der universelle Baustein
Kohlenstoff ist ein Element (Ordnungszahl 6), das im Periodensystem zu finden ist. Sein prägendes Merkmal ist seine Fähigkeit, starke kovalente Bindungen mit sich selbst und vielen anderen Elementen einzugehen, wodurch eine Vielzahl von Verbindungen entsteht.
In seiner elementaren Form kann Kohlenstoff in verschiedenen strukturellen Konfigurationen existieren.
Das Konzept der Allotrope
Diese verschiedenen strukturellen Formen eines einzelnen Elements werden Allotrope genannt. Die Atome sind identisch, aber ihre Anordnung im Raum ist unterschiedlich, was zu dramatisch unterschiedlichen physikalischen und chemischen Eigenschaften führt.
Das klassische Beispiel ist die Beziehung zwischen weichem, grauem Graphit, der in Bleistiften verwendet wird, und hartem, transparentem Diamant, der in Schmuck verwendet wird. Beide sind reiner Kohlenstoff, aber ihre Eigenschaften weichen aufgrund ihrer Atomstruktur vollständig voneinander ab.
Häufige Kohlenstoff-Allotrope
Graphen ist nur eines von mehreren wichtigen Kohlenstoff-Allotropen. Die wichtigsten sind:
- Diamant: Kohlenstoffatome sind in einem starren, dreidimensionalen tetraedrischen Gitter angeordnet. Dies macht ihn unglaublich hart.
- Graphit: Kohlenstoffatome sind in Schichten eines hexagonalen Gitters angeordnet, die übereinander gestapelt sind. Diese Schichten können leicht gleiten, was Graphit weich macht.
- Graphen: Eine einzelne, isolierte Schicht des hexagonalen Gitters, aus dem Graphit besteht.
- Amorpher Kohlenstoff: Eine Form, wie Ruß oder Holzkohle, bei der Kohlenstoffatome keine langreichweitige kristalline Ordnung aufweisen.
Was macht Graphen zu einer einzigartigen Form von Kohlenstoff?
Graphens Ruhm rührt daher, dass es der reinste Ausdruck des zweidimensionalen Potenzials von Kohlenstoff ist. Es ist die grundlegende Struktur für andere Allotrope.
Ein echtes zweidimensionales Material
Das prägende Merkmal von Graphen ist, dass es eine einzelne Atomlage ist. Mit nur einem Atom Dicke ist es das dünnste jemals geschaffene Material, eine echte 2D-Ebene von Atomen.
Das Wabengitter
Die Kohlenstoffatome in Graphen sind durch sp²-Bindungen verbunden und bilden ein perfekt wiederholendes hexagonales Muster, ähnlich einer Honigwabe oder einem Maschendrahtzaun. Diese flache, fest gebundene Struktur ist die Quelle seiner bemerkenswerten Stabilität und Stärke.
Das Ausgangsmaterial für andere Materialien
Das Verständnis von Graphen verdeutlicht seine Beziehung zu anderen Kohlenstoffformen. Man kann Graphit einfach als einen Stapel unzähliger Graphenschichten betrachten. Darüber hinaus kann man eine Graphenschicht konzeptionell zu einem Rohr rollen, um ein Kohlenstoffnanoröhrchen zu bilden, oder sie zu einer Kugel wickeln, um ein Fulleren (Buckyball) zu bilden.
Abwägungen und praktische Realitäten verstehen
Obwohl die Eigenschaften von Graphen außergewöhnlich sind, wird seine praktische Anwendung durch erhebliche Herausforderungen in der Realität eingeschränkt. Die Anerkennung dieser Einschränkungen ist der Schlüssel zu einem objektiven Verständnis.
Die Herausforderung der Massenproduktion
Die Herstellung großer, defektfreier Schichten von reinem Graphen ist extrem schwierig und teuer. Die berühmte "Scotch-Tape-Methode", die zu seiner Entdeckung verwendet wurde (Schichten von Graphit abziehen), ist für den industriellen Einsatz nicht skalierbar.
"Graphen" vs. Graphenderivate
Viele Produkte, die als "Graphen" vermarktet werden, verwenden tatsächlich verwandte Materialien wie Graphenoxid (GO) oder reduziertes Graphenoxid (rGO). Diese sind einfacher und billiger in großen Mengen herzustellen, haben aber andere und oft schlechtere elektrische und mechanische Eigenschaften im Vergleich zu reinem Graphen.
Keine Universallösung
Graphen ist ein Spezialmaterial. Obwohl es stärker als Stahl und leitfähiger als Kupfer ist, bedeuten seine Kosten und Integrationsschwierigkeiten, dass traditionelle Materialien für die überwiegende Mehrheit der Anwendungen praktischer und kostengünstiger bleiben.
Wie man über Kohlenstoffmaterialien denkt
Ihre Perspektive auf die Beziehung zwischen Kohlenstoff und Graphen hängt von Ihrem Ziel ab. Nutzen Sie diese Punkte, um Ihr Denken zu strukturieren.
- Wenn Ihr Hauptaugenmerk auf der Grundlagenchemie liegt: Denken Sie daran, dass Graphen ein Allotrop des Elements Kohlenstoff ist, definiert durch seine einzigartige 2D-Wabenstruktur.
- Wenn Ihr Hauptaugenmerk auf der Materialwissenschaft liegt: Konzentrieren Sie sich darauf, wie Graphens
sp²-gebundenes Gitter zu außergewöhnlichen Eigenschaften – Stärke, Leitfähigkeit und Leichtigkeit – führt, die sich grundlegend von 3D-Allotropen wie Diamant unterscheiden. - Wenn Ihr Hauptaugenmerk auf kommerziellen Produkten liegt: Seien Sie kritisch gegenüber Marketingaussagen und verstehen Sie, dass das verwendete "Graphen" oft ein Derivat ist, wobei die Herausforderung darin besteht, eine kostengünstige Produktion in großem Maßstab zu erreichen.
Letztendlich ist das Erkennen des Unterschieds zwischen Kohlenstoff als Element und Graphen als Struktur der Schlüssel zum Verständnis einer neuen Klasse von Materialien, die auf atomarer Ebene entwickelt wurden.
Zusammenfassungstabelle:
| Merkmal | Kohlenstoff (Element) | Graphen (Allotrop) |
|---|---|---|
| Definition | Ein chemisches Element (C) | Eine einzelne Schicht von Kohlenstoffatomen in einem 2D-Wabengitter |
| Dimensionalität | N/A (Elementarer Baustein) | Zweidimensional (2D) |
| Wichtige Allotrope | Diamant, Graphit, Amorpher Kohlenstoff | Die grundlegende Struktur für Graphit, Kohlenstoffnanoröhrchen |
| Primärer Unterschied | Der universelle Baustein | Eine spezifische, hochgeordnete Struktur aus Kohlenstoffatomen |
Bereit, fortschrittliche Materialien in Ihrer Forschung zu nutzen?
Das Verständnis der Nuancen von Materialien wie Graphen ist der Schlüssel zur Innovation. Bei KINTEK sind wir darauf spezialisiert, Ihnen die hochwertige Laborausrüstung und Verbrauchsmaterialien zu liefern, die Sie benötigen, um die Grenzen der Materialwissenschaft zu erweitern. Egal, ob Sie mit Kohlenstoff-Allotropen oder anderen fortschrittlichen Materialien arbeiten, unsere Produkte unterstützen Präzision, Zuverlässigkeit und Entdeckung.
Lassen Sie KINTEK Ihr Partner in der Forschung sein. Kontaktieren Sie noch heute unsere Experten, um die perfekten Lösungen für die einzigartigen Herausforderungen Ihres Labors zu finden.
Visuelle Anleitung
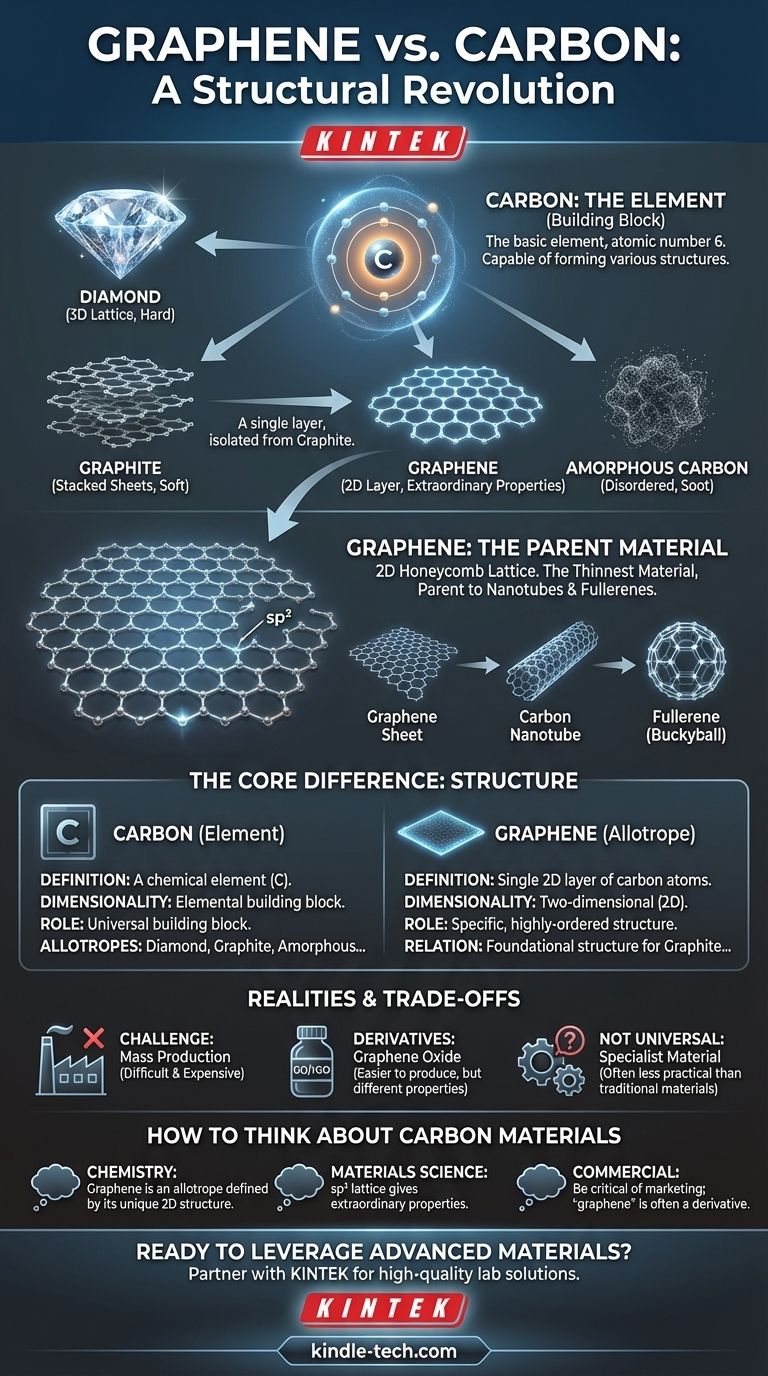
Ähnliche Produkte
- Graphit-Vakuumofen Hochwärmeleitfähige Folien-Graphitierungsöfen
- Graphit-Scheiben-Stab- und Plattenelektrode Elektrochemische Graphitelektrode
- Graphitierungs-Vakuumofen für ultrahohe Temperaturen
- Vertikaler Hochtemperatur-Graphit-Vakuum-Graphitierungs-Ofen
- Hochreine reine Graphittiegel für die Verdampfung
Andere fragen auch
- Was ist der Temperaturbereich eines Graphitofens? Bis zu 3000°C für die Verarbeitung fortschrittlicher Materialien.
- Wie hoch ist die Temperatur eines Graphitofens? Erreichen Sie extreme Hitze bis zu 3000 °C
- Welches Gas wird im Graphitofen verwendet? Maximieren Sie die Genauigkeit mit dem richtigen Inertgas
- Was sind die Vor- und Nachteile eines Graphitofens? Entfesseln Sie extreme Hitzleistung
- Was sind die Nachteile von Graphitöfen? Wichtigste Einschränkungen und Betriebskosten










