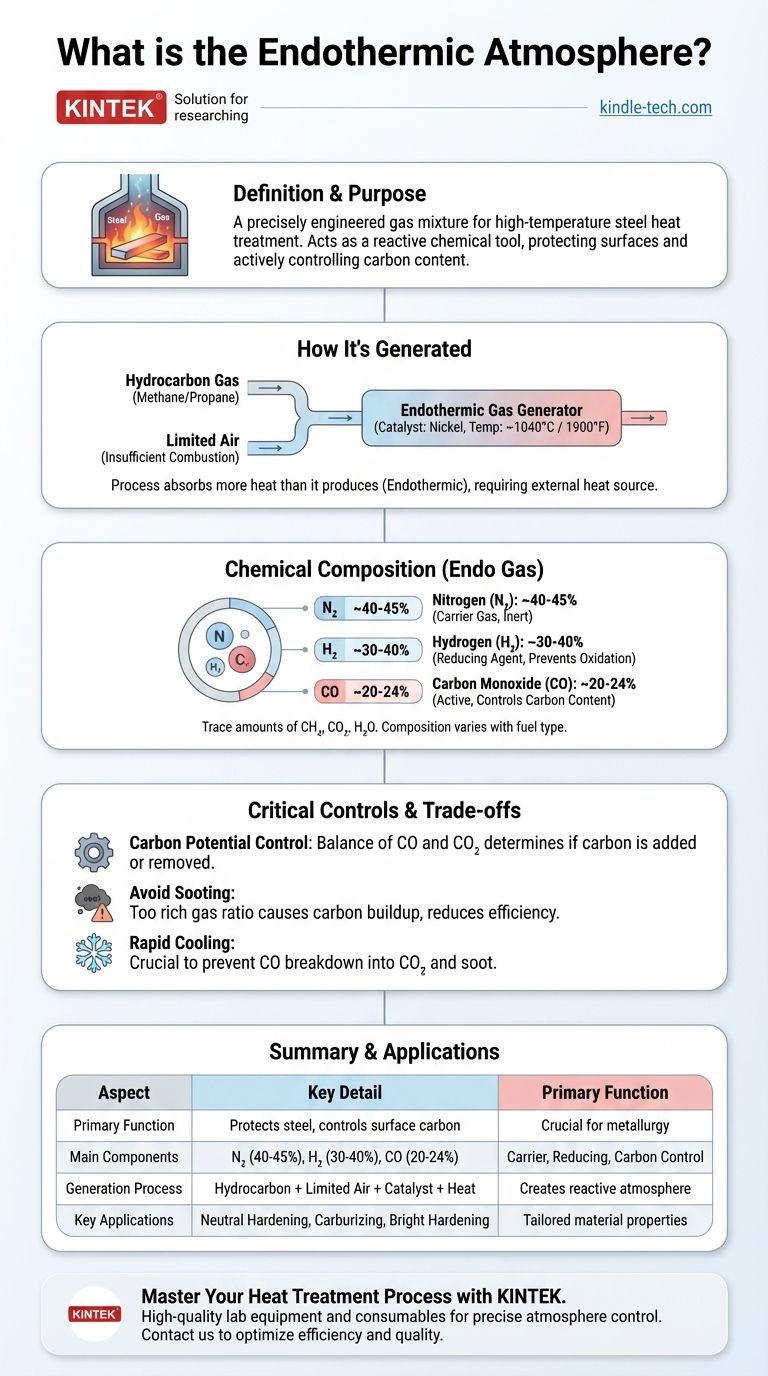
In der Welt der Metallurgie ist eine endotherme Atmosphäre ein präzise konstruiertes Gasgemisch, das zum Schutz und zur Kontrolle von Stahloberflächen während der Hochtemperatur-Wärmebehandlung verwendet wird. Sie wird erzeugt, indem ein Kohlenwasserstoffgas (wie Methan oder Propan) bei hohen Temperaturen mit einer begrenzten Menge Luft über einem Katalysator umgesetzt wird. Das resultierende Gas ist reich an Kohlenmonoxid und Wasserstoff, was es chemisch reaktiv und ideal für die Kontrolle des Kohlenstoffgehalts von Stahl macht.
Eine endotherme Atmosphäre ist nicht nur eine Schutzschicht; sie ist ein reaktives chemisches Werkzeug. Ihr Hauptzweck ist die aktive Steuerung des Kohlenstoffs auf der Oberfläche eines Stahls, um Oxidation zu verhindern und sicherzustellen, dass das Endprodukt die exakt erforderlichen Eigenschaften aufweist.

Wie eine endotherme Atmosphäre erzeugt wird
Die Erzeugung einer endothermen Atmosphäre, oft als „Endogas“ bezeichnet, ist ein kontrollierter industrieller Prozess, der in einem speziellen Gerät stattfindet.
Die Kernbestandteile: Kohlenwasserstoffgas und Luft
Der Prozess beginnt mit der Mischung eines Kohlenwasserstoffgases mit Luft. Entscheidend ist, dass die verwendete Luftmenge absichtlich für eine vollständige Verbrennung unzureichend ist – typischerweise weniger als die Hälfte dessen, was zur vollständigen Verbrennung des Brennstoffs erforderlich wäre.
Dieses präzise Verhältnis ist entscheidend. Bei der Verwendung von Methan (CH4) ist beispielsweise ein Luft-Gas-Verhältnis von etwa 2,77 zu 1 erforderlich, während Propan (C3H8) ein Verhältnis von nahe 7,16 zu 1 benötigt.
Die Reaktionskammer: Generator und Katalysator
Dieses Gas-Luft-Gemisch wird komprimiert und in einen endothermen Gasgenerator geleitet. Dort strömt es durch eine beheizte Kammer, die einen Nickel-basierten Katalysator bei einer Temperatur von etwa 1900°F (1040°C) enthält.
Die hohe Hitze und der Katalysator ermöglichen eine chemische Reaktion, die das ursprüngliche Kohlenwasserstoff-Luft-Gemisch aufspaltet.
Die chemische Umwandlung: Warum sie „endotherm“ ist
Der Begriff endotherm bedeutet, dass die Reaktion mehr Wärme absorbiert, als sie erzeugt. Die unvollständige Verbrennung erzeugt nicht genügend Energie aus sich selbst heraus, um den Prozess aufrechtzuerhalten.
Daher muss der Generator kontinuierlich externe Wärme zuführen, um die Reaktion am Laufen zu halten, was das definierende Merkmal ist, nach dem die Atmosphäre benannt ist.
Die chemische Zusammensetzung von „Endo“-Gas
Nach der Reaktion wird das Gas schnell abgekühlt. Dieser Abkühlungsschritt ist entscheidend, um die chemische Zusammensetzung „einzufrieren“ und zu verhindern, dass sich die wünschenswerten Komponenten in Ruß und Kohlendioxid zersetzen.
Die Hauptkomponenten: CO, H₂ und N₂
Eine typische endotherme Atmosphäre besteht aus drei Hauptgasen:
- Stickstoff (N₂): ~40-45%. Größtenteils inert, dient es als Trägergas.
- Wasserstoff (H₂): ~30-40%. Ein starkes Reduktionsmittel, das Oxidation (Zunder) auf der Stahloberfläche verhindert.
- Kohlenmonoxid (CO): ~20-24%. Dies ist die reaktivste Komponente, die für die Kontrolle des Kohlenstoffgehalts des Stahls verantwortlich ist.
Das Gas enthält auch Spuren von nicht umgesetztem Methan (CH₄), Kohlendioxid (CO₂) und Wasserdampf (H₂O).
Anpassung des Rezepts für verschiedene Brennstoffe
Die genaue Zusammensetzung variiert je nach verwendetem Kohlenwasserstoffbrennstoff. Eine aus Propan erzeugte Atmosphäre weist im Vergleich zu einer aus Methan erzeugten Atmosphäre eine etwas höhere Konzentration an Kohlenmonoxid und Stickstoff auf. Diese Flexibilität ermöglicht es den Bedienern, das Gas für spezifische Anwendungen anzupassen.
Verständnis der Kompromisse und kritischen Steuerungen
Obwohl sie leistungsstark ist, erfordert eine endotherme Atmosphäre eine sorgfältige Handhabung, um wirksam und sicher zu sein. Ihre reaktive Natur ist sowohl ihre größte Stärke als auch eine potenzielle Fehlerquelle.
Die Gefahr der Verrußung
Ist das Verhältnis von Kohlenwasserstoff zu Luft zu reich (zu wenig Luft), kann der Generator mit Kohlenstoffruß verstopfen. Dies verringert die Effizienz, erfordert kostspielige Reinigungen und kann Rußpartikel auf die behandelten Teile übertragen.
Kontrolle des „Kohlenstoffpotenzials“
Der wichtigste Parameter, der gesteuert werden muss, ist das Kohlenstoffpotenzial. Dies ist die Fähigkeit der Atmosphäre, den Kohlenstoffgehalt im Stahl entweder hinzuzufügen, zu entfernen oder beizubehalten. Es wird durch das Gleichgewicht von CO und CO₂ im Gas bestimmt.
Durch sorgfältige Überwachung und Anpassung der Gaszusammensetzung kann ein Wärmebehandler das Kohlenstoffpotenzial der Atmosphäre genau auf den zu bearbeitenden Stahl abstimmen.
Die Bedeutung der schnellen Abkühlung
Wie bereits erwähnt, muss das Gas nach der Erzeugung schnell abgekühlt werden. Kühlt es zu langsam ab, kann sich die Hauptreaktion umkehren: Das Kohlenmonoxid zersetzt sich in Kohlendioxid und festen Kohlenstoff (Ruß). Dies entzieht der Atmosphäre ihre nützlichste Komponente und verursacht einen Wartungsaufwand.
Die richtige Wahl für Ihr Ziel treffen
Das Verständnis der Funktion einer endothermen Atmosphäre ermöglicht es Ihnen, sie für unterschiedliche metallurgische Ergebnisse korrekt anzuwenden.
- Wenn Ihr Hauptaugenmerk auf dem Nitrieren liegt: Das Kohlenstoffpotenzial der Atmosphäre muss so gesteuert werden, dass es exakt dem Kohlenstoffgehalt des Stahls entspricht, um sowohl Aufkohlung als auch Entkohlung zu verhindern.
- Wenn Ihr Hauptaugenmerk auf dem Einsatzhärten liegt: Die Atmosphäre muss mit einem höheren Kohlenstoffpotenzial als der Stahl betrieben werden, damit Kohlenmonoxid Kohlenstoffatome auf die Oberfläche des Teils übertragen kann.
- Wenn Ihr Hauptaugenmerk auf der Prozesseffizienz liegt: Ihre oberste Priorität ist die Aufrechterhaltung des korrekten Gas-/Luft-Verhältnisses und der Generator-Temperatur, um eine gleichbleibende Gasqualität zu gewährleisten und Verrußung zu verhindern.
Letztendlich bedeutet die Beherrschung der endothermen Atmosphäre die Beherrschung der präzisen chemischen Umgebung, die moderne, hochwertige Wärmebehandlung auszeichnet.
Zusammenfassungstabelle:
| Aspekt | Wichtige Details |
|---|---|
| Hauptfunktion | Schützt Stahl und steuert aktiv den Oberflächenkohlenstoffgehalt. |
| Hauptbestandteile | 40-45% Stickstoff (N₂), 30-40% Wasserstoff (H₂), 20-24% Kohlenmonoxid (CO). |
| Erzeugungsprozess | Reaktion von Kohlenwasserstoffgas (z. B. Methan, Propan) mit begrenzter Luft über einem Katalysator bei ca. 1040°C (1900°F). |
| Wichtige Anwendungen | Nitrieren, Einsatzhärten, Blankhärten. |
| Kritische Steuerung | Kohlenstoffpotenzial (Gleichgewicht von CO/CO₂) zur Vermeidung von Entkohlung oder Verrußung. |
Beherrschen Sie Ihren Wärmebehandlungsprozess mit KINTEK
Präzise metallurgische Ergebnisse erfordern eine zuverlässige Kontrolle Ihrer Ofenatmosphäre. KINTEK ist spezialisiert auf hochwertige Laborgeräte und Verbrauchsmaterialien für die industrielle Wärmebehandlung. Unsere Lösungen helfen Ihnen, das exakte Kohlenstoffpotenzial und die Gaszusammensetzung aufrechtzuerhalten, die für perfekte Ergebnisse beim Einsatzhärten, Nitrieren und mehr erforderlich sind.
Lassen Sie sich von unseren Experten helfen, Ihre Prozesseffizienz und Produktqualität zu optimieren. Kontaktieren Sie KINTEK noch heute, um Ihre spezifischen Laboranforderungen zu besprechen.
Visuelle Anleitung
Ähnliche Produkte
- 1400℃ Kammerofen mit kontrollierter Atmosphäre und Stickstoff- und Inertgasatmosphäre
- 1700℃ Kontrollierte Atmosphäre Ofen Stickstoff Inertgas Ofen
- 1200℃ Schutzgasofen Stickstoff-Inertgas-Atmosphärenofen
- Kontrollierter Hochtemperatur-Wasserstoff-Ofen
Andere fragen auch
- Was ist die Rolle der Ofenatmosphäre? Beherrschen Sie die präzise metallurgische Kontrolle für Ihre Wärmebehandlung
- Kann man Kupfer ohne Flussmittel auf Messing löten? Ja, aber nur unter diesen spezifischen Bedingungen.
- Wie wird Sauerstoff (O2) in kontrollierten Ofenatmosphären eingesetzt? Beherrschen der Oberflächentechnik für Metalle
- Was ist die Funktion eines hochpräzisen Schutzgasofens für die Legierung 617? Simulation extremer VHTR-Bedingungen
- Welche Notwendigkeit hat ein Muffelofen mit kontrollierter Atmosphäre für die Korrosionsforschung? Nachbildung realistischer industrieller Risiken



