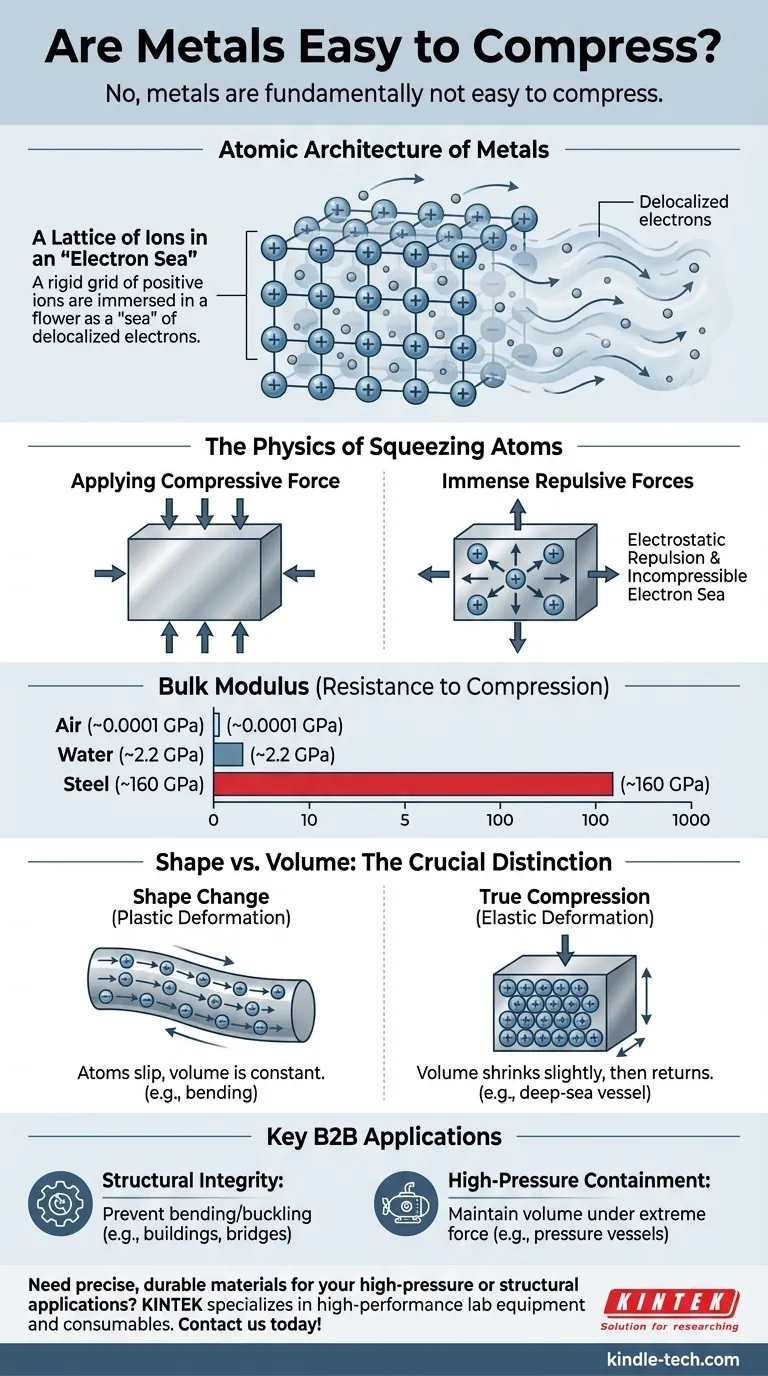
Nein, Metalle sind grundsätzlich nicht leicht komprimierbar. Sie sind tatsächlich außergewöhnlich widerstandsfähig gegen jede Kraft, die versucht, ihr Volumen zu reduzieren. Dieser hohe Kompressionswiderstand ist ein entscheidendes Merkmal, das aus ihrer einzigartigen atomaren Struktur und den starken elektrostatischen Kräften, die sie steuern, resultiert.
Obwohl wir oft sehen, wie Metalle gebogen, gedehnt oder umgeformt werden, beinhalten diese Aktionen hauptsächlich eine Änderung der Form des Materials, nicht eine signifikante Reduzierung seines Volumens. Eine echte volumetrische Kompression erfordert die Überwindung der immensen Abstoßungskräfte zwischen Atomkernen, was Metalle zu einer der inkompressibelsten Materialklassen macht, die es gibt.

Die atomare Architektur von Metallen
Um zu verstehen, warum Metalle einer Kompression widerstehen, müssen wir zuerst ihre innere Struktur betrachten. Sie unterscheidet sich von der vieler anderer Materialien.
Ein Gitter von Ionen in einem "Elektronensee"
Metalle bestehen nicht aus diskreten, neutralen Atomen. Stattdessen bilden sie eine hochgeordnete kristalline Struktur oder ein Gitter, das aus positiv geladenen Ionen besteht.
Die äußersten Elektronen jedes Atoms lösen sich ab und werden delokalisiert. Sie sind nicht mehr mit einem einzelnen Atom verbunden und können sich frei durch die gesamte Struktur bewegen.
Dies erzeugt das klassische Modell eines Metalls: ein starres Gitter positiver Ionen, eingebettet in ein mobiles "Meer" gemeinsamer Elektronen.
Der flexible "Klebstoff"
Dieses Elektronenmeer wirkt wie ein starker, aber flexibler elektrostatischer Klebstoff. Es hält die positiven Ionen zusammen, weshalb Metalle stark sind.
Die Beweglichkeit dieser Elektronen ermöglicht es den Metallatomen auch, aneinander vorbeizugleiten, ohne die Bindungen zu brechen. Dies erklärt, warum Metalle duktil (zu Drähten ziehbar) und formbar (zu Blechen hämmerbar) sind.
Die Physik des Zusammendrückens von Atomen
Wenn Sie eine Druckkraft auf ein Metall ausüben, versuchen Sie, diese stabile Atomanordnung in einen kleineren Raum zu zwingen.
Kerne zusammendrücken
Die primäre Wirkung der Kompression besteht darin, die positiv geladenen Atomkerne näher aneinander zu drücken.
Wenn der Abstand zwischen diesen Kernen abnimmt, nimmt die elektrostatische Abstoßung zwischen ihnen – die Kraft, die sie auseinanderdrückt – exponentiell zu. Diese Kraft wird bei sehr kleinen Abständen unglaublich stark.
Eine inkompressible Flüssigkeit
Gleichzeitig widersteht das "Meer" der Elektronen selbst der Kompression. So wie es unglaublich schwierig ist, eine Flüssigkeit wie Wasser zu komprimieren, widersteht diese dichte Wolke negativ geladener Elektronen stark dem Packen in ein kleineres Volumen.
Die Kombination dieser beiden Effekte erzeugt einen immensen Innendruck, der jeder externen Druckkraft entgegenwirkt.
Inkompressibilität quantifizieren: Der Kompressionsmodul
Dieser Kompressionswiderstand ist nicht nur ein qualitatives Konzept; er ist eine messbare physikalische Eigenschaft.
Was ist der Kompressionsmodul?
Der Kompressionsmodul ist das präzise Maß für den Widerstand eines Stoffes gegen gleichmäßige Kompression. Er ist definiert als das Verhältnis der Druckerhöhung zur resultierenden fraktionellen Volumenabnahme.
Ein höherer Kompressionsmodul bedeutet, dass ein Material schwerer zu komprimieren ist.
Metalle haben extrem hohe Kompressionsmoduln
Metalle wie Stahl, Titan und Wolfram haben einige der höchsten Kompressionsmoduln aller gängigen Materialien. Dies ist ein direktes Ergebnis der starken Abstoßungskräfte innerhalb ihres Atomgitters.
Zum Vergleich: Der Kompressionsmodul von Stahl beträgt etwa 160 Gigapascal (GPa). Im Gegensatz dazu beträgt der von Wasser etwa 2,2 GPa und der der Luft, die Sie atmen, etwa 0,0001 GPa. Sie bräuchten einen immensen Druck, um selbst eine winzige Volumenreduzierung bei einem Metall zu erreichen.
Die Nuancen verstehen: Form vs. Volumen
Ein häufiger Fehler ist die Verwechslung einer Formänderung mit einer Volumenänderung.
Elastische vs. plastische Verformung
Wenn Sie auf einen Metallstab drücken und ihn kürzer machen, handelt es sich typischerweise um plastische Verformung (Fließen). Die Atome gleiten aneinander vorbei und ändern die Abmessungen des Objekts. Das Gesamtvolumen des Materials bleibt jedoch fast genau gleich.
Echte Kompression, gemessen am Kompressionsmodul, ist eine elastische Verformung, bei der das Volumen unter Druck leicht schrumpft und in seinen ursprünglichen Zustand zurückkehrt, wenn der Druck nachlässt. Bei Metallen ist diese Volumenänderung winzig.
Verhalten bei Zug vs. Kompression
Während Metalle Volumenänderungen stark widerstehen, können ihr Verhalten bei Zug (Ziehen) und Kompression (Drücken) unterschiedliche Versagensmodi aufweisen.
Ein Metallstab, der auf Zug beansprucht wird, wird schließlich "einschnüren" und brechen. Derselbe Stab, der auf Kompression beansprucht wird, wird eher knicken (wenn er schlank ist) oder ausbauchen (wenn er kurz ist), lange bevor sein Volumen signifikant reduziert wird.
Die richtige Wahl für Ihr Ziel treffen
Das Verständnis dieser Eigenschaft ist für nahezu jede Ingenieur- oder Designanwendung entscheidend.
- Wenn Ihr Hauptaugenmerk auf der strukturellen Integrität liegt: Wählen Sie Metalle mit hoher Druckfließgrenze, wie Baustahl oder Aluminiumlegierungen, um dauerhaftes Biegen, Knicken oder Verkürzen unter Last zu verhindern.
- Wenn Ihr Hauptaugenmerk auf der Hochdruckeindämmung liegt: Wählen Sie Materialien mit einem sehr hohen Kompressionsmodul, wie Stahllegierungen, Nickellegierungen oder Wolfram, für Anwendungen wie Druckbehälter oder Tiefsee-Tauchboote, bei denen die Volumenstabilität unter extremen äußeren Kräften von größter Bedeutung ist.
Letztendlich ist der ausgeprägte Kompressionswiderstand eines Metalls eine direkte und starke Folge der fundamentalen Kräfte, die seine atomare Struktur bestimmen.
Zusammenfassungstabelle:
| Eigenschaft | Beschreibung | Warum es wichtig ist |
|---|---|---|
| Kompressionsmodul | Misst den Widerstand gegen gleichmäßige Kompression. | Hohe Werte (z.B. Stahl: 160 GPa) bedeuten extreme Inkompressibilität. |
| Atomare Struktur | Gitter positiver Ionen in einem "Meer" delokalisierter Elektronen. | Erzeugt starke elektrostatische Abstoßung bei Kompression. |
| Verformungsart | Volumenänderung (elastisch) vs. Formänderung (plastisch). | Echte Kompression ist minimal; Formänderungen sind häufiger. |
| Schlüsselanwendungen | Strukturelle Integrität, Hochdruckeindämmung. | Leitet die Materialauswahl für Ingenieurwesen und Design. |
Benötigen Sie präzise, langlebige Materialien für Ihre Hochdruck- oder strukturellen Anwendungen? KINTEK ist spezialisiert auf Hochleistungs-Laborgeräte und Verbrauchsmaterialien und bedient Branchen, die auf Materialintegrität unter Belastung angewiesen sind. Lassen Sie sich von unseren Experten bei der Auswahl der richtigen Lösungen für die einzigartigen Herausforderungen Ihres Labors unterstützen. Kontaktieren Sie uns noch heute, um Ihre Anforderungen zu besprechen!
Visuelle Anleitung