In der Chemieingenieurwissenschaft wird die Druckerhöhung in einem Reaktor grundlegend durch die Manipulation der Variablen des Idealen Gasgesetzes (PV=nRT) erreicht. Die gängigsten Methoden sind die Zugabe von mehr Material (Gas), die Erhöhung der Systemtemperatur oder die mechanische Reduzierung des Reaktorvolumens. Jede Methode dient einem bestimmten Zweck und hat erhebliche Auswirkungen auf die Kinetik, das Gleichgewicht und die allgemeine Sicherheit der Reaktion.
Die zentrale Herausforderung ist nicht einfach, wie man den Druck erhöht, sondern warum man es tut. Die Wahl der richtigen Methode hängt vollständig davon ab, ob Ihr Ziel darin besteht, die Reaktantenkonzentration zu erhöhen, das chemische Gleichgewicht zu verschieben oder die Phase der Materialien im Reaktor zu steuern.

Die grundlegenden Prinzipien der Druckerzeugung
Im Kern ist Druck das Ergebnis von Gasmolekülen, die mit den Wänden eines Behälters kollidieren. Um diesen Druck zu erhöhen, müssen Sie diese Kollisionen häufiger oder stärker machen. Das Ideale Gasgesetz liefert den theoretischen Rahmen dafür, wie dies geschieht.
Erhöhung der Molzahl (n): Die direkte Zufuhrmethode
Dies ist der einfachste Ansatz. Durch die Zugabe von mehr Gasmolekülen in ein festes Volumen erhöhen Sie die Anzahl der Kollisionen mit den Reaktorwänden und erhöhen dadurch den Druck.
Es besteht jedoch ein kritischer Unterschied zwischen der Zugabe eines Reaktanten und der Zugabe eines Inertgases. Die Zugabe von mehr gasförmigem Reaktanten erhöht dessen Partialdruck, was dessen Konzentration direkt erhöht und die Reaktionsgeschwindigkeit beschleunigen kann.
Umgekehrt erhöht die Zugabe eines Inertgases (wie Stickstoff oder Argon) den Gesamtsystemdruck, ändert aber nicht die Partialdrücke der Reaktanten. Diese Technik wird oft verwendet, um das Phasenverhalten zu steuern oder zur Wärmeregulierung, nicht um die Reaktionsgeschwindigkeit direkt zu beeinflussen.
Erhöhung der Temperatur (T): Die thermische Methode
Das Erhitzen eines versiegelten Reaktors erhöht die kinetische Energie der Gasmoleküle im Inneren. Diese energetisierten Moleküle bewegen sich schneller, was zu häufigeren und stärkeren Kollisionen mit den Reaktorwänden führt, was sich als Druckerhöhung manifestiert.
Diese Methode ist oft ein Nebeneffekt der Durchführung einer Reaktion bei höherer Temperatur, um deren Geschwindigkeit zu erhöhen. Die Druckerhöhung muss als Teil des Reaktordesigns antizipiert und gehandhabt werden.
Verringerung des Volumens (V): Die mechanische Methode
Bei bestimmten Reaktortypen kann der Druck durch mechanische Reduzierung des Innenvolumens erhöht werden. Man denke an einen Kolben in einem Zylinder, der ein Gas komprimiert.
Diese Methode ist bei großtechnischen kontinuierlichen Reaktoren seltener, ist aber ein primäres Prinzip bei bestimmten Laboraufbauten, Batch-Prozessen und spezifischen Typen von Kompressoren oder Motoren.
Chemische Auswirkungen höheren Drucks
Die Druckerhöhung ist ein mächtiges Werkzeug, um das Ergebnis einer chemischen Reaktion zu beeinflussen und zu steuern. Sie ist nicht nur ein physikalischer Parameter, sondern ein wichtiger Treiber des chemischen Verhaltens.
Auswirkungen auf die Reaktionsgeschwindigkeit
Bei den meisten Gasphasenreaktionen führt die Druckerhöhung durch Zugabe weiterer Reaktanten dazu, dass die Moleküle näher zusammenrücken. Diese höhere Konzentration führt zu häufigeren molekularen Kollisionen, was im Allgemeinen zu einer schnelleren Reaktionsgeschwindigkeit führt.
Auswirkungen auf das Gleichgewicht
Dies wird durch das Prinzip von Le Chatelier bestimmt. Wenn eine reversible Reaktion eine unterschiedliche Anzahl von Gasmolen auf der Reaktanten- und Produktseite aufweist, verschiebt eine Druckänderung das Gleichgewicht.
Eine Druckerhöhung begünstigt die Seite der Reaktion mit weniger Gasmolen. Das klassische Beispiel ist der Haber-Bosch-Prozess zur Ammoniaksynthese (N₂ + 3H₂ ⇌ 2NH₃), bei dem hoher Druck verwendet wird, um das Gleichgewicht zum Produkt Ammoniak zu verschieben.
Auswirkungen auf das Phasenverhalten
Druck ist auch ein kritisches Werkzeug zur Steuerung des physikalischen Zustands von Substanzen. Hoher Druck kann verhindern, dass eine Flüssigkeit selbst bei hohen Temperaturen siedet, was für viele Flüssigphasenreaktionen unerlässlich ist. Er kann auch verwendet werden, um Gase zur Trennung zu verflüssigen oder Reaktionen zu erleichtern, die an der Grenzfläche zwischen einem Gas und einer Flüssigkeit stattfinden.
Verständnis der Kompromisse und Sicherheitsrisiken
Während höherer Druck erhebliche Prozessvorteile bieten kann, birgt er auch erhebliche Kosten und Gefahren, die sorgfältig gemanagt werden müssen.
Material- und Baukosten
Hochdruckreaktoren erfordern dickere Stahlwände, fortschrittlichere Legierungen und hochspezialisierte Dichtungen und Armaturen, um die Eindämmung zu gewährleisten. Dies erhöht die anfänglichen Investitionsausgaben (CAPEX) eines Projekts dramatisch.
Energieverbrauch
Das Komprimieren von Gasen auf hohe Drücke ist ein extrem energieintensiver Prozess. Dies führt direkt zu höheren laufenden Betriebskosten (OPEX) und kann die wirtschaftliche Rentabilität eines Prozesses erheblich beeinflussen.
Kritische Sicherheitsgefahren
Die wichtigste Überlegung ist die Sicherheit. Ein Hochdrucksystem speichert eine enorme Menge an potenzieller Energie. Ein Bruch oder Versagen kann zu einer katastrophalen, explosiven Freisetzung führen.
Alle Hochdrucksysteme müssen mit mehreren Sicherheitsebenen ausgestattet sein, einschließlich Überdruckventilen, Berstscheiben sowie strengen Inspektions- und Wartungsprotokollen, um diese Risiken zu mindern.
Die richtige Wahl für Ihr Ziel treffen
Die korrekte Methode zur Druckerhöhung wird durch das spezifische Ziel Ihres chemischen Prozesses bestimmt.
- Wenn Ihr Hauptaugenmerk darauf liegt, die Reaktionsgeschwindigkeit und Ausbeute zu erhöhen: Die direkte Zugabe von mehr gasförmigem Reaktanten ist die effektivste Strategie, da sie die Partialdrücke erhöht, die die Reaktion antreiben.
- Wenn Ihr Hauptaugenmerk darauf liegt, ein chemisches Gleichgewicht zu verschieben: Die Erhöhung des Gesamtsystemdrucks, entweder durch Kompression oder Zugabe von Reaktanten, ist grundlegend für Reaktionen, bei denen die Produktseite weniger Gasmole aufweist.
- Wenn Ihr Hauptaugenmerk darauf liegt, eine flüssige Phase über ihrem normalen Siedepunkt zu halten: Die Erhöhung des Gesamtdrucks, oft mit einem Inertgas, ist der Schlüssel zur Schaffung der notwendigen Prozessbedingungen.
Letztendlich geht es bei der Steuerung des Reaktordrucks darum, die Thermodynamik und Kinetik des Systems strategisch zu manipulieren, um Ihr gewünschtes Ergebnis sicher und effizient zu erzielen.
Zusammenfassungstabelle:
| Methode | Primärer Mechanismus | Wichtige chemische Implikation |
|---|---|---|
| Erhöhung der Molzahl (n) | Zugabe von mehr Gasmolekülen | Erhöht die Reaktantenkonzentration/Reaktionsgeschwindigkeit |
| Erhöhung der Temperatur (T) | Erhöhung der molekularen kinetischen Energie | Sekundärer Effekt des Erhitzens zur Beschleunigung von Reaktionen |
| Verringerung des Volumens (V) | Mechanische Kompression des Gases | Verschiebt das Gleichgewicht zu weniger Gasmolen |
Benötigen Sie eine präzise Druckregelung für Ihre Laborprozesse? KINTEK ist spezialisiert auf hochwertige Laborgeräte und Verbrauchsmaterialien, einschließlich robuster Reaktorsysteme, die für ein sicheres und effizientes Druckmanagement ausgelegt sind. Unsere Lösungen helfen Ihnen, optimale Reaktionskinetik, Ausbeute und Sicherheit zu erreichen. Kontaktieren Sie KINTEK noch heute, um zu besprechen, wie wir die spezifischen Anforderungen Ihres Labors unterstützen können.
Visuelle Anleitung
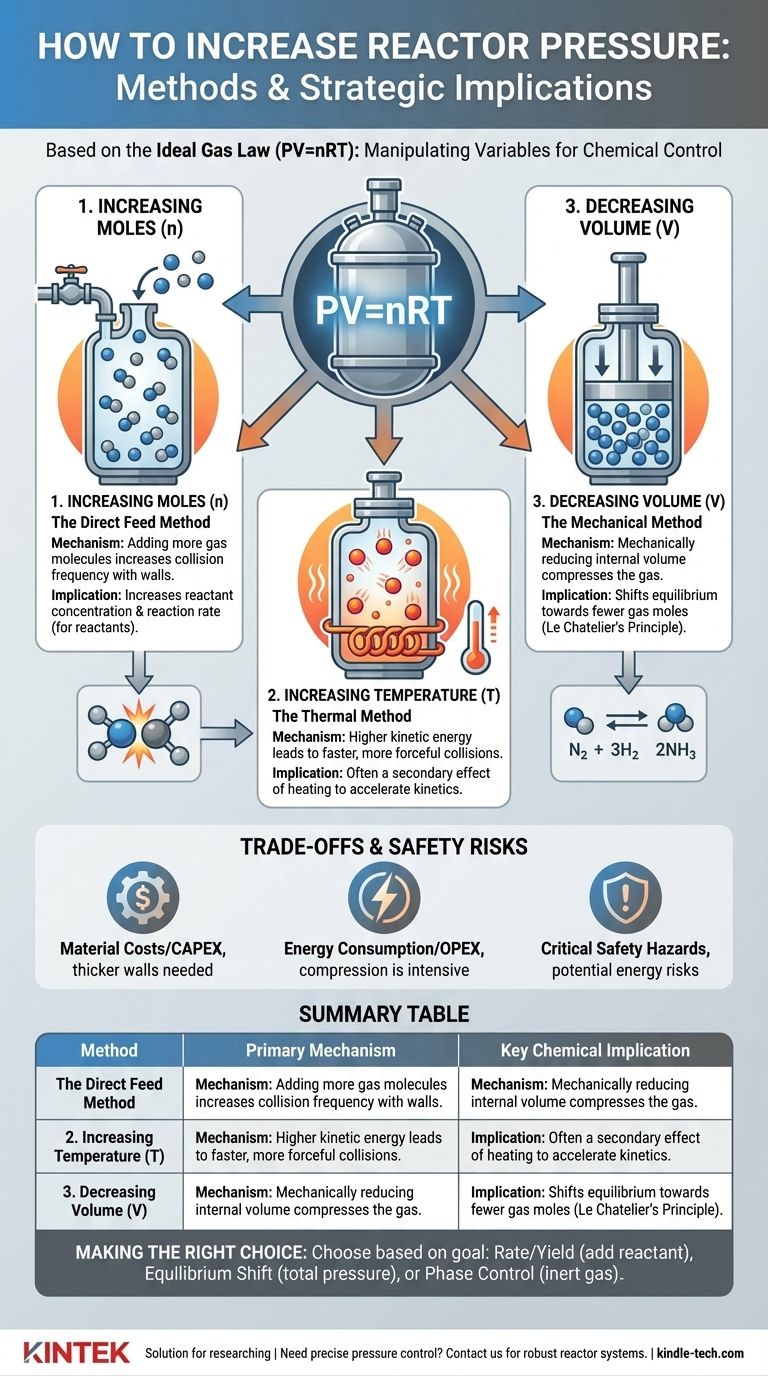
Ähnliche Produkte
- Anpassbare Labor-Hochtemperatur-Hochdruckreaktoren für vielfältige wissenschaftliche Anwendungen
- Anpassbare Hochdruckreaktoren für fortschrittliche wissenschaftliche und industrielle Anwendungen
- Edelstahl-Hochdruck-Autoklav-Reaktor Labor-Druckreaktor
- Mini-Edelstahl-Hochdruck-Autoklavenreaktor für den Laboreinsatz
- Hochdruck-Laborautoklav-Reaktor für Hydrothermalsynthese
Andere fragen auch
- Welche experimentellen Bedingungen bietet ein HTHP-Reaktor für Coiled Tubing? Optimierung der Korrosionssimulation unter Tage
- Welche Rolle spielen Hochtemperatur-Hochdruck (HTHP)-Reaktoren bei der Simulation der Korrosion von Öl- und Gasbohrungen?
- Wie steuern Sie hohen Druck in einem Reaktor? Ein Leitfaden für sicheren & stabilen Betrieb
- Welche Rolle spielt ein Hochtemperatur-Hochdruckreaktor bei der Synthese von CoFe2O4/Fe? Präzision bei Kern-Schale-Strukturen freischalten
- Wie wirkt sich der anfängliche Sauerstoffdruck auf die Nassoxidation von pharmazeutischen Klärschlämmen aus? Beherrschen Sie Ihre Oxidationstiefe



















