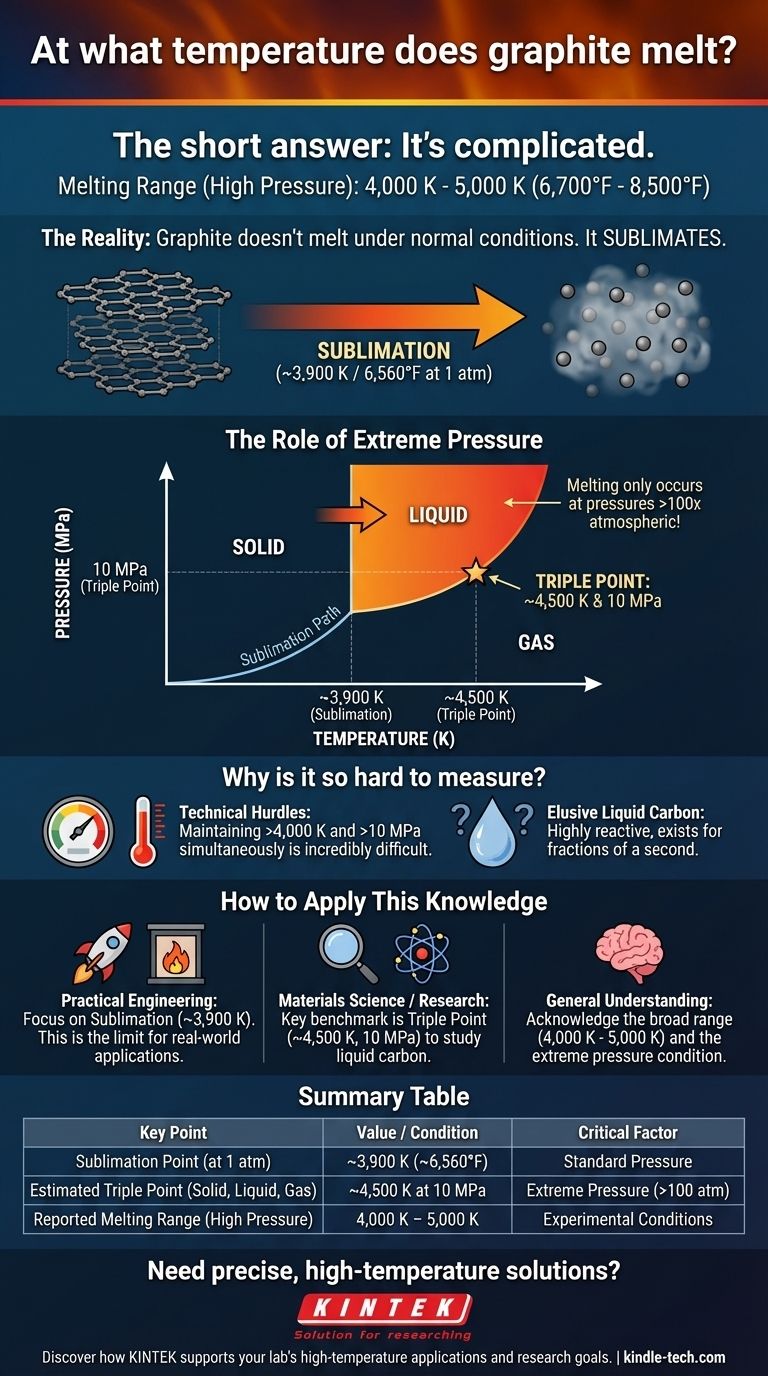
Der Schmelzpunkt von Graphit ist kein einzelner, fester Wert. Jahrzehntelange Experimente haben eine breite Palette von Ergebnissen geliefert, die die Schmelztemperatur im Allgemeinen zwischen 4.000 K und 5.000 K (etwa 6.700 °F bis 8.500 °F) ansiedeln. Diese Ungewissheit besteht, weil Graphit unter normalen Bedingungen überhaupt nicht schmilzt – er sublimiert direkt vom festen in den gasförmigen Zustand.
Das Kernproblem ist der Druck. Um Graphit zur Verflüssigung zu zwingen, muss extremer Druck (etwa das Hundertfache des normalen atmosphärischen Drucks) ausgeübt werden, während es gleichzeitig auf Tausende von Grad erhitzt wird. Die immense technische Schwierigkeit dieses Prozesses ist der Grund, warum ein einziger, definitiver Schmelzpunkt schwer fassbar bleibt.

Warum Graphit dem Schmelzen widersteht
Um die Herausforderung des Schmelzens von Graphit zu verstehen, müssen wir über die Temperatur hinausblicken und die grundlegende Rolle des Drucks berücksichtigen.
Das Problem der Sublimation
Bei atmosphärischem Standarddruck haben Materialien bei steigender Temperatur einen klaren Weg von fest zu flüssig zu gasförmig. Graphit ist anders.
Seine Atome sind durch so starke kovalente Bindungen zusammengehalten, dass sie beim Erhitzen genügend Energie gewinnen, um sich vollständig zu lösen und direkt in ein Gas überzugehen. Dieser Prozess wird als Sublimation bezeichnet. Bei Graphit geschieht dies bei etwa 3.900 K (6.560 °F).
Die Rolle des extremen Drucks
Um die Sublimation zu verhindern und Graphit in einen flüssigen Zustand zu zwingen, ist immenser Druck erforderlich. Dieses Verhältnis zwischen Temperatur, Druck und Zustand (fest, flüssig, gasförmig) wird durch das Phasendiagramm eines Materials beschrieben.
Das Schlüsselmerkmal ist der Tripelpunkt: die spezifische Kombination aus Temperatur und Druck, bei der die festen, flüssigen und gasförmigen Phasen alle im Gleichgewicht existieren können. Für Graphit wird der Tripelpunkt auf etwa 4.500 K und 10 Megapascal (MPa) geschätzt, was fast dem Hundertfachen des normalen atmosphärischen Drucks entspricht.
Nur bei Drücken über diesem Tripelpunkt kann eine eigenständige flüssige Kohlenstoffphase existieren.
Die Herausforderung der präzisen Messung
Die extremen Bedingungen, die erforderlich sind, um den Tripelpunkt von Graphit zu erreichen, sind der Hauptgrund für die widersprüchlichen experimentellen Daten.
Technische Hürden
Die genaue Aufrechterhaltung und Messung einer stabilen Temperatur von über 4.000 K bei gleichzeitiger Anwendung von über 100 Atmosphären Druck liegt an der Grenze unserer derzeitigen technologischen Möglichkeiten.
Unterschiedliche experimentelle Methoden, wie Laserheizung oder elektrische Widerstandsheizung, können leichte Abweichungen in den Bedingungen verursachen, was zu der breiten Spanne der berichteten Schmelzpunkte führt.
Die schwer fassbare Natur von flüssigem Kohlenstoff
Selbst wenn er erreicht wird, ist flüssiger Kohlenstoff eines der exotischsten und am schwierigsten zu untersuchenden Materialien überhaupt. Er ist hochreaktiv und existiert unter kontrollierten Bedingungen nur für Sekundenbruchteile, was eine definitive Analyse extrem erschwert.
Diese experimentelle Unsicherheit ist nicht neu; sie ist eine gut dokumentierte wissenschaftliche Herausforderung, die seit über 60 Jahren besteht.
Wie man dieses Wissen anwendet
Die „richtige“ Temperatur für den Phasenübergang von Graphit hängt vollständig von Ihrer Anwendung ab. Das Verständnis des Kontexts ist wichtiger als das Auswendiglernen einer einzelnen Zahl.
- Wenn Ihr Hauptaugenmerk auf der praktischen Ingenieurwissenschaft liegt (Öfen, Raketendüsen): Die Sublimationstemperatur von ~3.900 K bei Normaldruck ist der kritischste Wert. Dies ist die Temperaturgrenze für die Verwendung von Graphit in den meisten realen Hochtemperaturanwendungen.
- Wenn Ihr Hauptaugenmerk auf Materialwissenschaft oder Physikforschung liegt: Der Tripelpunkt von ~4.500 K und 10 MPa ist der Schlüsselmaßstab. Dies stellt die Mindestbedingungen dar, unter denen flüssiger Kohlenstoff erzeugt und untersucht werden kann.
- Wenn Sie eine allgemeine Schätzung für die Schmelzkurve benötigen: Erkennen Sie die breite Spanne von 4.000 K bis 5.000 K an und verstehen Sie, dass dies nur unter extremen, nicht-atmosphärischen Drücken geschieht.
Letztendlich beruht die bemerkenswerte Stabilität von Graphit bei hohen Temperaturen auf seiner Präferenz, gasförmig zu werden, anstatt zu schmelzen.
Zusammenfassungstabelle:
| Wichtiger Punkt | Wert / Bedingung |
|---|---|
| Sublimationspunkt (bei 1 atm) | ~3.900 K (~6.560°F) |
| Geschätzter Tripelpunkt (Fest, Flüssig, Gas) | ~4.500 K bei 10 MPa |
| Berichteter Schmelzbereich (Hoher Druck) | 4.000 K - 5.000 K |
| Kritischer Faktor | Extremer Druck (>100 atm) |
Benötigen Sie präzise Hochtemperaturlösungen für Ihr Labor?
Das Verhalten von Graphit unter extremen Bedingungen unterstreicht die Notwendigkeit zuverlässiger Hochleistungsausrüstung. Bei KINTEK sind wir darauf spezialisiert, robuste Laborgeräte und Verbrauchsmaterialien anzubieten, die den anspruchsvollen Anforderungen moderner Labore gerecht werden.
Ob Sie mit Hochtemperaturprozessen oder fortschrittlicher Materialwissenschaft arbeiten, unsere Produkte gewährleisten Genauigkeit, Haltbarkeit und Sicherheit.
Kontaktieren Sie uns noch heute, um herauszufinden, wie KINTEK die Hochtemperaturanwendungen und Forschungsziele Ihres Labors unterstützen kann.
Visuelle Anleitung
Ähnliche Produkte
- Graphit-Vakuumofen Hochwärmeleitfähige Folien-Graphitierungsöfen
- Graphit-Scheiben-Stab- und Plattenelektrode Elektrochemische Graphitelektrode
- Graphitierungs-Vakuumofen für ultrahohe Temperaturen
- Hochreine reine Graphittiegel für die Verdampfung
- Isostatisch gepresste Graphit-Kohlenstoffplatte
Andere fragen auch
- Was ist der Zweck eines Graphitofens? Erreichen extremer Temperaturen für fortschrittliche Materialien
- Was macht ein Graphitofen? Extreme Hitze und ultra-sensitive Analyse erreichen
- Wie hoch ist die Temperatur eines Graphitofens? Erreichen Sie extreme Hitze bis zu 3000 °C
- Was sind die Nachteile von Graphitöfen? Wichtigste Einschränkungen und Betriebskosten
- Was ist der Nachteil eines Graphittiegels? Umgang mit Reaktivitäts- und Kontaminationsrisiken












