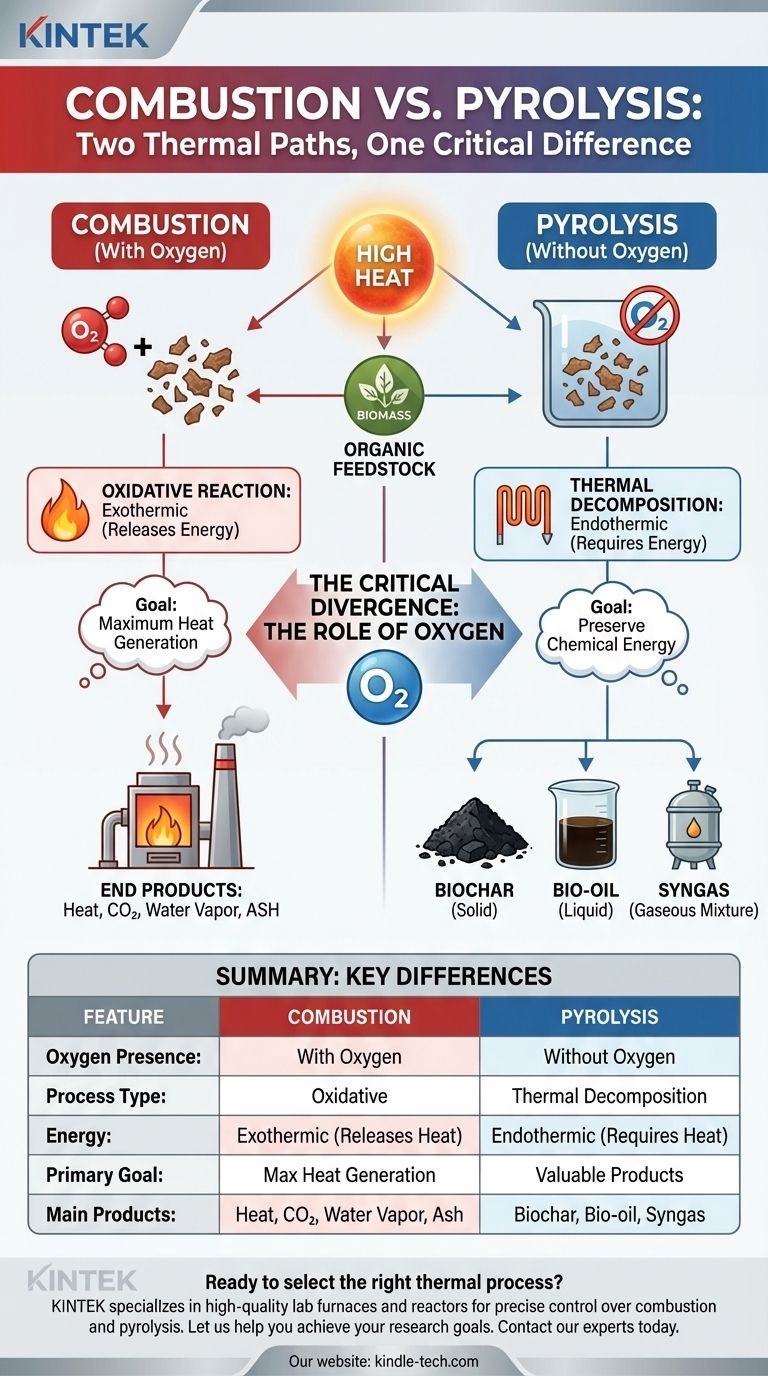
Im Kern sind sowohl Verbrennung als auch Pyrolyse thermische Zersetzungsprozesse, die hohe Hitze nutzen, um organische Materialien abzubauen. Sie stellen zwei verschiedene Wege zur Umwandlung von Materie mit Energie dar, die vom gleichen Grundprinzip ausgehen: der Anwendung von Hitze zur Einleitung einer chemischen Veränderung.
Der entscheidende Unterschied liegt nicht in der Hitze, sondern in der Luft. Die Verbrennung ist ein oxidativer Prozess, der mit Sauerstoff stattfindet, während die Pyrolyse ein nicht-oxidativer Prozess ist, der ohne Sauerstoff abläuft, was die Reaktion und ihre Endprodukte grundlegend verändert.

Die Grundlage: Was beide Prozesse gemeinsam haben
Obwohl ihre Ergebnisse sehr unterschiedlich sind, beginnen Verbrennung und Pyrolyse von einem gemeinsamen Ausgangspunkt aus. Das Verständnis dieser Grundlage ist der Schlüssel zum Erfassen ihrer Beziehung.
Hohe Hitze als treibende Kraft
Beide Prozesse beruhen auf der Anwendung hoher Temperaturen auf ein Ausgangsmaterial, typischerweise organische Materie wie Biomasse. Diese thermische Energie ist es, die die komplexen chemischen Bindungen im Material aufbricht und seine Umwandlung einleitet.
Transformation des Ausgangsmaterials
In beiden Fällen wird ein festes oder flüssiges Ausgangsmaterial in verschiedene Aggregatzustände umgewandelt. Das ursprüngliche Material wird irreversibel in einfachere Bestandteile zerlegt.
Erzeugung gasförmiger Nebenprodukte
Sowohl Verbrennung als auch Pyrolyse setzen Gase frei. Die Zusammensetzung und der Nutzen dieser Gase sind jedoch ein primärer Unterschied zwischen den beiden Methoden.
Die kritische Abweichung: Die Rolle des Sauerstoffs
Die Anwesenheit oder Abwesenheit von Sauerstoff ist die einzige Variable, die bestimmt, ob der Prozess Verbrennung oder Pyrolyse ist. Dieser Faktor bestimmt den gesamten chemischen Weg.
Verbrennung: Eine oxidative Reaktion
Die Verbrennung ist eine exotherme Reaktion, was bedeutet, dass sie Energie in Form von Wärme und Licht freisetzt. Sie ist definiert durch die schnelle Oxidation einer Brennstoffquelle in Gegenwart eines Oxidationsmittels, typischerweise Sauerstoff aus der Luft. Wir nennen dies umgangssprachlich „Brennen“.
Das Ziel der Verbrennung ist es, die gespeicherte chemische Energie des Brennstoffs so schnell wie möglich freizusetzen.
Pyrolyse: Eine thermische Reaktion ohne Sauerstoff
Die Pyrolyse ist hauptsächlich ein endothermer Prozess, was bedeutet, dass sie einen konstanten Energieeintrag zur Aufrechterhaltung der Reaktion benötigt. Indem man Material in einer sauerstofffreien Umgebung erhitzt, verhindert man, dass es verbrennt.
Anstatt freigesetzt zu werden, bleibt die chemische Energie erhalten und konzentriert sich in den entstehenden Produkten. Man kann es sich eher als „Backen“ oder „Rösten“ des Materials vorstellen, anstatt es zu verbrennen.
Vergleich der Endprodukte
Der praktischste Unterschied zwischen den beiden Prozessen liegt darin, was übrig bleibt, wenn die Reaktion abgeschlossen ist.
Verbrennung liefert Asche und Wärme
Die primären Ergebnisse der vollständigen Verbrennung sind Wärme, Kohlendioxid (CO2), Wasserdampf und ein fester Rückstand mit geringer Energie, bekannt als Asche. Das Potenzial des Brennstoffs wurde vollständig zur Erzeugung thermischer Energie aufgebraucht.
Pyrolyse liefert wertvolle, energiedichte Produkte
Die Pyrolyse zerlegt das Material in drei wertvolle Produkte:
- Biokohle: Ein stabiler, kohlenstoffreicher Feststoff.
- Bio-Öl: Eine Flüssigkeit, die zu Kraftstoffen raffiniert werden kann.
- Synthesegas: Eine Mischung aus brennbaren Gasen.
Diese Produkte behalten einen hohen Prozentsatz der Energie des ursprünglichen Ausgangsmaterials bei, was sie für andere Anwendungen nützlich macht.
Die richtige Wahl für Ihr Ziel treffen
Das Verständnis des Kernunterschieds ermöglicht es Ihnen, den richtigen Prozess basierend auf Ihrem Hauptziel auszuwählen.
- Wenn Ihr Hauptaugenmerk auf sofortiger und maximaler Wärmeerzeugung liegt: Die Verbrennung ist die direkteste und einfachste Methode zur Umwandlung der chemischen Energie eines Brennstoffs in thermische Energie.
- Wenn Ihr Hauptaugenmerk auf der Herstellung wertvoller, lagerfähiger Produkte aus einem Ausgangsmaterial liegt: Die Pyrolyse ist der notwendige Prozess, um chemische Energie in Form von Biokohle, Bio-Öl und Synthesegas zu konservieren.
Letztendlich hängt die Wahl zwischen dem Verbrennen eines Materials zur Wärmeerzeugung oder dem „Backen“ zur Herstellung neuer Produkte vollständig von der Anwesenheit von Sauerstoff ab.
Zusammenfassungstabelle:
| Merkmal | Verbrennung | Pyrolyse |
|---|---|---|
| Sauerstoffpräsenz | Mit Sauerstoff | Ohne Sauerstoff |
| Prozesstyp | Oxidativ | Thermische Zersetzung |
| Energie | Exotherm (Setzt Wärme frei) | Endotherm (Benötigt Wärme) |
| Hauptziel | Maximale Wärmeerzeugung | Herstellung wertvoller Produkte |
| Hauptprodukte | Wärme, CO₂, Wasserdampf, Asche | Biokohle, Bio-Öl, Synthesegas |
Bereit, den richtigen thermischen Prozess für die Anforderungen Ihres Labors auszuwählen?
Ob sich Ihre Forschung auf Energieerzeugung oder Materialumwandlung konzentriert, die richtige Ausrüstung ist entscheidend. KINTEK ist spezialisiert auf hochwertige Laboröfen und Reaktoren, die für die präzise Steuerung von Verbrennungs- und Pyrolyseprozessen entwickelt wurden. Unsere Lösungen gewährleisten die Genauigkeit und Wiederholbarkeit, die Ihre Experimente erfordern.
Lassen Sie uns Ihnen helfen, Ihre Forschungsziele zu erreichen. Kontaktieren Sie noch heute unsere Experten, um Ihre spezifische Anwendung zu besprechen und die perfekte Ausrüstung für Ihr Labor zu finden.
Visuelle Anleitung