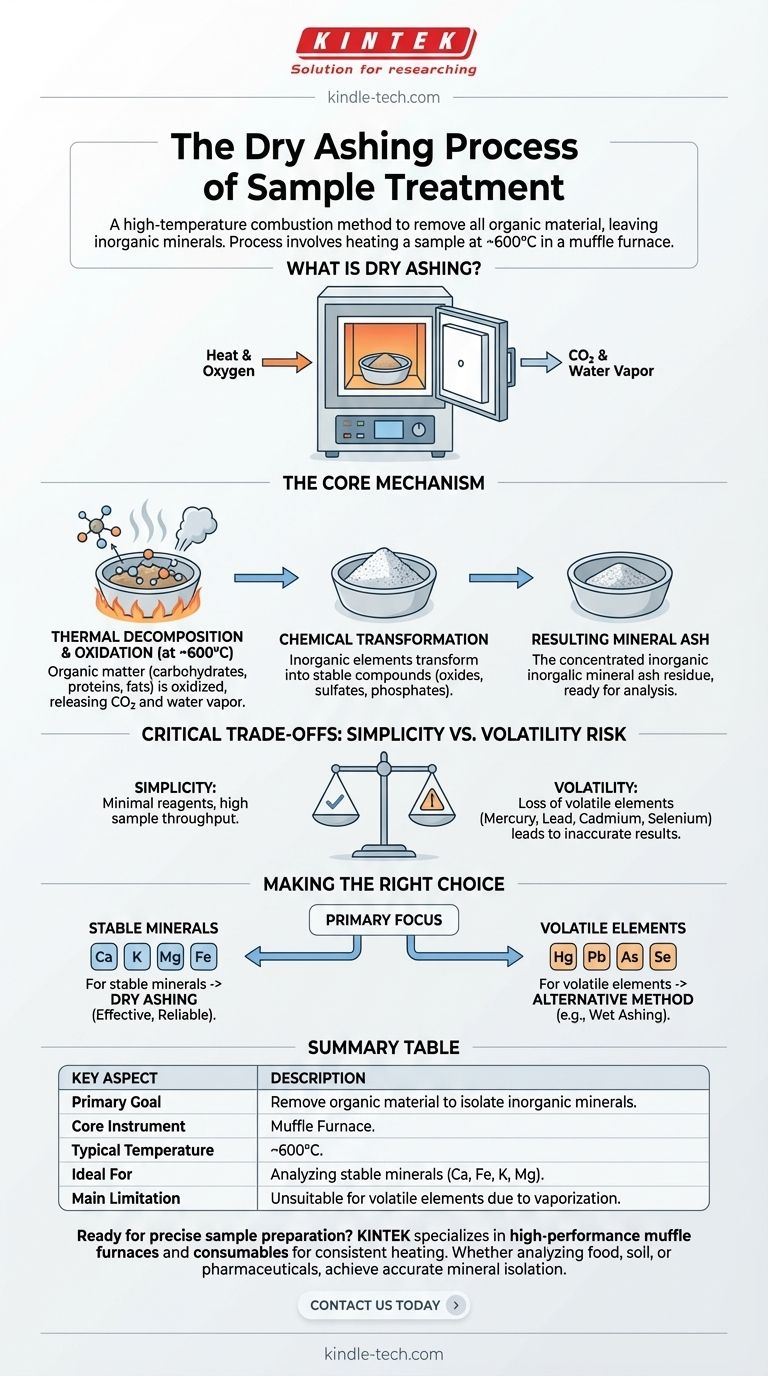
Im Wesentlichen ist die Trockenasche-Veraschung eine Hochtemperatur-Verbrennungsmethode, die verwendet wird, um alles organische Material aus einer Probe zu entfernen, sodass nur die anorganischen, mineralischen Bestandteile zur Analyse zurückbleiben. Der Prozess beinhaltet das Erhitzen einer Probe in einem speziellen Hochtemperaturofen, dem Muffelofen, auf Temperaturen um 600 °C, bis nur noch ein Mineralasche-Rückstand übrig ist.
Die Trockenasche-Veraschung ist eine leistungsstarke Technik zur Isolierung des gesamten Mineralgehalts einer Probe, aber ihre Hochtemperatur-Natur führt zu einem kritischen Kompromiss: Einfachheit und Effektivität gehen mit dem Risiko des Verlusts flüchtiger Mineralien einher, was zu ungenauen Ergebnissen führen kann.

Der Kernmechanismus der Trockenasche-Veraschung
Die Rolle des Muffelofens
Ein Muffelofen ist das primäre Instrument, das für die Trockenasche-Veraschung verwendet wird. Er bietet die präzise kontrollierte Hochtemperaturumgebung, die für eine vollständige Verbrennung erforderlich ist.
Der Ofen erhitzt die Probe, die typischerweise in einem Keramik- oder Porzellantiegel gehalten wird, treibt Wasser aus und verbrennt systematisch die organische Matrix.
Thermische Zersetzung und Oxidation
Wenn die Temperatur steigt, treten zwei Schlüsselprozesse auf. Zuerst verdampfen Wasser und andere flüchtige Verbindungen.
Dann, bei etwa 600 °C, wird die organische Materie (wie Kohlenhydrate, Proteine und Fette) vollständig oxidiert – sie reagiert mit dem Sauerstoff in der Luft und wird in Kohlendioxid und Wasserdampf umgewandelt, die freigesetzt werden.
Chemische Umwandlung von Mineralien
Die verbleibenden anorganischen Elemente liegen nicht in ihrer ursprünglichen Form vor. Die intensive Hitze wandelt sie in stabilere Verbindungen wie Oxide, Sulfate und Phosphate um.
Die resultierende Asche ist eine konzentrierte Probe des Mineralgehalts des ursprünglichen Materials, bereit für die weitere quantitative Analyse.
Verständnis der kritischen Kompromisse
Die Haupteinschränkung: Flüchtigkeit
Der größte Nachteil der Trockenasche-Veraschung ist der potenzielle Verlust flüchtiger Elemente. Mineralien wie Quecksilber, Blei, Cadmium und Selen können bei den hohen Temperaturen des Prozesses verdampfen.
Dieser Verlust führt zu einer Unterschätzung dieser Elemente in der Endanalyse und erzeugt ein ungenaues Ergebnis. Die Methode ist daher für Proben, bei denen diese spezifischen Elemente von Interesse sind, ungeeignet.
Einfachheit vs. Genauigkeit
Die Trockenasche-Veraschung wird oft wegen ihrer Einfachheit bevorzugt, da sie nur minimale Reagenzien erfordert und viele Proben gleichzeitig verarbeiten kann. Diese Einfachheit muss jedoch gegen das Potenzial für Ungenauigkeit abgewogen werden.
Wenn bekannt ist, dass eine Probe flüchtige Mineralien enthält, kann eine Niedertemperaturmethode oder eine andere Technik wie die Nassveraschung erforderlich sein, um genaue Ergebnisse zu gewährleisten.
Die richtige Wahl für Ihre Analyse treffen
Die Wahl der richtigen Probenvorbereitungsmethode hängt vollständig von Ihren analytischen Zielen ab.
- Wenn Ihr Hauptaugenmerk auf stabilen, nichtflüchtigen Mineralien liegt (z. B. Kalzium, Kalium, Magnesium, Eisen): Die Trockenasche-Veraschung ist eine äußerst effektive, einfache und zuverlässige Methode.
- Wenn Ihr Hauptaugenmerk auf flüchtigen oder Spurenelementen liegt (z. B. Quecksilber, Blei, Arsen, Selen): Die Trockenasche-Veraschung ist ungeeignet und liefert ungenaue Daten; Sie müssen eine alternative Methode wie die Nassveraschung verwenden.
Letztendlich ist das Verständnis der grundlegenden Prinzipien und Einschränkungen der Trockenasche-Veraschung der Schlüssel zur Erstellung zuverlässiger und aussagekräftiger analytischer Daten.
Zusammenfassungstabelle:
| Wesentlicher Aspekt | Beschreibung |
|---|---|
| Hauptziel | Entfernung von organischem Material zur Isolierung des anorganischen Mineralgehalts für die Analyse. |
| Kerninstrument | Muffelofen. |
| Typische Temperatur | ~600°C. |
| Ideal für | Analyse stabiler Mineralien wie Kalzium, Eisen, Kalium und Magnesium. |
| Haupteinschränkung | Aufgrund der Verdampfung ungeeignet für flüchtige Elemente (z. B. Quecksilber, Blei, Selen). |
Bereit für eine präzise und zuverlässige Probenvorbereitung?
Die richtige Ausrüstung ist entscheidend für eine genaue Trockenasche-Veraschung. KINTEK ist spezialisiert auf Hochleistungs-Muffelöfen und Laborverbrauchsmaterialien, die für eine konsistente Hochtemperaturbegheizung ausgelegt sind. Ob Sie Lebensmittel, Boden oder Pharmazeutika analysieren, unsere Lösungen helfen Ihnen, den Mineralgehalt sicher zu isolieren.
Kontaktieren Sie uns noch heute, um die spezifischen Anforderungen Ihres Labors zu besprechen, und lassen Sie sich von unseren Experten bei der Auswahl der perfekten Ausrüstung für Ihre Anwendung unterstützen.
Visuelle Anleitung
Ähnliche Produkte
- 1200℃ Muffelofen für Labor
- 1800℃ Muffelofen für Labor
- 1400℃ Muffelofen für Labor
- 1700℃ Muffelofen für Labor
- Hochtemperatur-Muffelofen für Laborentbinderung und Vorsintern
Andere fragen auch
- Warum wird ein Labor-Hochtemperatur-Muffelofen für die Nachglühbehandlung von Kupferoxid benötigt?
- Wie beeinflusst ein Muffelofen die Verdichtung von 8YSZ-Keramik? Meisterung der Präzisionssinterung bei 1500°C
- Wie wird ein Labor-Hochtemperatur-Muffelofen bei der Sol-Gel-Synthese für Perowskit-Katalysatoren eingesetzt?
- Warum wird ein Hochtemperatur-Muffelofen für die Kalzinierung von Ni-Ag-Katalysatorvorläufern verwendet? Aktivität optimieren
- Wie gewährleistet ein Muffelofen Zuverlässigkeit beim Kalzinierungsrösten? Präzision bei der Umwandlung von Pellets erreichen



















