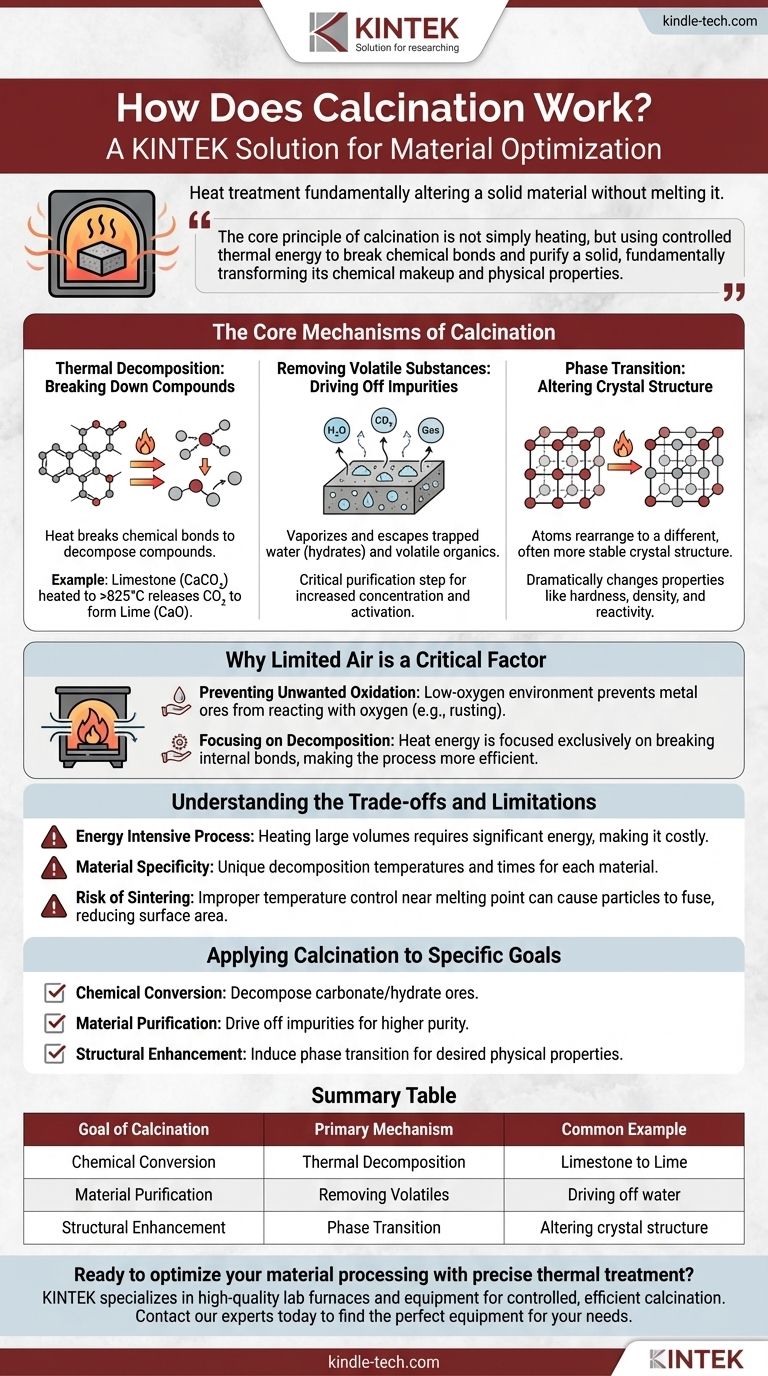
Im Wesentlichen ist die Kalzinierung ein Wärmebehandlungsprozess, der ein festes Material grundlegend verändert, ohne es zu schmelzen. Durch Erhitzen einer Substanz auf eine hohe Temperatur in einer sauerstoffarmen Umgebung erzwingt man die thermische Zersetzung, treibt flüchtige Verunreinigungen wie Wasser und Kohlendioxid aus oder verändert die innere Kristallstruktur des Materials.
Das Kernprinzip der Kalzinierung ist nicht einfach nur Erhitzen, sondern die Nutzung kontrollierter thermischer Energie, um chemische Bindungen zu brechen und einen Feststoff zu reinigen, wodurch dessen chemische Zusammensetzung und physikalische Eigenschaften grundlegend transformiert werden.

Die Kernmechanismen der Kalzinierung
Um zu verstehen, wie Kalzinierung funktioniert, müssen Sie die drei primären Veränderungen betrachten, die sie in einem Material hervorrufen kann, wenn es hoher Hitze ausgesetzt wird.
Thermische Zersetzung: Verbindungen aufbrechen
Dies ist das häufigste Ziel der Kalzinierung. Wärme liefert die notwendige Energie, um die chemischen Bindungen innerhalb einer Verbindung zu brechen, wodurch diese in einfachere Substanzen zerfällt.
Das klassische Beispiel ist die Herstellung von Kalk (Calciumoxid) aus Kalkstein (Calciumcarbonat). Beim Erhitzen auf über 825 °C (1517 °F) zerfällt der Kalkstein, setzt Kohlendioxidgas frei und hinterlässt den gereinigten Kalk.
Entfernen flüchtiger Substanzen: Verunreinigungen austreiben
Viele Rohstoffe enthalten eingeschlossenes Wasser (Hydrate) oder andere flüchtige organische Verbindungen. Die Kalzinierung erhitzt das Material bis zu einem Punkt, an dem diese Substanzen verdampfen und entweichen.
Dies ist ein entscheidender Reinigungsschritt, der eine konzentriertere oder wasserfreie (wasserfreie) Version des gewünschten Materials hinterlässt. Dies erhöht die Reinheit und kann das Material für nachfolgende Prozesse „aktivieren“.
Phasenübergang: Kristallstruktur verändern
Manchmal besteht das Ziel nicht darin, die chemische Zusammensetzung zu ändern, sondern die physikalische Form des Materials zu verändern.
Erhitzen kann dazu führen, dass sich die Atome in einem Feststoff neu anordnen und eine andere, oft stabilere oder nützlichere Kristallstruktur bilden. Dies wird als Phasenübergang bezeichnet und kann Eigenschaften wie Härte, Dichte und Reaktivität dramatisch verändern.
Warum begrenzte Luft ein entscheidender Faktor ist
Die Bedingung, eine begrenzte Luftzufuhr (oder gar keine Luft) zu verwenden, unterscheidet die Kalzinierung von anderen Wärmebehandlungen wie dem Rösten.
Verhindern unerwünschter Oxidation
Viele Metallerze reagieren beim Erhitzen in Gegenwart von Sauerstoff mit diesem zu einem Oxid. Dies ist derselbe grundlegende Prozess wie das Rosten.
Durch die Durchführung der Erhitzung in einer sauerstoffarmen Umgebung verhindert die Kalzinierung gezielt das Auftreten dieser unerwünschten Oxidationsreaktionen und stellt sicher, dass die gewünschte chemische Veränderung stattfindet.
Fokus auf Zersetzung
Wenn Sauerstoff aus der Gleichung entfernt wird, konzentriert sich die zugeführte Wärmeenergie ausschließlich auf eine Aufgabe: das Brechen der inneren Bindungen des Materials selbst. Dies macht den Prozess für seinen beabsichtigten Zweck effizienter und vorhersehbarer.
Verständnis der Kompromisse und Einschränkungen
Obwohl leistungsstark, ist die Kalzinierung ein präziser industrieller Prozess mit wichtigen Überlegungen.
Energieintensiver Prozess
Das Erhitzen großer Mengen fester Materialien auf Hunderte oder sogar Tausende von Grad erfordert eine erhebliche Menge an Energie. Dies macht es zu einem kostspieligen und ressourcenintensiven Schritt in jeder Produktionskette.
Materialspezifität
Es gibt keine universelle Temperatur für die Kalzinierung. Jedes Material hat eine einzigartige Zersetzungstemperatur und erforderliche Heizzeit. Was perfekt für Kalkstein funktioniert, kann für eine andere Erzart völlig unwirksam oder sogar zerstörerisch sein.
Risiko des Sinterns
Wenn die Temperatur unsachgemäß kontrolliert wird und zu nahe an den Schmelzpunkt des Materials gerät, können die Partikel zu verschmelzen beginnen. Dieser Prozess, Sintern genannt, kann die Oberfläche und Reaktivität des Endprodukts verringern, was oft unerwünscht ist.
Anwendung der Kalzinierung auf spezifische Ziele
Die Entscheidung, Kalzinierung anzuwenden, hängt vollständig von Ihrem gewünschten Ergebnis ab.
- Wenn Ihr Hauptaugenmerk auf der chemischen Umwandlung liegt: Kalzinierung ist die ideale Methode, um ein Carbonat- oder Hydraterz in eine nützlichere Oxidform zu zersetzen.
- Wenn Ihr Hauptaugenmerk auf der Materialreinigung liegt: Verwenden Sie Kalzinierung, um flüchtige Verunreinigungen wie Wasser oder Restlösungsmittel auszutreiben und ein konzentrierteres und reineres Endprodukt zu erzeugen.
- Wenn Ihr Hauptaugenmerk auf der strukturellen Verbesserung liegt: Wenden Sie Kalzinierung an, um einen Phasenübergang zu induzieren, der die Kristallstruktur des Materials ändert, um die gewünschten physikalischen Eigenschaften zu erreichen.
Letztendlich ist die Kalzinierung ein grundlegendes Werkzeug zur präzisen Steuerung der chemischen Zusammensetzung und physikalischen Eigenschaften fester Materialien.
Zusammenfassungstabelle:
| Ziel der Kalzinierung | Primärer Mechanismus | Häufiges Beispiel |
|---|---|---|
| Chemische Umwandlung | Thermische Zersetzung | Kalkstein (CaCO₃) zu Kalk (CaO) |
| Materialreinigung | Entfernung flüchtiger Stoffe | Austreiben von Wasser aus einem Hydrat |
| Strukturelle Verbesserung | Phasenübergang | Veränderung der Kristallstruktur eines Materials |
Bereit, Ihre Materialverarbeitung mit präziser Wärmebehandlung zu optimieren? Der Kalzinierungsprozess ist entscheidend, um die richtigen chemischen und physikalischen Eigenschaften Ihrer Materialien zu erzielen. KINTEK ist spezialisiert auf hochwertige Laboröfen und Geräte, die für eine kontrollierte, effiziente Kalzinierung entwickelt wurden. Ob in Forschung, Entwicklung oder Produktion, unsere Lösungen helfen Ihnen, Verunreinigungen auszutreiben, Phasenübergänge zu induzieren und überlegene Ergebnisse zu erzielen. Kontaktieren Sie noch heute unsere Experten, um die perfekte Kalzinierungsausrüstung für die spezifischen Anforderungen Ihres Labors zu finden.
Visuelle Anleitung