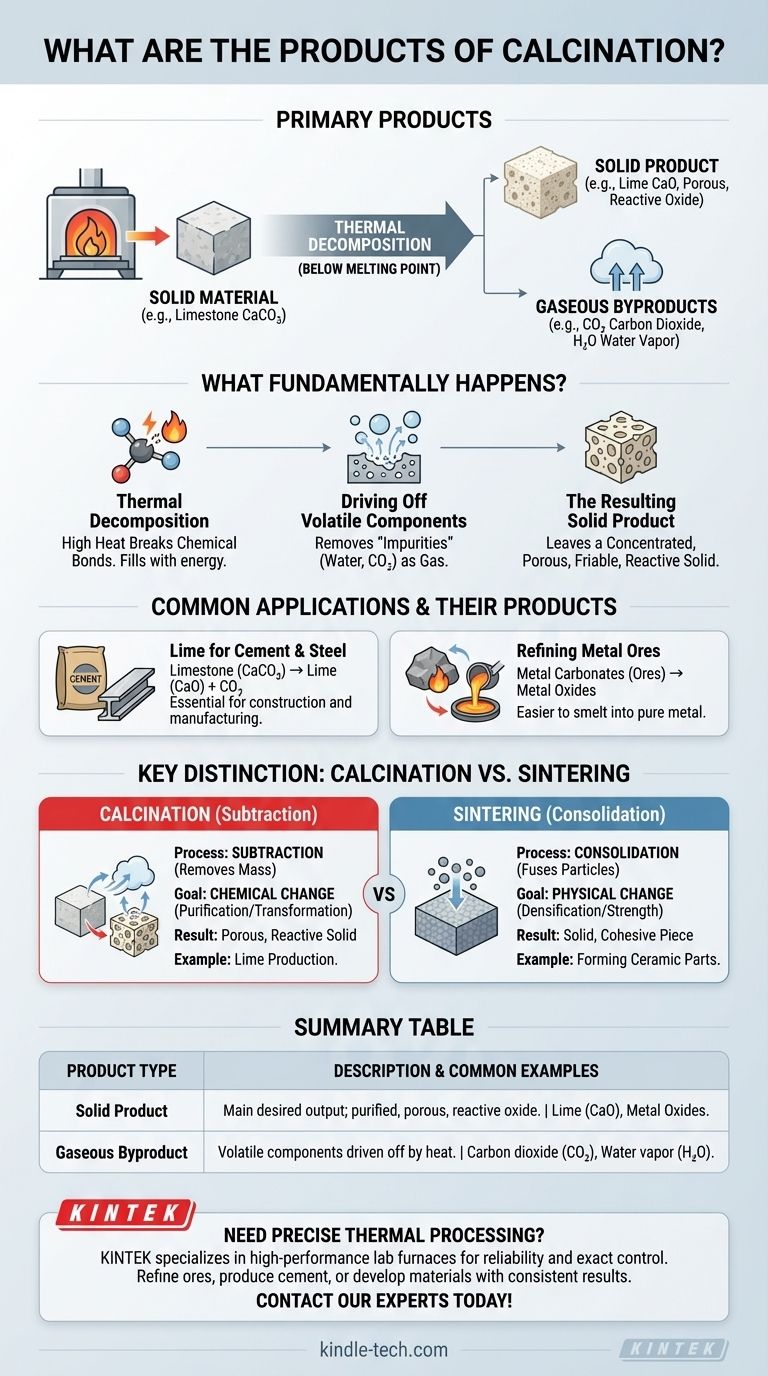
Kurz gesagt, die Hauptprodukte der Kalzinierung sind ein Feststoff, der einer thermischen Zersetzung unterzogen wurde, und ein oder mehrere gasförmige Nebenprodukte. Wenn beispielsweise Kalkstein (Calciumcarbonat) kalziniert wird, zersetzt er sich in festen Kalk (Calciumoxid) und Kohlendioxidgas, das durch die Hitze ausgetrieben wird. Der entstehende Feststoff ist das hauptsächlich gewünschte Produkt.
Die Kalzinierung ist im Grunde ein Reinigungs- und Umwandlungsprozess. Ihr Zweck ist es, einen festen Stoff zu erhitzen, um ihn chemisch aufzuspalten, wobei flüchtige Bestandteile wie Wasser oder Kohlendioxid ausgetrieben werden, um ein konzentrierteres, poröseres oder reaktiveres Festprodukt zu erzeugen.
Was passiert im Grunde während der Kalzinierung?
Das Prinzip der thermischen Zersetzung
Die Kalzinierung ist ein Prozess der thermischen Zersetzung, was bedeutet, dass hohe Hitze verwendet wird, um eine Verbindung in einfachere Substanzen zu zerlegen. Entscheidend ist, dass dies bei einer Temperatur unter dem Schmelzpunkt des Materials geschieht.
Der Prozess erzwingt eine chemische Veränderung durch das Brechen von Bindungen. Das häufigste Beispiel ist die Zersetzung eines Carbonats in sein Oxid und Kohlendioxidgas.
Austreiben flüchtiger Bestandteile
Das Kernziel der Kalzinierung ist die Entfernung von "flüchtigen" Substanzen, die chemisch im Feststoff gebunden sind. Der Verweis bezeichnet dies als die "Entfernung von Verunreinigungen".
Diese Substanzen sind typischerweise Wasser (aus hydratisierten Mineralien), Kohlendioxid (aus Carbonaten wie Kalkstein) oder andere zersetzbare Verbindungen. Die Erhitzung liefert die notwendige Energie, damit diese Komponenten als Gas entweichen können.
Das resultierende feste Produkt
Der verbleibende Feststoff ist das Hauptprodukt. Es handelt sich oft um ein Oxid des ursprünglichen Materials, wie Kalk (CaO) aus Kalkstein (CaCO₃).
Während das Gas entweicht, hinterlässt es eine poröse, brüchige Struktur. Deshalb beschreibt der Verweis den entstehenden Kalk als in einem "leicht pulverisierbaren Zustand", was seine Oberfläche und chemische Reaktivität erhöht.
Häufige Anwendungen und ihre Produkte
Herstellung von Kalk für Zement
Das ikonischste Beispiel ist die Herstellung von Kalk aus Kalkstein. Das feste Produkt, Kalk (Calciumoxid), ist ein grundlegender Bestandteil von Zement und wird auch in der Stahlherstellung und chemischen Produktion verwendet.
Raffinierung von Metallerzen
Die Kalzinierung ist ein wichtiger Schritt in der Metallurgie. Erze wie Zinkcarbonat (Smithsonit) oder Bleicarbonat (Cerussit) werden erhitzt, um sie in ihre jeweiligen Oxide umzuwandeln.
Diese Metalloxide sind das gewünschte Produkt, da sie in einem nachfolgenden Schritt viel einfacher zu reinem Metall reduziert (verhüttet) werden können.
Den Hauptunterschied verstehen: Kalzinierung vs. Sintern
Kalzinierung: Ein Prozess der Subtraktion
Die Kalzinierung ist ein subtraktiver Prozess. Sie entfernt Masse aus dem Material in Form von Gas.
Ihr Hauptziel ist die chemische Veränderung: die Reinigung eines Materials oder seine Umwandlung in ein nützlicheres chemisches Zwischenprodukt. Der resultierende Feststoff ist oft poröser und physikalisch schwächer.
Sintern: Ein Prozess der Konsolidierung
Das Sintern hingegen ist ein Prozess der Konsolidierung. Es verwendet Hitze, um kleine Partikel miteinander zu verschmelzen oder zu verschweißen, wodurch die Dichte und Festigkeit des Materials erhöht wird.
Es findet keine wesentliche chemische Veränderung statt, und es wird keine Masse verloren. Das Ziel ist es, ein Pulver in ein festes, zusammenhängendes Stück umzuwandeln, wie im Verweis angegeben.
Die richtige Wahl für Ihr Ziel treffen
Der gewählte Prozess hängt vollständig davon ab, was das Endmaterial leisten soll.
- Wenn Ihr Hauptaugenmerk auf der Reinigung eines Erzes oder der Herstellung eines chemischen Zwischenprodukts wie Kalk liegt: Sie beschäftigen sich mit der Kalzinierung, bei der das Schlüsselprodukt das feste Oxid ist, das nach dem Entfernen flüchtiger Gase zurückbleibt.
- Wenn Ihr Hauptaugenmerk darauf liegt, ein starkes, dichtes Endteil aus einem Pulver herzustellen: Sie beschäftigen sich mit dem Sintern, bei dem das Produkt eine feste Masse ist, die durch das Verschmelzen von Partikeln ohne chemische Veränderung entsteht.
Letztendlich ist das Verständnis, ob Sie ein Material zersetzen oder konsolidieren müssen, der Schlüssel zur Auswahl des richtigen thermischen Prozesses.

Zusammenfassungstabelle:
| Produkttyp | Beschreibung | Häufige Beispiele |
|---|---|---|
| Festes Produkt | Das hauptsächlich gewünschte Ergebnis; ein gereinigtes, poröses und reaktives Oxid. | Kalk (CaO) aus Kalkstein (CaCO₃), Metalloxide aus Erzen. |
| Gasförmiges Nebenprodukt | Flüchtige Bestandteile, die während der Zersetzung durch Hitze ausgetrieben werden. | Kohlendioxid (CO₂), Wasserdampf (H₂O). |
Benötigen Sie präzise thermische Verarbeitungsanlagen für Ihre Kalzinierungs- oder Sinterprojekte? KINTEK ist spezialisiert auf Hochleistungs-Laboröfen und thermische Verarbeitungssysteme, die auf Zuverlässigkeit und exakte Temperaturkontrolle ausgelegt sind. Ob Sie Erze veredeln, Zement herstellen oder neue Materialien entwickeln, unsere Ausrüstung gewährleistet konsistente, qualitativ hochwertige Ergebnisse. Kontaktieren Sie noch heute unsere Experten, um die perfekte Lösung für die Anforderungen Ihres Labors zu finden!
Visuelle Anleitung
Ähnliche Produkte
- Elektrische Drehrohrofen-Pyrolyseofenanlage Kalzinator Kleiner Drehrohrofen Rotierender Ofen
- Technische Keramik Aluminiumoxid Al2O3 Tiegel mit Deckel Zylindrischer Labor-Tiegel
- Technische Keramik Aluminiumoxid-Tiegel (Al2O3) für Thermische Analyse TGA DTA
- Hochtemperatur-verschleißfeste Aluminiumoxid-Al2O3-Platte für technische fortschrittliche Fein keramiken
- Vakuum Dental Porzellan Sinterofen
Andere fragen auch
- Wie hoch ist die Temperatur eines Drehrohrofens? Es hängt von Ihrem Material und Prozessziel ab
- Wie werden Drehrohröfen beheizt? Erklärung der direkten vs. indirekten Heizmethoden
- Bei welcher Temperatur findet die Pyrolyse statt? Ein Leitfaden zur Steuerung Ihres Produktausstoßes
- Was sind die Prinzipien eines Drehrohrofens? Beherrschen Sie die Mechanik der Hochtemperaturverarbeitung
- Ist ein Drehrohrofen ein Ofen? Entdecken Sie die Hauptunterschiede für die industrielle Verarbeitung












