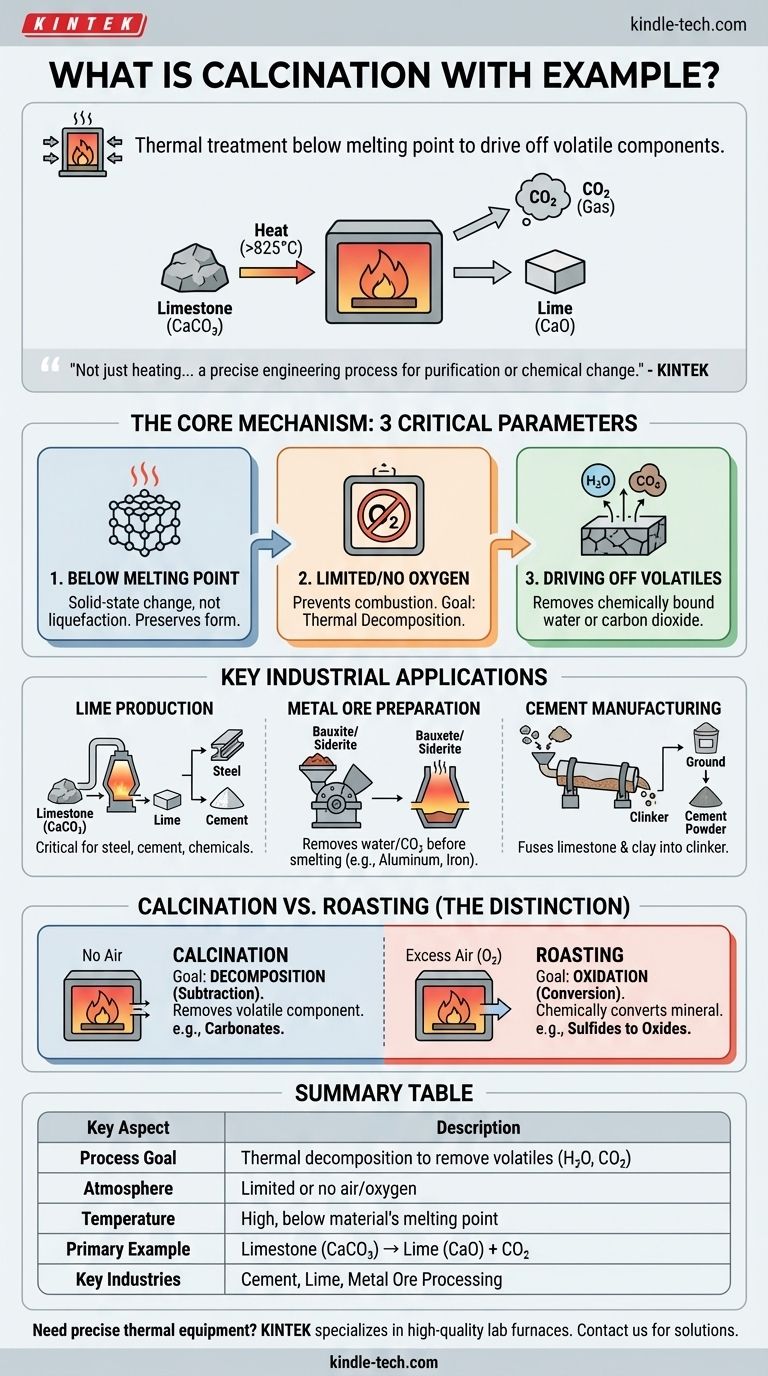
Im Kern ist die Kalzinierung ein thermisches Behandlungsverfahren, bei dem ein fester Werkstoff auf eine hohe Temperatur unterhalb seines Schmelzpunkts erhitzt wird, und zwar in Abwesenheit oder bei begrenzter Zufuhr von Luft. Diese kontrollierte Erhitzung dient nicht dazu, die Substanz zu schmelzen, sondern eine thermische Zersetzung zu bewirken, wodurch flüchtige Bestandteile ausgetrieben werden. Das häufigste Beispiel ist die Erhitzung von Kalkstein (Kalziumkarbonat) zur Herstellung von Branntkalk (Kalziumoxid) unter Freisetzung von Kohlendioxidgas.
Bei der Kalzinierung geht es nicht nur darum, etwas zu erhitzen. Es ist ein präzises technisches Verfahren, das darauf abzielt, ein Material zu reinigen oder seine chemische Zusammensetzung zu verändern, indem Wärme genutzt wird, um Bindungen zu brechen und spezifische flüchtige Substanzen wie Wasser oder Kohlendioxid auszutreiben.

Der Kernmechanismus: Was passiert bei der Kalzinierung?
Die Kalzinierung wird durch drei kritische Parameter definiert: Temperatur, Atmosphäre und die resultierende chemische Veränderung. Das Verständnis jedes Einzelnen ist der Schlüssel zum Erfassen des Prozesses.
Erhitzen unterhalb des Schmelzpunkts
Die Temperatur wird so weit erhöht, dass chemische Bindungen aufgebrochen werden, aber absichtlich unterhalb des Schmelzpunkts des Materials gehalten. Das Ziel ist es, eine Veränderung im festen Zustand hervorzurufen, nicht ihn zu verflüssigen.
Dadurch bleibt die feste Form des Materials erhalten, während seine chemische Zusammensetzung verändert wird, was es oft poröser oder reaktiver für nachfolgende Schritte macht.
Begrenzte oder keine Sauerstoffzufuhr
Der Prozess findet in einer Umgebung mit sehr wenig oder gar keinem Sauerstoff statt. Dies ist ein entscheidender Unterschied zu anderen Wärmebehandlungsverfahren.
Das Fehlen von Sauerstoff verhindert Verbrennung oder Oxidation. Das Ziel ist die thermische Zersetzung (Aufspaltung durch Hitze), nicht eine Reaktion mit der Umgebungsluft.
Austreiben flüchtiger Substanzen
Der Hauptzweck der Kalzinierung besteht darin, einen flüchtigen Anteil aus dem Feststoff zu entfernen. Dies beinhaltet typischerweise das Austreiben von chemisch gebundenem Wasser (Hydraten) oder Kohlendioxid (aus Karbonaten).
Wenn beispielsweise Kalkstein (CaCO₃) kalziniert wird, zerfällt er durch die Hitze in festen Branntkalk (CaO) und Kohlendioxidgas (CO₂), das entweicht.
Wichtige industrielle Anwendungen
Die Kalzinierung ist ein grundlegender Prozess in mehreren wichtigen Industrien und wird zur Vorbereitung von Materialien für die Weiterverarbeitung oder zur Herstellung eines Endprodukts eingesetzt.
Herstellung von Branntkalk aus Kalkstein
Dies ist das Paradebeispiel. Kalkstein wird auf über 825 °C (1517 °F) erhitzt, was die Reaktion verursacht: CaCO₃(s) → CaO(s) + CO₂(g).
Das resultierende Produkt, Branntkalk (CaO), ist eine entscheidende Komponente bei der Herstellung von Stahl, Zement und zahlreichen chemischen Prozessen.
Aufbereitung von Metallerzen
In der Metallurgie ist die Kalzinierung ein üblicher Vorbereitungsschritt vor dem Schmelzen. Sie entfernt Wasser aus hydratisierten Erzen wie Bauxit (Aluminiumerz) oder Siderit (Eisenerz).
Sie entfernt auch Kohlendioxid aus Karbonaterzen wie Smithsonit (ZnCO₃) oder Calamin (eine Mischung aus Zinkerzen), was die anschließende Metallgewinnung effizienter macht.
Herstellung von Zement
Die Herstellung von Portlandzement beinhaltet das Erhitzen einer Mischung aus Kalkstein und Ton in einem Ofen auf etwa 1450 °C (2640 °F).
Dieser Kalzinierungsprozess treibt CO₂ aus und verschmilzt die Materialien chemisch zu einer neuen Substanz, dem sogenannten „Klinker“. Der Klinker wird dann zu dem feinen Pulver zermahlen, das wir als Zement kennen.
Den Hauptunterschied verstehen: Kalzinierung vs. Rösten
Viele Menschen verwechseln Kalzinierung mit Rösten, einem weiteren Hochtemperaturverfahren in der Metallurgie. Der Unterschied liegt in den atmosphärischen Bedingungen und der beabsichtigten chemischen Reaktion.
Das Ziel der Kalzinierung: Zersetzung
Wie bereits dargelegt, nutzt die Kalzinierung Hitze in Abwesenheit von Luft, um eine Verbindung aufzubrechen. Es ist ein Prozess der Subtraktion, bei dem eine flüchtige Komponente aus dem Erz entfernt wird.
Das Ziel des Röstens: Oxidation
Das Rösten hingegen wird in überschüssiger Luft durchgeführt. Sein Zweck ist es, ein Mineral durch Oxidation in einen neuen Zustand umzuwandeln. Eine häufige Anwendung ist die Umwandlung von Sulfiderzen in leichter zu verarbeitende Oxide (z. B. 2ZnS + 3O₂ → 2ZnO + 2SO₂).
Die richtige Wahl für Ihre Analyse treffen
Um den beobachteten Prozess korrekt zu identifizieren, konzentrieren Sie sich auf die Inputs und den beabsichtigten Output.
- Wenn das Hauptziel die Entfernung von Wasser oder CO₂ aus einem Karbonat oder Hydrat ist: Sie beobachten eine Kalzinierung, die Hitze zur thermischen Zersetzung einer Verbindung nutzt.
- Wenn das Hauptziel die Reaktion eines Sulfiderzes mit Sauerstoff zur Bildung eines Oxids ist: Sie beobachten ein Rösten, das sowohl Hitze als auch überschüssige Luft nutzt, um eine Oxidation auszulösen.
- Wenn das Hauptziel die Herstellung von Zementklinker oder industriellem Branntkalk ist: Sie beobachten eine der am weitesten verbreiteten und kritischsten Anwendungen der Kalzinierung.
Das Verständnis dieses grundlegenden Unterschieds zwischen thermischer Zersetzung (Kalzinierung) und Oxidation (Rösten) ist der Schlüssel zum Beherrschen dieser zentralen industriellen Prozesse.
Zusammenfassungstabelle:
| Wesentlicher Aspekt | Beschreibung |
|---|---|
| Ziel des Prozesses | Thermische Zersetzung zur Entfernung flüchtiger Substanzen (z. B. H₂O, CO₂) |
| Atmosphäre | Begrenzte oder keine Luft/Sauerstoff |
| Temperatur | Hoch, aber unterhalb des Schmelzpunkts des Materials |
| Hauptbeispiel | Kalkstein (CaCO₃) → Branntkalk (CaO) + Kohlendioxid (CO₂) |
| Schlüsselindustrien | Zementherstellung, Branntkalkproduktion, Erzaufbereitung |
| Kontrastierender Prozess | Rösten (verwendet überschüssige Luft zur Oxidation) |
Benötigen Sie präzise thermische Verarbeitungsanlagen für Ihr Labor oder Ihre Produktionslinie?
Die Kalzinierung ist ein kritischer Schritt in vielen industriellen und Forschungsanwendungen und erfordert zuverlässige und genaue Heizeinrichtungen. KINTEK ist spezialisiert auf hochwertige Laboröfen und thermische Verarbeitungslösungen, die für Prozesse wie Kalzinierung, Rösten und mehr entwickelt wurden.
Unsere Geräte bieten die präzise Temperaturkontrolle und die atmosphärischen Bedingungen, die erforderlich sind, um konsistente Ergebnisse von hoher Reinheit zu erzielen, sei es bei der Verarbeitung von Mineralien, der Synthese von Materialien oder der Entwicklung neuer Produkte.
Kontaktieren Sie KINTEK noch heute, um zu besprechen, wie unsere spezialisierten thermischen Geräte die Effizienz und Genauigkeit Ihrer Materialverarbeitungsworkflows verbessern können.
Visuelle Anleitung
Ähnliche Produkte
- Elektrische Drehrohrofen-Pyrolyseofenanlage Kalzinator Kleiner Drehrohrofen Rotierender Ofen
- Elektrischer Drehrohrofen Kontinuierlicher Betrieb Kleine Drehrohrofen Heizpyrolyseanlage
- Nicht verzehrender Vakuumlichtbogen-Induktionsofen
- Vertikaler Hochtemperatur-Graphit-Vakuum-Graphitierungs-Ofen
- Graphitierungs-Vakuumofen für ultrahohe Temperaturen
Andere fragen auch
- Was sind die Prinzipien eines Drehrohrofens? Beherrschen Sie die Mechanik der Hochtemperaturverarbeitung
- Welche Arten von Kalzinatoren gibt es? Ein Leitfaden zur Auswahl der richtigen thermischen Verarbeitungsanlage
- Was ist ein elektrischer Drehrohrofen? Erzielen Sie eine überlegene gleichmäßige Erwärmung Ihrer Materialien
- Wie hoch ist die Temperatur eines Drehrohrofens? Es hängt von Ihrem Material und Prozessziel ab
- Wie hoch ist der Wirkungsgrad eines Drehrohrofens? Erreichen Sie einen thermischen Wirkungsgrad von über 95 %



















