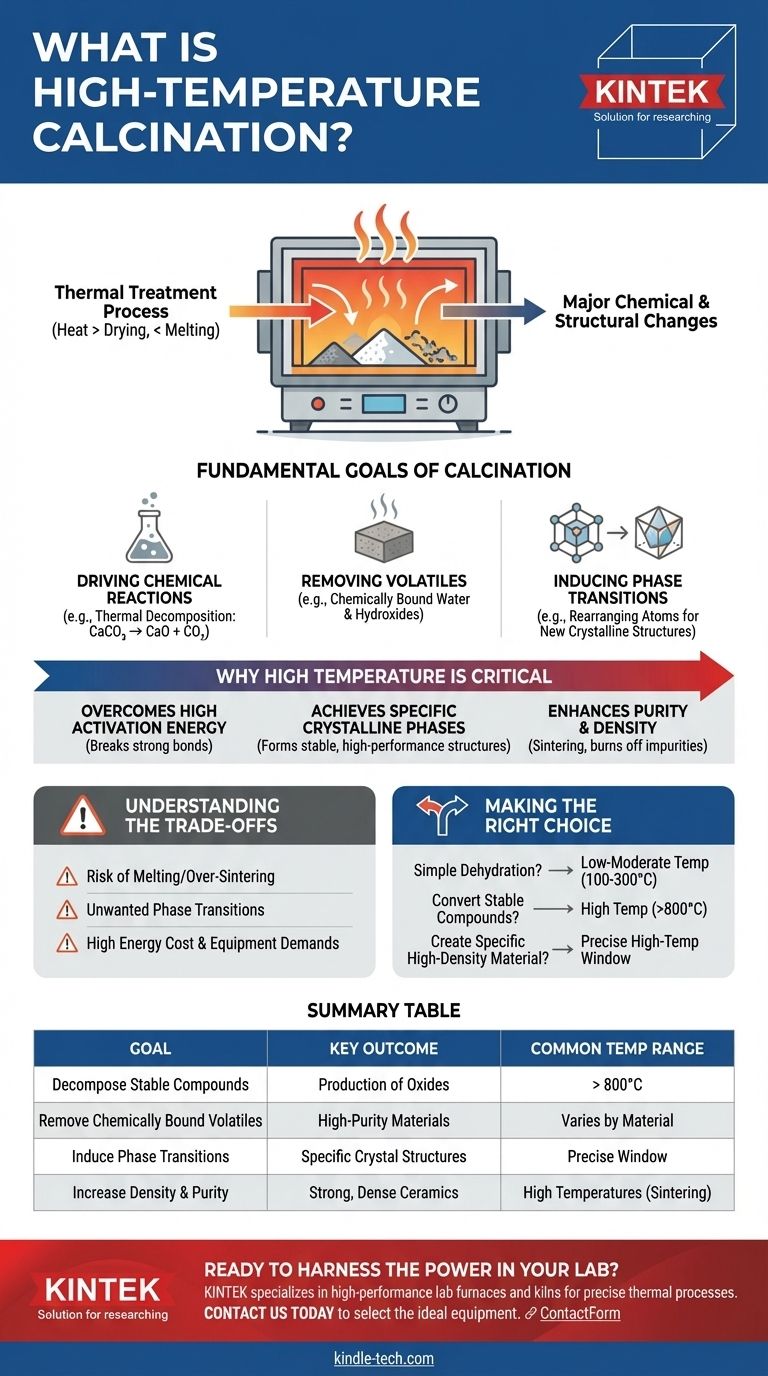
Im Wesentlichen ist die Hochtemperaturkalzinierung ein thermisches Behandlungsverfahren, das erhebliche Hitze nutzt – weit über das hinaus, was zum einfachen Trocknen erforderlich ist, aber unterhalb des Schmelzpunkts des Materials –, um große chemische oder strukturelle Veränderungen herbeizuführen. Im Gegensatz zu Varianten bei niedrigeren Temperaturen besteht ihr Zweck darin, hohe Energiebarrieren zu überwinden, typischerweise um hochstabile Verbindungen zu zersetzen, neue Kristallstrukturen zu erzeugen oder die Dichte und Reinheit eines Materials erheblich zu erhöhen.
Die spezifische Temperatur bei der Kalzinierung ist nicht willkürlich; sie ist die primäre Kontrollvariable, die die endgültigen Eigenschaften des Materials bestimmt. Hohe Temperaturen werden gezielt dann eingesetzt, wenn das Ziel darin besteht, eine chemische oder physikalische Umwandlung zu erzwingen, die einen erheblichen Energieeintrag erfordert.

Das grundlegende Ziel der Kalzinierung
Die Kalzinierung ist ein grundlegender Prozess in der Materialwissenschaft und Chemie. Ein fester Stoff wird in einer kontrollierten Atmosphäre (oft mit begrenzter oder keiner Luft) erhitzt, um eine spezifische Umwandlung zu erreichen.
Antrieb chemischer Reaktionen
Der häufigste Zweck der Kalzinierung ist die thermische Zersetzung. Hitze liefert die Energie, um chemische Bindungen aufzubrechen und eine Verbindung in eine neue Substanz umzuwandeln.
Ein klassisches industrielles Beispiel ist die Umwandlung von Kalkstein (Kalziumkarbonat, CaCO₃) in Branntkalk (Kalziumoxid, CaO) durch das Austreiben von Kohlendioxid (CO₂) bei Temperaturen, die oft 900 °C überschreiten.
Entfernung flüchtiger Bestandteile
Dies beinhaltet die Entfernung von Substanzen, die bei hohen Temperaturen flüchtig sind, aber bei Raumtemperatur chemisch gebunden sind. Dies geht über das einfache Trocknen hinaus.
Dazu gehört die Entfernung von chemisch gebundenem Wasser (Hydroxiden) oder anderen flüchtigen organischen oder anorganischen Verbindungen, die in der Struktur des Materials eingeschlossen sind.
Auslösung von Phasenübergängen
Hitze kann dazu führen, dass sich die Atome in einem Festkörper in eine andere Kristallstruktur umordnen, was als Phasenübergang bekannt ist.
Dies ist entscheidend, da verschiedene Kristallphasen desselben Materials sehr unterschiedliche Eigenschaften aufweisen können, wie Härte, Reaktivität oder Farbe.
Warum „Hohe Temperatur“ eine entscheidende Unterscheidung ist
Der Begriff „hohe Temperatur“ ist relativ, signalisiert aber, dass der Prozess genügend Energie für Umwandlungen erfordert, die bei mäßiger Hitze nicht möglich sind.
Überwindung hoher Aktivierungsenergie
Viele stabile Verbindungen, wie Karbonate und Sulfate, weisen sehr starke chemische Bindungen auf. Hohe Temperaturen liefern die notwendige Aktivierungsenergie, um diese Bindungen zu brechen und die Zersetzung einzuleiten. Man kann es sich so vorstellen, dass man einen viel größeren „Stoß“ benötigt, um die Reaktion zu starten.
Erreichen spezifischer Kristallphasen
Bestimmte Hochleistungsmaterialien, wie bestimmte Keramiken oder Katalysatoren, bilden ihre gewünschte, stabile Kristallphase nur bei sehr hohen Temperaturen. Die Hitze ermöglicht den Atomen genügend Mobilität, um sich in der energetisch günstigsten (und oft robustesten) Struktur einzulagern.
Verbesserung von Reinheit und Dichte
Bei hohen Temperaturen beginnen die Partikel in einem Prozess zu verschmelzen, der an das Sintern grenzt. Dieser Prozess verbrennt restliche organische Verunreinigungen, treibt Hohlräume zwischen den Partikeln aus und erhöht die endgültige Dichte und Festigkeit des Materials erheblich. Dies ist entscheidend bei der Herstellung von Keramiken und bestimmten Metallpulvern.
Die Abwägungen verstehen
Die Verwendung hoher Temperaturen bringt Komplexitäten und Risiken mit sich, die sorgfältig gemanagt werden müssen. Die Wahl der falschen Temperatur kann schlimmer sein als gar nichts zu tun.
Die Gefahr des Schmelzens oder Übersinterns
Das Grundprinzip der Kalzinierung ist das Erhitzen unterhalb des Schmelzpunkts. Wenn die Temperatur zu hoch oder schlecht kontrolliert ist, kann das Material schmelzen oder übermäßig sintern, wodurch seine gewünschten Eigenschaften wie die Oberfläche (bei einem Katalysator) oder die Partikelform zerstört werden.
Unerwünschte Phasenübergänge
So wie hohe Temperaturen eine gewünschte Kristallphase erzeugen können, kann das Überschreiten der optimalen Temperatur einen Übergang zu einer unerwünschten Phase auslösen. Dies kann das Endprodukt für seinen beabsichtigten Zweck unbrauchbar machen.
Energiekosten und Ausrüstungsanforderungen
Hochtemperaturprozesse sind von Natur aus energieintensiv und teuer. Sie erfordern spezielle Öfen (Brennöfen), die mit robusten feuerfesten Materialien gebaut sind, um extremen thermischen Belastungen standzuhalten, was erhebliche Betriebs- und Kapitalkosten verursacht.
Die richtige Wahl für Ihr Ziel treffen
Die korrekte Kalzinierungstemperatur wird ausschließlich durch das gewünschte Ergebnis für Ihr spezifisches Material bestimmt.
- Wenn Ihr Hauptaugenmerk auf einfacher Dehydratisierung liegt: Sie benötigen wahrscheinlich nur eine Kalzinierung bei niedriger bis mäßiger Temperatur (z. B. 100–300 °C), um physikalisch adsorbiertes Wasser zu entfernen.
- Wenn Ihr Hauptaugenmerk auf der Umwandlung stabiler Verbindungen wie Karbonaten in Oxide liegt: Sie benötigen eine Hochtemperaturkalzinierung (z. B. > 800 °C), um die Energie zuzuführen, die zum Aufbrechen starker chemischer Bindungen erforderlich ist.
- Wenn Ihr Hauptaugenmerk auf der Herstellung eines spezifischen hochdichten oder kristallinen Materials (wie einer Keramik) liegt: Sie müssen eine präzise gesteuerte Hochtemperaturkalzinierung verwenden, oft in einem spezifischen Temperaturbereich, um die Zielphase und -dichte ohne Schmelzen zu erreichen.
Letztendlich ist die Temperatur das mächtigste Werkzeug, das Ihnen zur Verfügung steht, um die endgültige Chemie und Struktur Ihres Materials zu definieren.
Zusammenfassungstabelle:
| Ziel der Hochtemperaturkalzinierung | Wichtigstes Ergebnis | Häufiger Temperaturbereich |
|---|---|---|
| Zersetzung stabiler Verbindungen (z. B. Karbonate) | Herstellung von Oxiden (z. B. Branntkalk aus Kalkstein) | > 800°C |
| Entfernung chemisch gebundener flüchtiger Bestandteile | Hochreine, dehydrierte Materialien | Materialabhängig |
| Auslösung von Phasenübergängen | Erzeugung spezifischer Kristallstrukturen | Präzises Hochtemperaturband |
| Erhöhung von Dichte & Reinheit | Feste, dichte Keramiken & Pulver | Hohe Temperaturen (Sintern) |
Bereit, die Kraft der Hochtemperaturkalzinierung in Ihrem Labor zu nutzen?
Die für eine erfolgreiche Kalzinierung erforderliche präzise Temperaturkontrolle ist entscheidend. KINTEK ist spezialisiert auf Hochleistungs-Laboröfen und Brennöfen, die für anspruchsvolle thermische Prozesse entwickelt wurden. Ob Sie Karbonate zersetzen, neue Keramiken entwickeln oder Materialien reinigen – unsere Ausrüstung gewährleistet die Genauigkeit und Wiederholbarkeit, die Sie benötigen.
Kontaktieren Sie uns noch heute über das untenstehende Formular, um Ihre spezifische Anwendung zu besprechen. Unsere Experten helfen Ihnen bei der Auswahl des idealen Ofens, um Ihre Materialumwandlungsziele zu erreichen.
Visuelle Anleitung
Ähnliche Produkte
- 1700℃ Labor-Hochtemperatur-Rohröfen mit Aluminiumoxidrohr
- 1400℃ Labor-Hochtemperatur-Rohröfen mit Aluminiumoxidrohr
- Hochtemperatur-Muffelofen für Laborentbinderung und Vorsintern
- Vakuum-Wärmebehandlungs- und Drucksinterofen für Hochtemperaturanwendungen
- Vertikaler Hochtemperatur-Graphit-Vakuum-Graphitierungs-Ofen
Andere fragen auch
- Welche Rolle spielt ein Hochtemperatur-Rohrofen bei der Synthese von N/O-codotiertem Kohlenstoff? Meistern Sie die präzise Dotierung
- Was sind die Hauptfunktionen eines Hochtemperatur-Röhrenofens für Iridium-basierte inverse Opale? Leitfaden zur Experten-Glühung
- Was sind die Hauptanwendungsbereiche von Muffel- und Röhrenöfen bei Photokatalysatoren? Optimierung der Metallbeladung & Trägersynthese
- Warum wird ein Hochtemperatur-Rohrofen für die Produktion von Biokohle aus Tabakstroh benötigt? Experte Pyrolyse-Leitfaden
- Welche Funktionen erfüllt ein Labor-Hochtemperatur-Röhrenofen? Beherrschung der Katalysatorsynthese & Karbonisierung



















