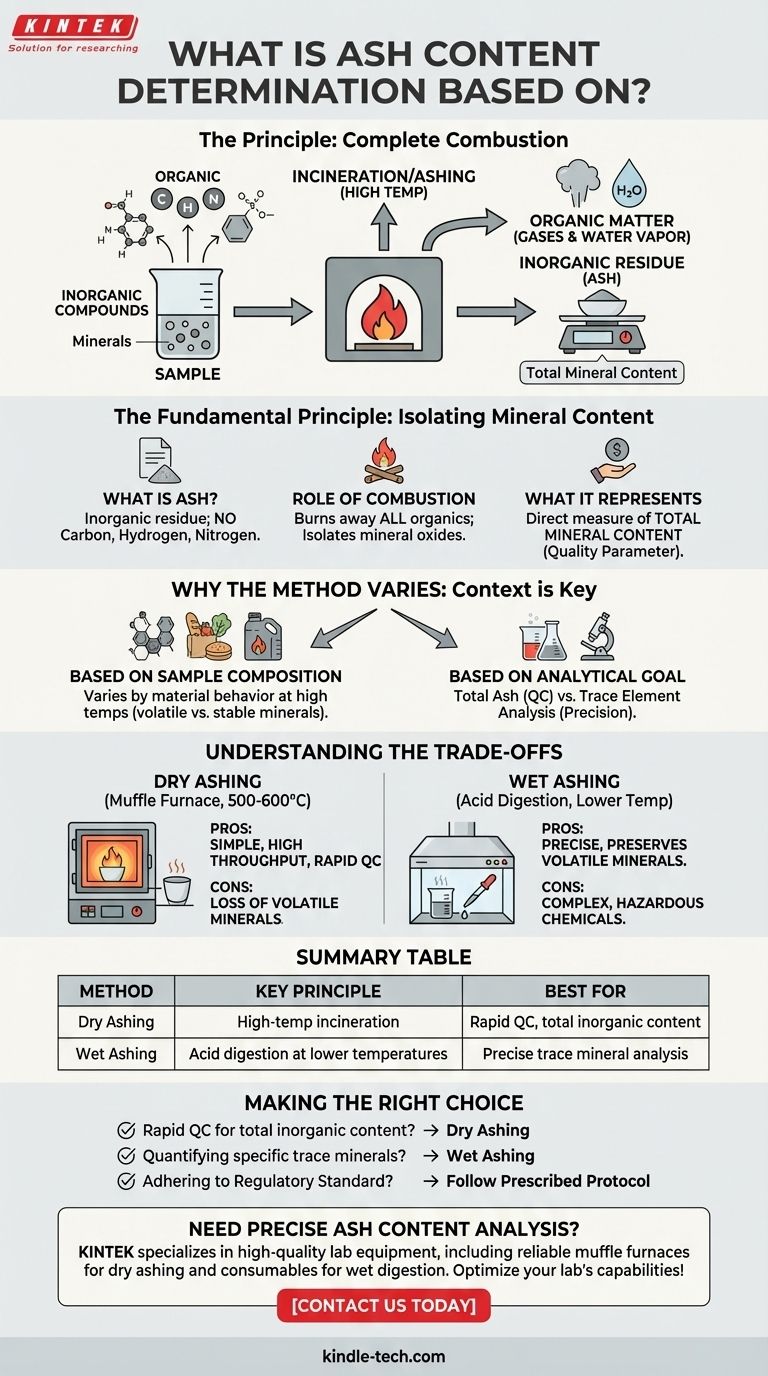
Kurz gesagt, die Bestimmung des Aschegehalts basiert auf dem Prinzip der vollständigen Verbrennung. Bei diesem Verfahren wird eine Probe bei hohen Temperaturen verbrannt, um sämtliche organische Materie zu eliminieren, sodass nur der anorganische, nicht brennbare Rückstand zurückbleibt, der anschließend gewogen wird. Dieser Rückstand oder die Asche repräsentiert den gesamten Mineralgehalt des ursprünglichen Materials.
Der Kern der Ascheanalyse besteht darin, die brennbaren organischen Bestandteile von den nicht brennbaren anorganischen Mineralien zu trennen. Die spezifische verwendete Methode – wie heiß, wie lange und mit welcher Vorbereitung – wird basierend auf der Probenart und dem letztendlichen Ziel der Analyse ausgewählt.

Das Grundprinzip: Isolierung des Mineralgehalts
Die Aschebestimmung ist eine grundlegende analytische Technik zur Quantifizierung der Gesamtmenge anorganischen Materials in einer Probe. Das Verfahren beruht auf einer einfachen, aber wirkungsvollen Trennmethode.
Was ist „Asche“?
Die Asche ist der anorganische Rückstand, der verbleibt, nachdem eine Probe vollständig verbrannt wurde. Sie enthält nicht die organischen Bestandteile wie Kohlenstoff, Wasserstoff und Stickstoff, die während des Brennens in Gase und Wasserdampf umgewandelt werden.
Die Rolle der vollständigen Verbrennung
Um die Asche zu isolieren, wird eine Probe in einem Hochtemperaturofen erhitzt. Dieser als Veraschung oder Kalzinierung bekannte Prozess verbrennt alle organischen Substanzen.
Das verbleibende Material ist eine Mischung aus Oxiden der anorganischen Elemente – den Mineralien –, die in der ursprünglichen Probe vorhanden waren.
Was das Ergebnis darstellt
Das Gewicht der Asche ist ein direkter Maßstab für den gesamten Mineralgehalt. Dies ist ein kritischer Qualitätsparameter in vielen Branchen, von der Lebensmittelwissenschaft (Nährwert) über Polymere (Füllstoffgehalt) bis hin zur Brennstoffanalyse (Verunreinigungen).
Warum die Methode variiert: Der Kontext ist entscheidend
Es gibt keine einzelne, universelle Methode zur Aschebestimmung. Die geeignete Technik wird basierend auf der spezifischen Probe und dem Grund für die Durchführung des Tests ausgewählt.
Basierend auf der Probenzusammensetzung
Verschiedene Materialien verhalten sich bei hohen Temperaturen unterschiedlich. Die gewählte Methode muss eine vollständige Verbrennung der organischen Matrix gewährleisten, ohne dass versehentlich anorganische Bestandteile verloren gehen, die gemessen werden sollen.
Beispielsweise erfordert eine Probe mit hohem Gehalt an flüchtigen Mineralien (wie Blei oder Quecksilber) ein anderes Temperaturprotokoll als eine Probe mit stabilen Mineralien (wie Kalzium oder Magnesium).
Basierend auf dem analytischen Ziel
Wenn das Ziel lediglich die Messung der Gesamtasche als Qualitätsmetrik ist, ist oft eine einfache Trockenveraschung ausreichend.
Wenn die Asche jedoch für die weitere Analyse spezifischer Spurenelemente vorbereitet wird, kann eine kontrolliertere Methode wie die Nassveraschung erforderlich sein, um sicherzustellen, dass diese Elemente während des Prozesses nicht verloren gehen.
Wichtige Methodenparameter
Die Wahl der Methode bestimmt mehrere kritische Parameter:
- Ofentemperatur: Muss hoch genug sein, um organische Stoffe zu verbrennen, aber niedrig genug, um die Verflüchtigung von Mineralien zu verhindern.
- Verweilzeit: Die Dauer im Ofen, die für eine vollständige Verbrennung erforderlich ist.
- Probenvorbereitung: Vortrocknung oder andere Schritte, die für konsistente Ergebnisse erforderlich sind.
Die Abwägungen verstehen
Die beiden gängigsten Ansätze, die Trockenveraschung und die Nassveraschung, stellen einen klassischen Kompromiss zwischen Einfachheit und analytischer Präzision dar.
Trockenveraschung: Einfachheit und Durchsatz
Dies ist die gängigste Methode, bei der die Probe in einem Muffelofen bei Temperaturen zwischen typischerweise 500–600 °C erhitzt wird.
Sie ist einfach, sicher und ermöglicht die gleichzeitige Verarbeitung vieler Proben. Ihre hohen Temperaturen können jedoch zum Verlust flüchtiger Mineralien führen, was zu ungenauen Ergebnissen führt, wenn diese Elemente von Interesse sind.
Nassveraschung: Präzision und Erhaltung
Die Nassveraschung oder Nassaufschluss verwendet starke Säuren und Oxidationsmittel (wie Salpetersäure oder Schwefelsäure) und niedrigere Hitze, um die organische Materie abzubauen.
Diese Methode ist komplexer und zeitaufwändiger und erfordert den Umgang mit gefährlichen Chemikalien. Ihr Hauptvorteil ist die Erhaltung flüchtiger Mineralien, was sie zur überlegenen Wahl macht, wenn die Asche ein Vorläufer für die Spurenelementanalyse ist.
Die richtige Wahl für Ihre Analyse treffen
Die Auswahl des richtigen Ansatzes hängt vollständig davon ab, was Sie über die Probe erfahren möchten.
- Wenn Ihr Hauptaugenmerk auf einer schnellen Qualitätskontrolle des gesamten anorganischen Gehalts liegt: Die Trockenveraschung ist in der Regel die effizienteste und praktischste Methode.
- Wenn Ihr Hauptaugenmerk auf der Quantifizierung spezifischer Spurenmineralien, insbesondere flüchtiger, liegt: Die Nassveraschung ist erforderlich, um den Elementverlust zu verhindern und eine genaue nachgeschaltete Analyse zu gewährleisten.
- Wenn Sie einen behördlichen oder industriellen Standard (z. B. AOAC, ASTM) einhalten: Die Wahl wird für Sie getroffen; Sie müssen das vorgeschriebene Protokoll genau befolgen.
Letztendlich ermöglicht Ihnen das Verständnis dessen, was Asche darstellt, die Daten korrekt zu interpretieren und fundierte Entscheidungen zu treffen.
Zusammenfassungstabelle:
| Methode | Schlüsselprinzip | Am besten geeignet für |
|---|---|---|
| Trockenveraschung | Hochtemperaturkalzinierung in einem Muffelofen | Schnelle Qualitätskontrolle, Gesamt-Anorganikgehalt |
| Nassveraschung | Säureaufschluss bei niedrigeren Temperaturen | Genaue Spurenmineralanalyse, flüchtige Elemente |
Müssen Sie eine präzise Aschegehaltsanalyse in Ihrem Labor durchführen? Die richtige Ausrüstung ist entscheidend für genaue Ergebnisse. KINTEK ist spezialisiert auf hochwertige Laborgeräte, einschließlich zuverlässiger Muffelöfen für die Trockenveraschung und Verbrauchsmaterialien für den Nassaufschluss. Unsere Experten helfen Ihnen bei der Auswahl der perfekten Werkzeuge, um sicherzustellen, dass Ihre Mineralanalyse sowohl effizient als auch präzise ist. Kontaktieren Sie uns noch heute, um die Fähigkeiten Ihres Labors zu optimieren!
Visuelle Anleitung
Ähnliche Produkte
- Hochtemperatur-Muffelofen für Laborentbinderung und Vorsintern
- Vertikaler Hochtemperatur-Graphit-Vakuum-Graphitierungs-Ofen
- Graphit-Vakuumofen Hochwärmeleitfähige Folien-Graphitierungsöfen
- Graphit-Vakuumofen mit Bodenentleerung für Kohlenstoffmaterialien
- Graphit-Vakuum-Durchlaufgraphitierungsöfen
Andere fragen auch
- Welche Rolle spielt ein Kalzinierofen bei der Herstellung von Hohlkern-Schalen-Partikeln? Perfekte Nanostrukturen erzielen
- Warum ist die Ausglühbehandlung in einem Hochtemperatur-Muffelofen entscheidend für die Herstellung einer Sb-SnO2-Zwischenschicht?
- Welche Rolle spielt eine Muffelofen beim Rösten von Magnetitpellets? Optimierung der Mineralphase und Druckfestigkeit
- Welche Bedingungen bietet eine Muffelofen für die Speicherung von Energie aus Salzschmelzen? Experten-Simulation für CSP-Umgebungen
- Welche Bedeutung hat die Integration eines Hochtemperatur-Muffelofens in ein Schlagverschleiß-Prüfsystem?







