Im Wesentlichen ist die Kalzinierung ein thermischer Reinigungsprozess. Er beinhaltet das Erhitzen eines festen Materials auf eine hohe Temperatur, jedoch unterhalb seines Schmelzpunkts, in einer kontrollierten Atmosphäre mit wenig oder keiner Luft. Diese präzise Erhitzung treibt flüchtige Substanzen wie Wasser und Kohlendioxid aus, löst chemische Zersetzung aus oder verändert die innere Kristallstruktur des Materials, was zu einem reineren, stabileren oder reaktiveren Feststoff führt.
Der Kernzweck der Kalzinierung besteht nicht darin, ein Material zu schmelzen, sondern es umzuwandeln. Durch sorgfältige Kontrolle von Hitze und Atmosphäre können unerwünschte Bestandteile selektiv entfernt oder die Eigenschaften eines Materials verändert werden, ohne seinen festen Zustand zu verändern.

Wie die Kalzinierung grundlegend funktioniert
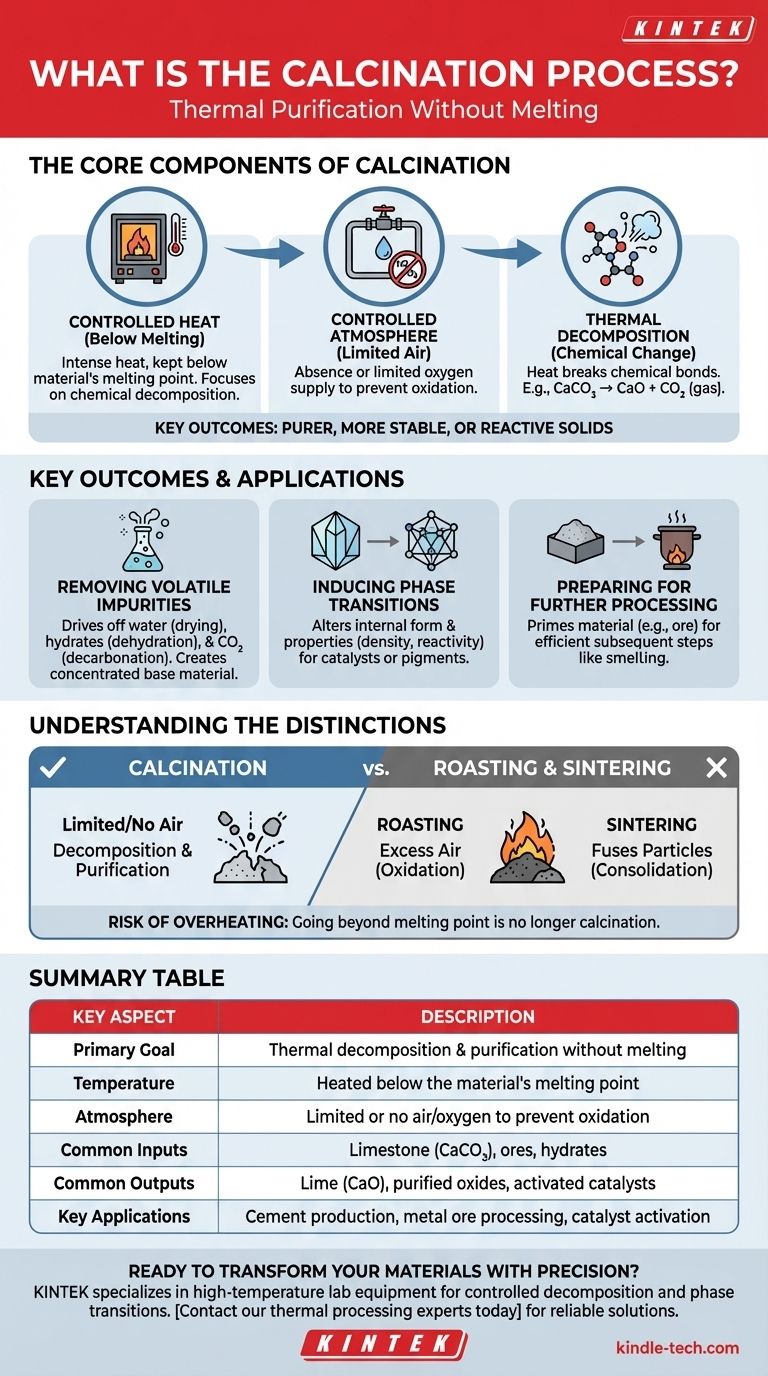
Um die Kalzinierung zu verstehen, ist es wichtig, ihre drei Kernkomponenten zu erfassen: kontrollierte Hitze, eine spezifische Atmosphäre und die daraus resultierenden chemischen Veränderungen.
Die Rolle der Hitze (unterhalb des Schmelzpunkts)
Der kritischste Parameter bei der Kalzinierung ist die Temperatur. Das Material wird intensiv erhitzt, aber immer unterhalb seines Schmelzpunkts gehalten.
Dies stellt sicher, dass sich der Prozess auf die chemische Zersetzung und nicht auf eine Zustandsänderung (von fest zu flüssig) konzentriert. Es ermöglicht den kontrollierten Abbau von Verbindungen innerhalb der festen Struktur.
Die kontrollierte Atmosphäre
Die Kalzinierung wird typischerweise in Abwesenheit oder bei begrenzter Zufuhr von Luft (Sauerstoff) durchgeführt.
Dies ist ein entscheidender Unterschied. Durch die Begrenzung des Sauerstoffs wird eine Oxidation oder Verbrennung verhindert. Das Ziel ist es, das Material allein durch Hitze (thermische Zersetzung) abzubauen, nicht es mit Sauerstoff reagieren zu lassen.
Das Hauptziel: Zersetzung
Die während der Kalzinierung zugeführte Wärme liefert die Energie, die zum Brechen chemischer Bindungen erforderlich ist. Dies wird als thermische Zersetzung bezeichnet.
Ein klassisches Beispiel ist die Herstellung von Kalk aus Kalkstein. Wenn Kalkstein (Calciumcarbonat, CaCO₃) kalziniert wird, zersetzt er sich zu Kalk (Calciumoxid, CaO) und setzt Kohlendioxid (CO₂) als flüchtigen Bestandteil frei.
Wichtige Ergebnisse der Kalzinierung
Abhängig vom Material und dem Ziel werden durch die Kalzinierung mehrere spezifische Ergebnisse erzielt.
Entfernung flüchtiger Verunreinigungen
Die häufigste Anwendung ist die Reinigung. Der Prozess treibt flüchtige Substanzen aus, also Bestandteile, die sich beim Erhitzen leicht in Gas umwandeln.
Dazu gehören physikalisch gebundenes Wasser (Trocknung), chemisch gebundenes Wasser in Hydraten (Dehydratisierung) und Kohlendioxid aus Karbonaterzen (Dekarbonisierung). Das Ergebnis ist eine konzentriertere und reinere Version des Grundmaterials.
Auslösung von Phasenübergängen
Manchmal besteht das Ziel nicht darin, etwas zu entfernen, sondern die innere Form des Materials zu verändern.
Die Kalzinierung kann einen Phasenübergang auslösen, der die Kristallstruktur des Materials verändert. Dies kann seine Eigenschaften wie Härte, Dichte oder Reaktivität verändern und es für einen bestimmten Anwendungszweck als Katalysator oder Pigment geeignet machen.
Vorbereitung von Materialien für die Weiterverarbeitung
Oft ist die Kalzinierung ein vorbereitender Schritt. Durch die Entfernung von Verunreinigungen und die Erzeugung einer reaktiveren Substanz (wie ein Oxid) wird das Material für einen nachfolgenden Prozess vorbereitet.
Beispielsweise kann die Kalzinierung eines Erzes die anschließende Gewinnung des Endmetalls durch Schmelzen effizienter und weniger energieintensiv machen.
Verständnis der Kompromisse und Unterschiede
Die Kalzinierung wird oft mit anderen thermischen Prozessen verwechselt. Das Verständnis der Unterschiede ist entscheidend, um ihre spezifische Funktion zu erfassen.
Kalzinierung vs. Rösten
Das Rösten ist ebenfalls ein thermischer Prozess, wird aber mit einem Überschuss an Luft durchgeführt. Sein Ziel ist die gezielte Oxidation. Zum Beispiel die Umwandlung eines Metallsulfiderzes in ein Metalloxid. Die Kalzinierung hingegen vermeidet aktiv die Oxidation.
Kalzinierung vs. Sintern
Auch das Sintern verwendet Hitze unterhalb des Schmelzpunkts, aber sein Ziel ist völlig anders. Das Sintern zielt darauf ab, kleine Partikel miteinander zu verschmelzen, um die Dichte und Festigkeit des Materials zu erhöhen. Die Kalzinierung reinigt und zersetzt; das Sintern konsolidiert. In vielen industriellen Arbeitsabläufen wird zuerst kalziniert und anschließend gesintert.
Die Gefahr der Überhitzung
Die Kontrolle der Temperatur ist von größter Bedeutung. Wird das Material über seinen Schmelzpunkt erhitzt, handelt es sich nicht mehr um Kalzinierung. Es wird zu Schmelzen oder Sintern, was unerwünscht sein kann und zu einem völlig anderen und oft unbrauchbaren Endprodukt führt.
Die richtige Wahl für Ihr Ziel treffen
Die Kalzinierung ist ein präzises Werkzeug zur Erzielung spezifischer Materialumwandlungen. Ihr Ziel bestimmt ihre Anwendung.
- Wenn Ihr Hauptaugenmerk auf der Reinigung eines Erzes liegt: Verwenden Sie die Kalzinierung, um Wasser und Carbonate auszutreiben und so ein konzentrierteres Oxid vor dem Schmelzen zu erzeugen.
- Wenn Ihr Hauptaugenmerk auf der Zementherstellung liegt: Die Kalzinierung von Kalkstein zur Herstellung von Kalk ist der grundlegende, unverzichtbare erste Schritt im Prozess.
- Wenn Ihr Hauptaugenmerk auf der Aktivierung eines Katalysators liegt: Verwenden Sie die Kalzinierung, um die ideale Kristallstruktur und Oberfläche zu erreichen, die für eine hohe chemische Reaktivität erforderlich sind.
Letztendlich ist die Kalzinierung eine grundlegende Technik in der Materialwissenschaft zur gezielten Modifizierung der chemischen Zusammensetzung und Struktur eines Feststoffs durch Hitze.
Zusammenfassungstabelle:
| Wesentlicher Aspekt | Beschreibung |
|---|---|
| Hauptziel | Thermische Zersetzung und Reinigung ohne Schmelzen |
| Temperatur | Erhitzt unterhalb des Schmelzpunkts des Materials |
| Atmosphäre | Begrenzte oder keine Luft/Sauerstoff, um Oxidation zu verhindern |
| Häufige Eingaben | Kalkstein (CaCO₃), Erze, Hydrate |
| Häufige Ausgaben | Kalk (CaO), gereinigte Oxide, aktivierte Katalysatoren |
| Wichtige Anwendungen | Zementherstellung, Metallerzverarbeitung, Katalysatoraktivierung |
Bereit, Ihre Materialien präzise zu transformieren?
Der Kalzinierungsprozess ist entscheidend für die Reinigung von Erzen, die Herstellung von Zement und die Aktivierung von Katalysatoren. KINTEK ist spezialisiert auf die Hochtemperatur-Laborgeräte, die für die zuverlässige und effiziente Durchführung dieser präzisen thermischen Umwandlungen erforderlich sind.
Egal, ob Sie Mineralien verarbeiten oder fortschrittliche Materialien entwickeln, unsere Expertise bei Laboröfen und Verbrauchsmaterialien stellt sicher, dass Sie über die richtigen Werkzeuge für kontrollierte Zersetzung und Phasenübergänge verfügen.
Kontaktieren Sie noch heute unsere Experten für thermische Prozesse, um zu besprechen, wie KINTEK-Lösungen Ihren Kalzinierungs-Workflow optimieren und Ihre Materialergebnisse verbessern können.
Visuelle Anleitung
Ähnliche Produkte
- Elektrische Drehrohrofen-Pyrolyseofenanlage Kalzinator Kleiner Drehrohrofen Rotierender Ofen
- Elektrischer Drehrohrofen Kontinuierlicher Betrieb Kleine Drehrohrofen Heizpyrolyseanlage
- Vertikaler Hochtemperatur-Graphit-Vakuum-Graphitierungs-Ofen
- Graphit-Vakuumofen Hochwärmeleitfähige Folien-Graphitierungsöfen
- Graphitierungs-Vakuumofen für ultrahohe Temperaturen
Andere fragen auch
- Was sind die Vorteile von Drehrohrofen? Erreichen Sie überlegene Gleichmäßigkeit & Effizienz
- Was sind die Nachteile eines Drehrohrofens? Hohe Kosten und betriebliche Herausforderungen
- Was sind die Prinzipien eines Drehrohrofens? Beherrschen Sie die Mechanik der Hochtemperaturverarbeitung
- Wie hoch ist die Temperatur eines Drehrohrofens? Es hängt von Ihrem Material und Prozessziel ab
- Was sind die Merkmale der Gleit-, Einsink- und Rollbewegungsmodi von Schüttgütern? Optimieren Sie Ihren Drehprozess



















