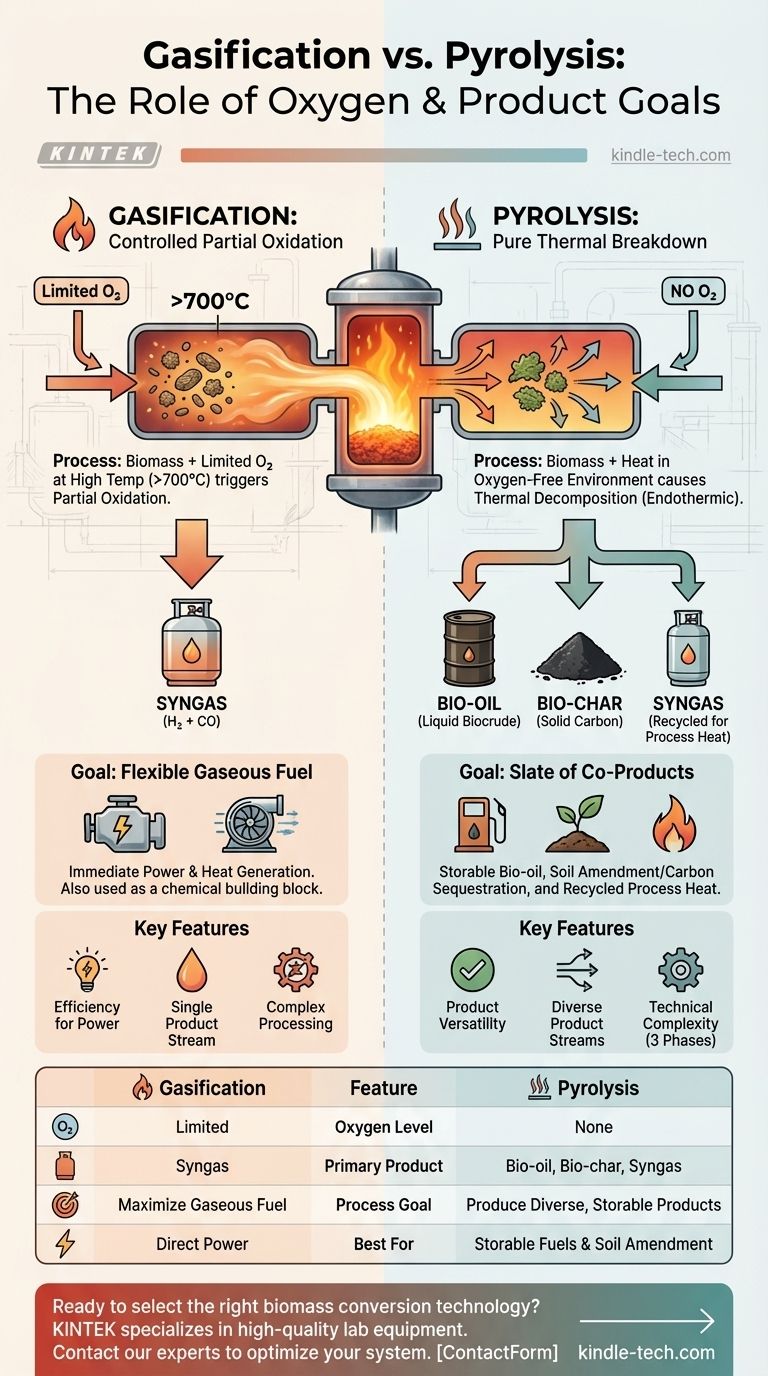
Grundsätzlich besteht der Hauptunterschied zwischen Vergasung und Pyrolyse in der Anwesenheit von Sauerstoff. Die Vergasung verwendet eine begrenzte, kontrollierte Menge Sauerstoff bei hohen Temperaturen, um Biomasse hauptsächlich in ein brennbares Gas umzuwandeln. Die Pyrolyse hingegen ist die thermische Zersetzung von Biomasse in völliger Abwesenheit von Sauerstoff, wodurch diese in eine Mischung aus flüssigem Bio-Öl, fester Biokohle und Gas zerfällt.
Dieser Unterschied ist nicht nur ein technisches Detail; er definiert den Kernzweck jedes Prozesses. Die Vergasung ist darauf ausgelegt, den Ausstoß eines einzigen Produkts – gasförmiger Brennstoff (Synthesegas) – für die sofortige Strom- und Wärmeerzeugung zu maximieren. Die Pyrolyse ist darauf ausgelegt, eine vielfältige Palette wertvoller und lagerfähiger Produkte zu erzeugen: flüssig, fest und gasförmig.

Die Rolle des Sauerstoffs: Oxidation vs. thermische Zersetzung
Die Entscheidung, Sauerstoff einzubeziehen oder auszuschließen, verändert die chemischen Reaktionen, die ablaufen, die Energiebilanz des Systems und die Art der Endprodukte grundlegend.
Vergasung: Kontrollierte partielle Oxidation
Bei der Vergasung wird ein Ausgangsmaterial wie Biomasse sehr hohen Temperaturen (typischerweise über 700 °C) mit einer unzureichenden Sauerstoffmenge für eine vollständige Verbrennung ausgesetzt.
Diese „sauerstoffarme“ Umgebung löst eine partielle Oxidation aus. Dieser Prozess setzt etwas Energie frei, was hilft, die Reaktion anzutreiben, während die Biomasse in ein Hauptprodukt zerfällt: Synthesegas oder Syngas. Syngas ist eine Mischung hauptsächlich aus Wasserstoff (H₂) und Kohlenmonoxid (CO).
Pyrolyse: Reine thermische Zersetzung
Die Pyrolyse ist ein streng thermochemischer Prozess. Durch das Erhitzen von Biomasse in einer sauerstofffreien (anaeroben) Umgebung verhindern Sie eine Verbrennung.
Anstatt zu brennen, spaltet die Hitze die komplexen organischen Polymere der Biomasse in kleinere Moleküle auf. Da keine Oxidation stattfindet, ist dieser Prozess hauptsächlich endotherm, was bedeutet, dass er eine konstante externe Energiequelle benötigt, um fortzufahren. Die entstehenden Produkte behalten einen hohen Anteil des ursprünglichen Energiegehalts des Ausgangsmaterials bei.
Eine Geschichte von zwei Produktströmen
Die unterschiedlichen chemischen Prozesse der Vergasung und der Pyrolyse führen zu völlig unterschiedlichen Ergebnissen, die jeweils für verschiedene Anwendungen geeignet sind.
Das Ziel der Vergasung: Ein flexibler gasförmiger Brennstoff
Das primäre Ergebnis der Vergasung ist Synthesegas. Dies ist ein unglaublich flexibles Zwischenprodukt.
Es kann direkt in Gasmotoren oder Turbinen verbrannt werden, um effizient Strom und Wärme zu erzeugen. Es kann auch als chemischer Baustein zur Synthese von flüssigen Brennstoffen (wie Diesel) oder wertvollen Chemikalien (wie Methanol und Ammoniak) verwendet werden.
Das Ziel der Pyrolyse: Eine Palette von Koppelprodukten
Die Pyrolyse ist nicht darauf ausgelegt, einen einzigen Ertrag zu maximieren, sondern drei verschiedene und wertvolle Produktströme gleichzeitig zu erzeugen.
- Bio-Öl: Eine Flüssigkeit, manchmal als Pyrolyseöl oder Biokohle bezeichnet, die gelagert, transportiert und zu erneuerbaren Kraftstoffen wie Benzin und Diesel aufbereitet werden kann.
- Biokohle: Ein stabiler, kohlenstoffreicher Feststoff, der ein ausgezeichneter Bodenverbesserer ist, da er die Wasserspeicherung und Nährstoffverfügbarkeit verbessert. Er dient auch als wirksame Methode zur langfristigen Kohlenstoffabscheidung.
- Synthesegas: Ein geringeres Volumen an nicht kondensierbaren Gasen, das oft recycelt wird, um die für den Betrieb des Pyrolyse-Reaktors erforderliche Prozesswärme zu liefern, wodurch das System autarker wird.
Die Abwägungen verstehen
Die Wahl zwischen diesen Technologien beinhaltet die Abwägung der Effizienz der Energieumwandlung gegenüber der Vielseitigkeit der Produkte.
Effizienz für die Stromerzeugung
Für die direkte Erzeugung von Strom und Wärme gilt die Vergasung im Allgemeinen als der effizientere Weg. Der Prozess ist optimiert, um die maximale Energiemenge des Ausgangsmaterials in ein einziges, brennbares Gas umzuwandeln, das für den Einsatz in Stromerzeugungssystemen bereit ist.
Vielseitigkeit der Produkte
Die Pyrolyse bietet eine überlegene Produktvielfalt. Anstatt die gesamte Biomasseenergie für die sofortige Stromerzeugung zu verwenden, erstellen Sie ein Portfolio von Produkten. Lagerfähiges Bio-Öl wirkt wie ein erneuerbares Rohöl, und Biokohle hat ihren eigenen ausgeprägten wirtschaftlichen und ökologischen Wert. Diese Flexibilität kann je nach Marktbedingungen ein erheblicher Vorteil sein.
Prozesskomplexität
Das Ergebnis der Vergasung ist ein einziger Gasstrom, was die nachgeschaltete Verarbeitung vereinfachen kann. Die Pyrolyse hingegen erzeugt Ergebnisse in drei verschiedenen Phasen (fest, flüssig und gasförmig), die gesammelt, getrennt und verarbeitet werden müssen, was die technische Komplexität des Gesamtsystems erhöhen kann.
Die richtige Wahl für Ihr Ziel treffen
Ihre Wahl zwischen Vergasung und Pyrolyse sollte von Ihrem Endziel bestimmt werden, nicht von den Prozessen selbst.
- Wenn Ihr Hauptaugenmerk auf sofortigem Strom oder Prozesswärme liegt: Die Vergasung ist der direktere und effizientere Weg, der Biomasse in ein brennbares Synthesegas umwandelt, das für Stromsysteme konzipiert ist.
- Wenn Ihr Hauptaugenmerk auf der Herstellung lagerfähiger flüssiger Brennstoffe oder wertvoller Koppelprodukte wie Biokohle liegt: Die Pyrolyse ist die überlegene Wahl, da sie speziell dafür entwickelt wurde, Biomasse in Bio-Öl und Biokohle zu zerlegen.
Das Verständnis dieses grundlegenden Unterschieds in Prozess und Zweck ist der Schlüssel zur Auswahl der richtigen Technologie für Ihr spezifisches Energie- oder Materialziel.
Zusammenfassungstabelle:
| Merkmal | Vergasung | Pyrolyse |
|---|---|---|
| Sauerstoffgehalt | Begrenzte, kontrollierte Menge | Vollständige Abwesenheit |
| Hauptprodukt | Synthesegas (H₂ + CO) | Bio-Öl, Biokohle und Synthesegas |
| Prozessziel | Maximierung des gasförmigen Brennstoffs für sofortige Strom-/Wärmeerzeugung | Herstellung vielfältiger, lagerfähiger Produkte |
| Am besten geeignet für | Direkte Strom- und Wärmeerzeugung | Lagerfähige flüssige Brennstoffe und Bodenverbesserer (Biokohle) |
Bereit, die richtige Biomasseumwandlungstechnologie für Ihr Labor oder Ihr Pilotprojekt auszuwählen? Die Wahl zwischen Vergasung und Pyrolyse ist entscheidend für das Erreichen Ihrer Energie- und Materialziele. KINTEK ist spezialisiert auf die Bereitstellung hochwertiger Laborgeräte und Verbrauchsmaterialien für beide Prozesse. Unsere Experten können Ihnen helfen, Ihr System für optimale Leistung zu entwerfen und auszustatten. Kontaktieren Sie unser Team noch heute, um Ihre spezifischen Anforderungen zu besprechen und herauszufinden, wie KINTEK Ihre Innovationen in den Bereichen erneuerbare Energien und Materialien unterstützen kann.
Visuelle Anleitung