Die Veraschung ist ein grundlegender Prozess in der analytischen Chemie, der verwendet wird, um organische Materialien aus einer Probe zu entfernen, wobei anorganische, nicht brennbare Asche für die weitere Analyse zurückbleibt. Diese Technik ist entscheidend für die Vorkonzentration von Spurensubstanzen und die Bestimmung der elementaren Zusammensetzung. Der Prozess beinhaltet das Erhitzen einer Probe in Gegenwart von Sauerstoff, wodurch organische Verbindungen verbrennen und oxidieren, während anorganische Rückstände als Asche verbleiben. Die Veraschung wird in Branchen wie der Lebensmittel-, Erdöl- und Umweltprüfung weit verbreitet eingesetzt und kann durch internationale Standards wie ISO, EN oder ASTM geregelt werden. Die resultierende Asche kann mittels Techniken wie Chromatographie oder Spektroskopie analysiert werden, um die elementare Zusammensetzung der Probe zu bestimmen.

Wichtige Punkte erklärt:
-
Definition und Zweck der Veraschung:
- Die Veraschung ist der Prozess des Erhitzens einer Probe, um organische Materialien zu entfernen und anorganische Asche zurückzulassen.
- Der Hauptzweck besteht darin, Spurensubstanzen für die chemische oder optische Analyse, wie Chromatographie oder Spektroskopie, vorzukonzentrieren.
- Sie wird in Branchen wie der Lebensmittel-, Erdöl- und Umweltprüfung eingesetzt, um die elementare Zusammensetzung zu bestimmen.
-
Mechanismus der Veraschung:
- Die Probe wird in Gegenwart von Sauerstoff erhitzt, wodurch organische Verbindungen verbrennen und oxidieren.
- Dieser Oxidationsprozess zersetzt organische Materialien in Gase (z. B. CO₂ und H₂O) und hinterlässt anorganische Rückstände (Asche).
- Die Asche besteht aus nicht brennbaren Verbindungen wie Metalloxiden, Salzen und Mineralien, die auf ihre elementare Zusammensetzung analysiert werden können.
-
Arten der Veraschung:
- Trockenveraschung: Beinhaltet das Erhitzen der Probe in einem Muffelofen bei hohen Temperaturen (typischerweise 500–600 °C) in Gegenwart von Luft. Diese Methode ist langsamer, aber für viele Probenarten geeignet.
- Nassveraschung: Verwendet starke Säuren (z. B. Salpetersäure oder Schwefelsäure), um organisches Material bei niedrigeren Temperaturen (etwa 350 °C) zu oxidieren. Diese Methode ist schneller und wird häufig für Lebensmittelproben verwendet.
- Beide Methoden zielen darauf ab, eine vollständige Verbrennung des organischen Materials zu erreichen, aber die Wahl hängt von der Probenart und den Analyseanforderungen ab.
-
Anwendungen der Veraschung:
- Lebensmittelindustrie: Wird zur Bestimmung des Aschegehalts verwendet, der den Mineralstoffgehalt in Lebensmitteln anzeigt.
- Erdölindustrie: Hilft bei der Analyse der anorganischen Rückstände in Kraftstoffen und Schmierstoffen.
- Umweltprüfung: Wird zur Beurteilung des Mineralstoffgehalts in Boden-, Wasser- und Luftproben verwendet.
- Pharmazie: Stellt die Reinheit von Rohstoffen und Endprodukten durch Analyse anorganischer Rückstände sicher.
-
Standards und Protokolle:
- Veraschungsprozesse werden häufig durch internationale Standards wie ISO, EN oder ASTM geregelt.
- Diese Standards definieren spezifische Verfahren, einschließlich Temperaturbereichen, Heizdauern und Probenvorbereitungsmethoden.
- Beispielsweise ist die Glühverlustbestimmung (Loss on Ignition, LOI) ein gängiges Protokoll, bei dem Proben vor und nach der Veraschung gewogen werden, um die Massenreduzierung zu bestimmen.
-
Vorteile der Veraschung:
- Entfernt unerwünschtes organisches Material und vereinfacht die Analyse anorganischer Komponenten.
- Liefert eine konzentrierte Probe von Spurenelementen und verbessert die Empfindlichkeit nachfolgender Analysetechniken.
- Kann auf eine breite Palette von Probenarten angewendet werden, von Feststoffen bis zu Flüssigkeiten.
-
Einschränkungen und Überlegungen:
- Hohe Temperaturen bei der Trockenveraschung können zur Verflüchtigung bestimmter Elemente führen, was zu ungenauen Ergebnissen führt.
- Die Nassveraschung ist zwar schneller, erfordert jedoch einen sorgfältigen Umgang mit ätzenden Säuren und eine ordnungsgemäße Entsorgung chemischer Abfälle.
- Bei der Wahl der Veraschungsmethode müssen die Eigenschaften der Probe und die interessierenden Elemente berücksichtigt werden.
-
Praktisches Beispiel: Nassveraschung in der Lebensmittelanalyse:
- Eine Lebensmittelprobe wird bei 350 °C in Gegenwart von Säuren erhitzt, bis das organische Material vollständig oxidiert ist.
- Die verbleibende Asche wird gewogen und der Aschegehalt basierend auf der Gewichtsänderung vor und nach dem Prozess berechnet.
- Diese Methode ist besonders nützlich zur Bestimmung des Mineralstoffgehalts in Lebensmitteln wie Getreide, Milchprodukten und Getränken.
Durch das Verständnis der Prinzipien und Anwendungen der Veraschung können Analysten Proben effektiv für eine genaue Elementaranalyse vorbereiten und so zuverlässige Ergebnisse in verschiedenen Branchen gewährleisten.
Zusammenfassungstabelle:
| Aspekt | Details |
|---|---|
| Definition | Erhitzen einer Probe zur Entfernung organischer Materialien, wobei anorganische Asche zurückbleibt. |
| Zweck | Vorkonzentration von Spurensubstanzen für die chemische oder optische Analyse. |
| Typen | Trockenveraschung (500–600 °C) und Nassveraschung (350 °C mit Säuren). |
| Anwendungen | Lebensmittel, Erdöl, Umweltprüfung, Pharmazie. |
| Standards | ISO, EN, ASTM (z. B. Glühverlustprotokoll). |
| Vorteile | Vereinfacht die anorganische Analyse, verbessert die Empfindlichkeit, vielseitige Anwendung. |
| Einschränkungen | Risiko der Verflüchtigung bei der Trockenveraschung; Umgang mit Säuren bei der Nassveraschung. |
Benötigen Sie Hilfe bei Veraschungstechniken für Ihr Labor? Kontaktieren Sie noch heute unsere Experten für maßgeschneiderte Lösungen!
Visuelle Anleitung
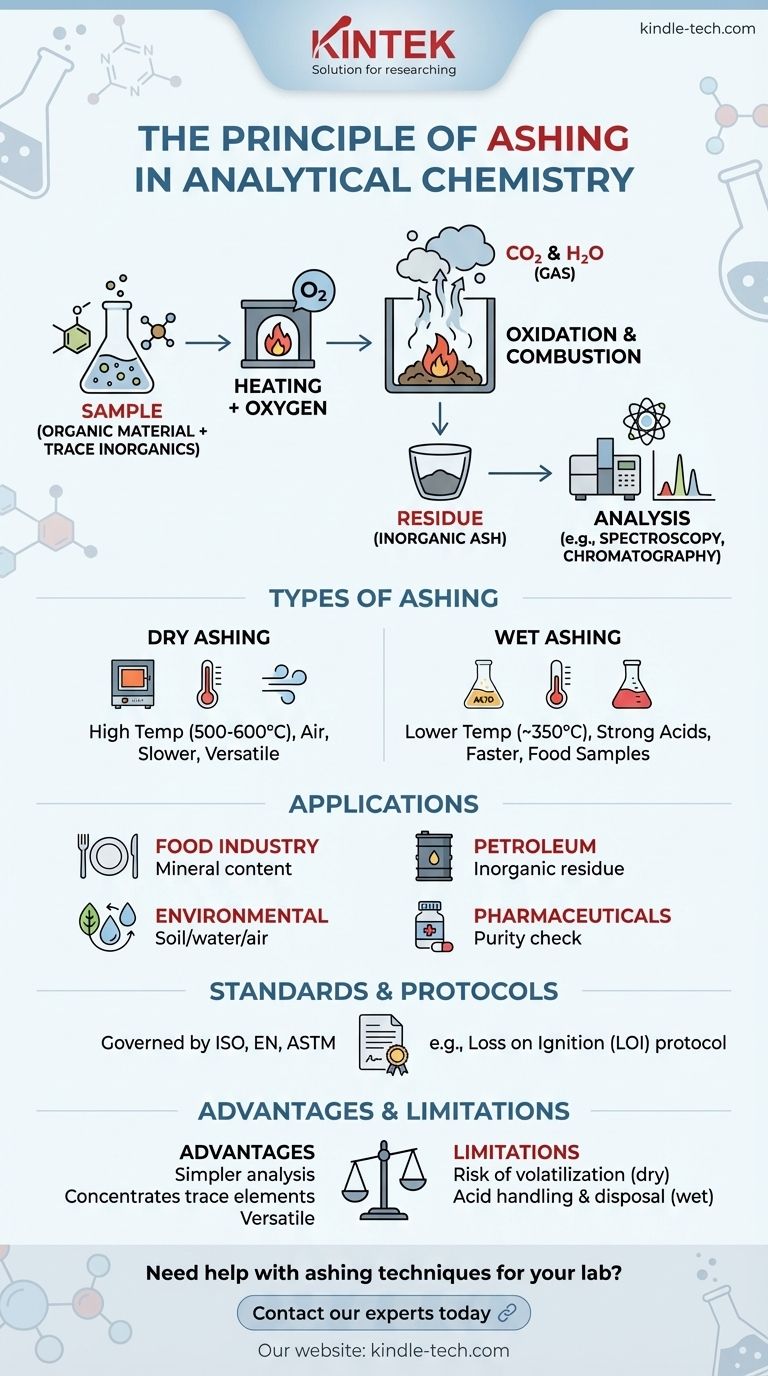
Ähnliche Produkte
- 1200℃ Muffelofen für Labor
- 1800℃ Muffelofen für Labor
- 1400℃ Muffelofen für Labor
- 1700℃ Muffelofen für Labor
- Hochtemperatur-Muffelofen für Laborentbinderung und Vorsintern
Andere fragen auch
- Was ist der Zweck des Kalzinierungsschritts bei 1473 K? Optimieren Sie Ihre Herstellung von Magnesium-Aluminium-Spinell
- Warum wird ein Hochtemperatur-Muffelofen für die Kalzinierung von Ni-Ag-Katalysatorvorläufern verwendet? Aktivität optimieren
- Wie wird ein Labor-Hochtemperatur-Muffelofen bei der Sol-Gel-Synthese für Perowskit-Katalysatoren eingesetzt?
- Wie beeinflusst ein Muffelofen die Verdichtung von 8YSZ-Keramik? Meisterung der Präzisionssinterung bei 1500°C
- Wie funktioniert ein Hochtemperatur-Muffelofen? Erreicht kontaminationsfreie, gleichmäßige Erwärmung



















