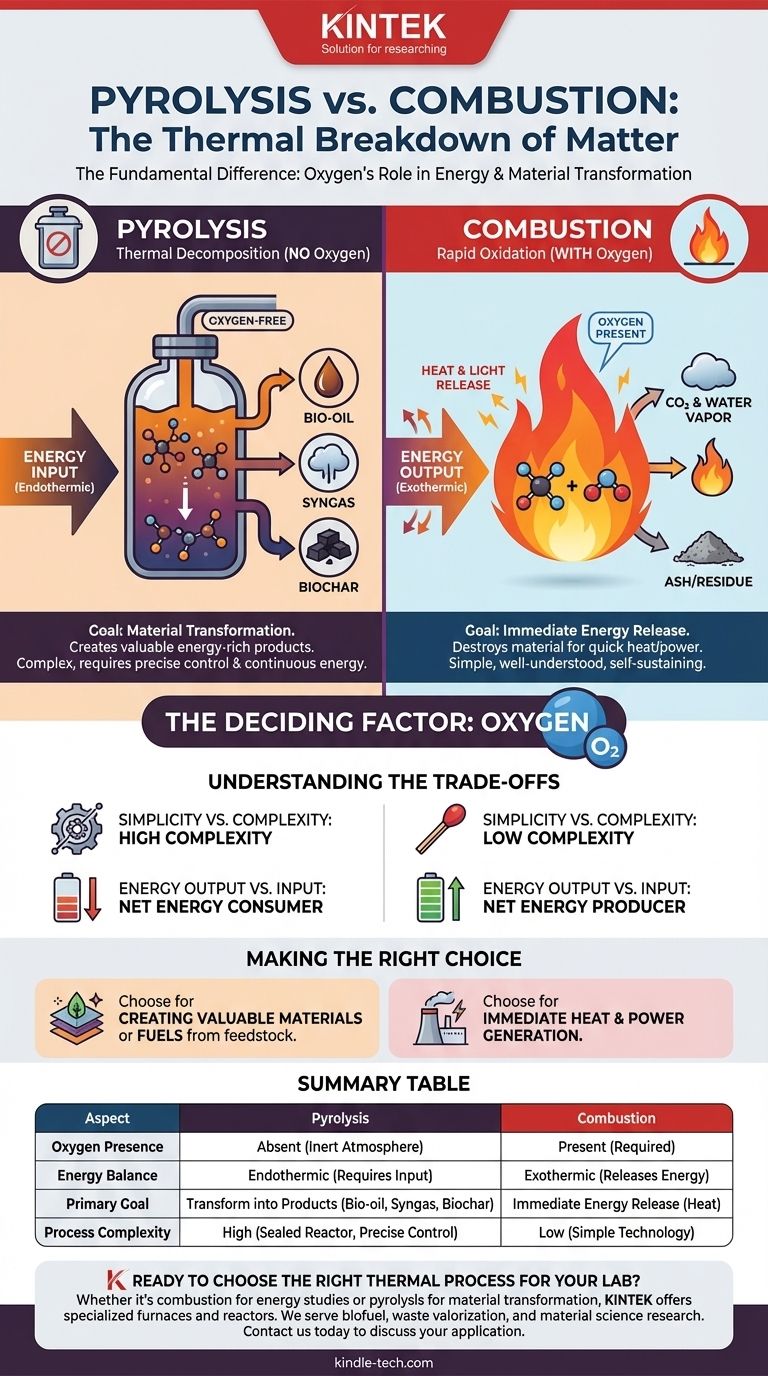
Im Kern sind Pyrolyse und Verbrennung zwei grundlegend unterschiedliche Arten, Materie durch Hitze abzubauen. Der entscheidende Unterschied liegt in der Anwesenheit oder Abwesenheit von Sauerstoff. Die Verbrennung ist ein schneller Oxidationsprozess – im Wesentlichen das Brennen –, der Energie freisetzt, während die Pyrolyse ein thermischer Zersetzungsprozess ist, der in einer sauerstofffreien Umgebung stattfindet und eine Energiezufuhr erfordert.
Der wichtigste Unterschied ist der Sauerstoff. Die Verbrennung nutzt Sauerstoff, um die Energie eines Materials schnell als Wärme freizusetzen, während die Pyrolyse Hitze in einer sauerstofffreien Umgebung nutzt, um ein Material in neue, energiereiche Produkte zu zerlegen.

Die Rolle des Sauerstoffs: Der entscheidende Faktor
Die Anwesenheit oder Abwesenheit von Sauerstoff verändert die chemischen Reaktionen, die Energiebilanz und die Endprodukte des thermischen Prozesses vollständig.
Verbrennung: Eine Reaktion mit Sauerstoff
Verbrennung ist das, was wir allgemein als Brennen kennen. Es ist ein exothermer Prozess, was bedeutet, dass er mehr Energie freisetzt, als er verbraucht, typischerweise in Form von Wärme und Licht.
Dieser Prozess beinhaltet die schnelle Reaktion eines Brennstoffs mit einem Oxidationsmittel, was fast immer der Sauerstoff in der Luft ist. Die Ergebnisse sind typischerweise einfache, energiemindernde Moleküle wie Kohlendioxid und Wasser sowie Aschereste.
Pyrolyse: Eine Zersetzung ohne Sauerstoff
Pyrolyse ist die thermische Zersetzung von Materialien bei hohen Temperaturen in einer inerten oder sauerstofffreien Atmosphäre. Da kein Sauerstoff vorhanden ist, mit dem es reagieren könnte, verbrennt das Material nicht.
Stattdessen bricht die Hitze die komplexen chemischen Bindungen des Ausgangsmaterials auf und wandelt es in eine Mischung kleinerer, oft wertvollerer Moleküle um. Dies ist ein endothermer Prozess, was bedeutet, dass er eine kontinuierliche Energiezufuhr benötigt, um die Reaktion aufrechtzuerhalten.
Analyse des Prozesses und seiner Produkte
Das Ziel jedes Prozesses bestimmt den Wert seiner Ergebnisse. Das eine zielt darauf ab, Energie sofort freizusetzen, während das andere darauf abzielt, sie in neuen Formen zu speichern.
Das Ziel der Verbrennung: Sofortige Energiefreisetzung
Der Hauptzweck der Verbrennung ist die schnellstmögliche Extraktion der gespeicherten chemischen Energie aus einem Brennstoff in Form von nutzbarer Wärme.
Die Nebenprodukte, wie Asche und Rauchgase, gelten im Allgemeinen als minderwertige Abfallprodukte, die entsorgt werden müssen. Das ursprüngliche Material wird effektiv zerstört, um seine Energie freizusetzen.
Das Ziel der Pyrolyse: Materialtransformation
Der Hauptzweck der Pyrolyse ist die Umwandlung eines minderwertigen Ausgangsmaterials in höherwertige Produkte. Sie ordnet die chemische Struktur des Materials neu an, anstatt nur seine Energie freizusetzen.
Die Produkte der Pyrolyse – typischerweise eine flüssige Bio-Öl, ein brennbares Gas (Synthesegas) und ein fester Kohlenstoffrückstand (Biochar) – behalten alle einen erheblichen Energiegehalt und haben verschiedene industrielle Anwendungen.
Die Abwägungen verstehen
Die Wahl zwischen diesen Prozessen beinhaltet das Verständnis ihrer inhärenten Komplexitäten und Energieanforderungen.
Einfachheit vs. Komplexität
Die Verbrennung ist eine relativ einfache und gut verstandene Technologie. Um ein Feuer zu erzeugen, werden nur Brennstoff, Sauerstoff und eine Zündquelle benötigt.
Die Pyrolyse ist weitaus komplexer. Sie erfordert einen versiegelten Reaktor, um eine sauerstofffreie Umgebung zu gewährleisten, sowie eine präzise Temperaturkontrolle, was die Ausrüstung spezialisierter und teurer macht.
Energieabgabe vs. Energieeinsatz
Die Verbrennung ist ein Netto-Energieerzeuger. Sobald die exotherme Reaktion begonnen hat, erhält sie sich selbst aufrecht und setzt überschüssige Energie frei.
Die Pyrolyse ist ein Netto-Energieverbraucher. Der endotherme Prozess erfordert eine konstante und erhebliche externe Wärmequelle, um das Ausgangsmaterial abzubauen. Die Energie geht nicht verloren, sondern wird in den chemischen Bindungen der neuen Produkte gespeichert.
Die richtige Wahl für Ihr Ziel treffen
Letztendlich hängt die Wahl zwischen Verbrennung und Pyrolyse vollständig davon ab, was Sie mit einem bestimmten Material erreichen möchten.
- Wenn Ihr Hauptaugenmerk auf der sofortigen Wärme- und Stromerzeugung liegt: Die Verbrennung ist die direkteste und etablierteste Methode zur Freisetzung der gespeicherten Energie eines Brennstoffs.
- Wenn Ihr Hauptaugenmerk auf der Herstellung wertvoller neuer Materialien oder Kraftstoffe aus einem Ausgangsmaterial liegt: Die Pyrolyse ist der notwendige Prozess zur Umwandlung von Materie in energiedichte Öle, Gase und Kohlenstoff.
Das Verständnis der grundlegenden Rolle des Sauerstoffs ist der Schlüssel zur Auswahl des richtigen thermischen Prozesses, um Ihr spezifisches Energie- oder Materialziel zu erreichen.
Zusammenfassungstabelle:
| Aspekt | Pyrolyse | Verbrennung |
|---|---|---|
| Sauerstoffpräsenz | Abwesend (inerte Atmosphäre) | Anwesend (zum Brennen erforderlich) |
| Energiebilanz | Endotherm (erfordert Energiezufuhr) | Exotherm (setzt Energie frei) |
| Hauptziel | Umwandlung des Ausgangsmaterials in wertvolle Produkte (Bio-Öl, Synthesegas, Biochar) | Sofortige Freisetzung von Energie in Form von Wärme |
| Prozesskomplexität | Hoch (erfordert versiegelten Reaktor, präzise Temperaturkontrolle) | Gering (relativ einfache Technologie) |
Bereit, den richtigen thermischen Prozess für Ihr Labor auszuwählen?
Ob Sie zuverlässige Verbrennungsgeräte für Energiestudien oder fortschrittliche Pyrolyseöfen für die Materialumwandlung benötigen, KINTEK hat die Lösung. Unsere spezialisierten Laborgeräte, einschließlich Öfen und Reaktoren, sind auf Präzision, Sicherheit und Reproduzierbarkeit ausgelegt.
Wir bedienen Labore, die sich konzentrieren auf:
- Forschung zu Biokraftstoffen und erneuerbaren Energien
- Studien zur Wertschöpfung und zum Recycling von Abfällen
- Materialwissenschaft und chemische Analyse
Kontaktieren Sie uns noch heute, um Ihre spezifische Anwendung zu besprechen. Unsere Experten helfen Ihnen bei der Auswahl der idealen Ausrüstung, um Ihre Forschungs- oder Produktionsziele zu erreichen.
Visuelle Anleitung