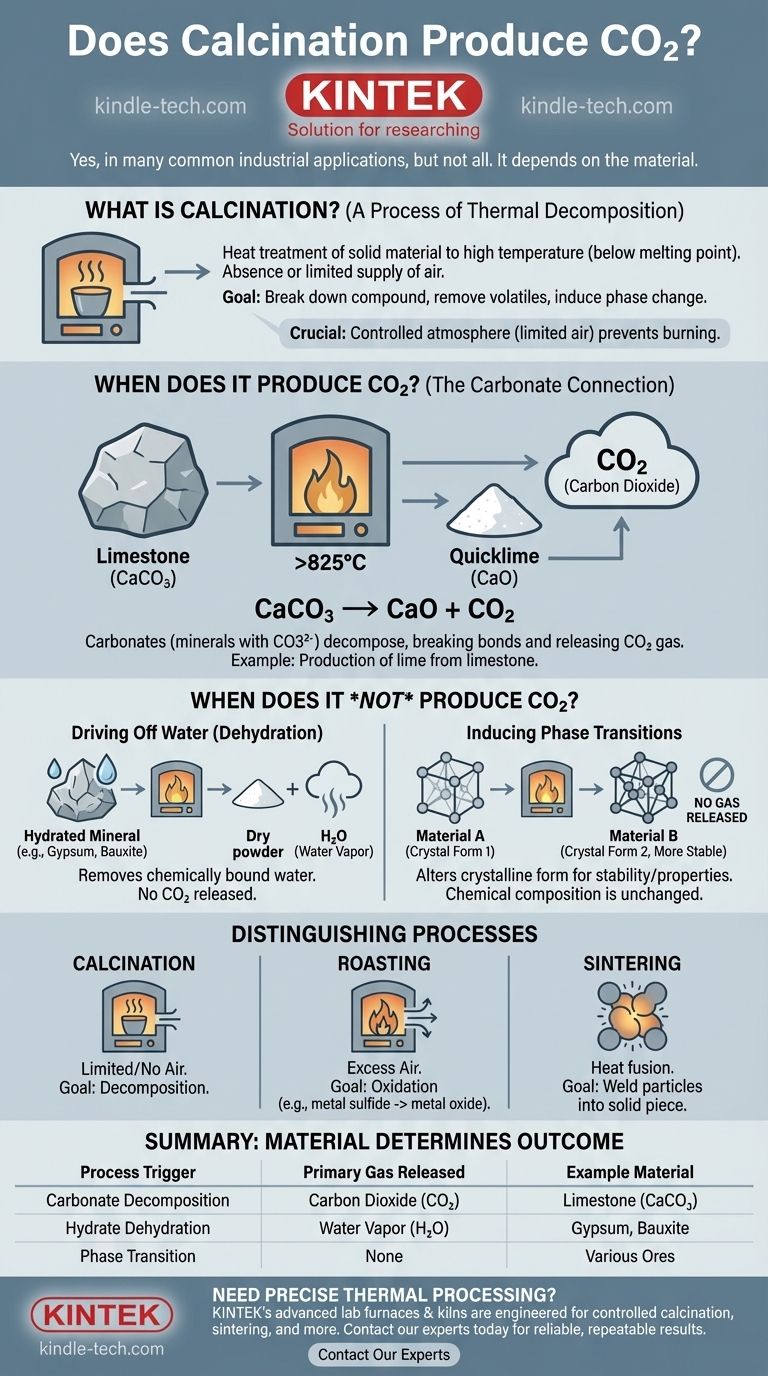
In vielen gängigen industriellen Anwendungen: Ja. Kalzinierung ist ein Erhitzungsprozess, und wenn er auf karbonathaltige Materialien wie Kalkstein angewendet wird, führt er zu einem chemischen Zerfall, bei dem erhebliche Mengen Kohlendioxid (CO2) freigesetzt werden. Die Herstellung von Kalk aus Kalkstein ist ein Paradebeispiel für diese Reaktion.
Der entscheidende Punkt ist, dass Kalzinierung ein Prozess ist, keine einzelne spezifische Reaktion. Ob dabei CO2 entsteht, hängt ausschließlich von der chemischen Zusammensetzung des erhitzten Materials ab.

Was ist Kalzinierung im Grunde?
Ein Prozess der thermischen Zersetzung
Kalzinierung ist ein Wärmebehandlungsprozess, bei dem ein festes Material auf eine hohe Temperatur, aber unterhalb seines Schmelzpunktes, erhitzt wird. Dies geschieht in Abwesenheit oder mit einer sehr begrenzten Zufuhr von Luft.
Der Hauptzweck besteht darin, eine thermische Zersetzung herbeizuführen, was bedeutet, die Verbindung durch Hitze abzubauen.
Das Ziel: Veränderung herbeiführen
Das Ziel der Kalzinierung ist nicht immer dasselbe. Sie kann verwendet werden, um:
- Eine flüchtige Substanz zu entfernen, wie CO2 aus Kalkstein oder Wasser aus einem hydratisierten Mineral.
- Verunreinigungen aus einem Erz zu entfernen.
- Einen Phasenübergang zu verursachen, der die Kristallstruktur und die Eigenschaften des Materials verändert.
Die Rolle der Atmosphäre
Die kontrollierte Atmosphäre (begrenzte Luftzufuhr) ist entscheidend. Sie verhindert, dass das Material verbrennt oder oxidiert, was die Kalzinierung von anderen Wärmebehandlungen wie dem Rösten unterscheidet.
Wann entsteht bei der Kalzinierung CO2?
Die Karbonat-Verbindung
Bei der Kalzinierung entsteht Kohlendioxid, wenn das Ausgangsmaterial ein Karbonat ist. Karbonate sind Mineralien, die das Karbonat-Ion (CO3²⁻) enthalten.
Beim Erhitzen zersetzen sich diese Mineralien, brechen ihre chemischen Bindungen auf und setzen die Kohlenstoff- und Sauerstoffatome als CO2-Gas frei.
Beispiel: Herstellung von Kalk aus Kalkstein
Das klassischste Beispiel ist die Kalzinierung von Kalkstein (Calciumcarbonat, CaCO₃).
Beim Erhitzen auf über 825 °C (1517 °F) zersetzt es sich zu Calciumoxid (CaO), auch bekannt als Branntkalk, und setzt Kohlendioxid frei. Die chemische Reaktion lautet: CaCO₃ → CaO + CO₂.
Andere Karbonaterze
Dieses Prinzip gilt auch für andere Karbonaterze wie Magnesit (MgCO₃) oder Dolomit (CaMg(CO₃)₂), die beim Erhitzen ebenfalls CO2 freisetzen.
Wann entsteht bei der Kalzinierung kein CO2?
Entfernung von Wasser (Dehydrierung)
Viele Mineralien werden kalziniert, um einfach Wasser (H₂O) zu entfernen, das chemisch in ihrer Kristallstruktur gebunden ist.
Zum Beispiel setzen die Kalzinierung von Bauxiterz zur Herstellung von Aluminiumoxid oder das Erhitzen von Gips zur Herstellung von Gipsputz Wasserdampf und kein Kohlendioxid frei.
Herbeiführen von Phasenübergängen
Manchmal wird ein Material einfach kalziniert, um seine kristalline Form zu verändern. Dies kann es stabiler, reaktiver oder ihm andere physikalische Eigenschaften verleihen.
In diesen Fällen ändert sich die chemische Zusammensetzung nicht, und es werden keine Gase freigesetzt.
Abgrenzung der Kalzinierung von ähnlichen Prozessen
Kalzinierung vs. Rösten
Rösten ist das Erhitzen eines Erzes in Anwesenheit von überschüssiger Luft. Sein Ziel ist typischerweise die Oxidation, wie die Umwandlung eines Metallsulfids in ein Metalloxid. Kalzinierung erfolgt in begrenzter oder keiner Luft, um eine Zersetzung zu bewirken.
Kalzinierung vs. Sintern
Sintern verwendet Wärme, um kleine Partikel zu einem einzigen, festen Stück zu verschmelzen, oft nachdem Verunreinigungen bereits entfernt wurden. Kalzinierung zerlegt ein Material; Sintern schweißt es zusammen.
Die richtige Wahl für Ihr Ziel treffen
Das Verständnis des Ausgangsmaterials ist der Schlüssel zur Vorhersage des Ergebnisses.
- Wenn Ihr Material ein Karbonat ist (wie Kalkstein oder Dolomit): Erwarten Sie eine signifikante CO2-Produktion als primäres Ergebnis des Prozesses.
- Wenn Ihr Material ein Hydrat ist (wie Bauxit oder Gips): Die primäre Emission wird Wasserdampf (Dampf) sein, kein CO2.
- Wenn Ihr Ziel darin besteht, die Kristallstruktur eines Materials zu ändern: Der Prozess setzt möglicherweise überhaupt keine Gase frei.
Letztendlich ist die Kalzinierung ein vielseitiges Werkzeug, das durch Hitze und eine kontrollierte Atmosphäre definiert wird, während ihre spezifischen Ergebnisse von der Chemie bestimmt werden.
Zusammenfassungstabelle:
| Prozessauslöser | Primär freigesetztes Gas | Beispielmaterial |
|---|---|---|
| Karbonatzersetzung | Kohlendioxid (CO₂) | Kalkstein (CaCO₃) |
| Hydrat-Dehydrierung | Wasserdampf (H₂O) | Gips, Bauxit |
| Phasenübergang | Keine | Verschiedene Erze |
Benötigen Sie präzise thermische Verarbeitung für Ihre Materialien? Die fortschrittlichen Laboröfen und -brennöfen von KINTEK sind für kontrollierte Kalzinierung, Sintern und mehr konzipiert. Egal, ob Sie Karbonate, Hydrate oder andere Materialien verarbeiten, unsere Geräte gewährleisten eine genaue Temperaturregelung und Atmosphärenmanagement für zuverlässige, wiederholbare Ergebnisse. Kontaktieren Sie noch heute unsere Experten, um die perfekte thermische Lösung für die spezifischen Anforderungen Ihres Labors zu finden.
Visuelle Anleitung
Ähnliche Produkte
- Elektrische Drehrohrofen-Pyrolyseofenanlage Kalzinator Kleiner Drehrohrofen Rotierender Ofen
- Elektrischer Drehrohrofen Kontinuierlicher Betrieb Kleine Drehrohrofen Heizpyrolyseanlage
- Vertikaler Hochtemperatur-Graphit-Vakuum-Graphitierungs-Ofen
- Graphit-Vakuumofen Hochwärmeleitfähige Folien-Graphitierungsöfen
- Graphitierungs-Vakuumofen für ultrahohe Temperaturen
Andere fragen auch
- Bei welcher Temperatur findet die Pyrolyse statt? Ein Leitfaden zur Steuerung Ihres Produktausstoßes
- Wie hoch ist der Wirkungsgrad eines Drehrohrofens? Erreichen Sie einen thermischen Wirkungsgrad von über 95 %
- Was sind die Merkmale der Gleit-, Einsink- und Rollbewegungsmodi von Schüttgütern? Optimieren Sie Ihren Drehprozess
- Wie werden Drehrohröfen beheizt? Erklärung der direkten vs. indirekten Heizmethoden
- Ist ein Drehrohrofen ein Ofen? Entdecken Sie die Hauptunterschiede für die industrielle Verarbeitung



















