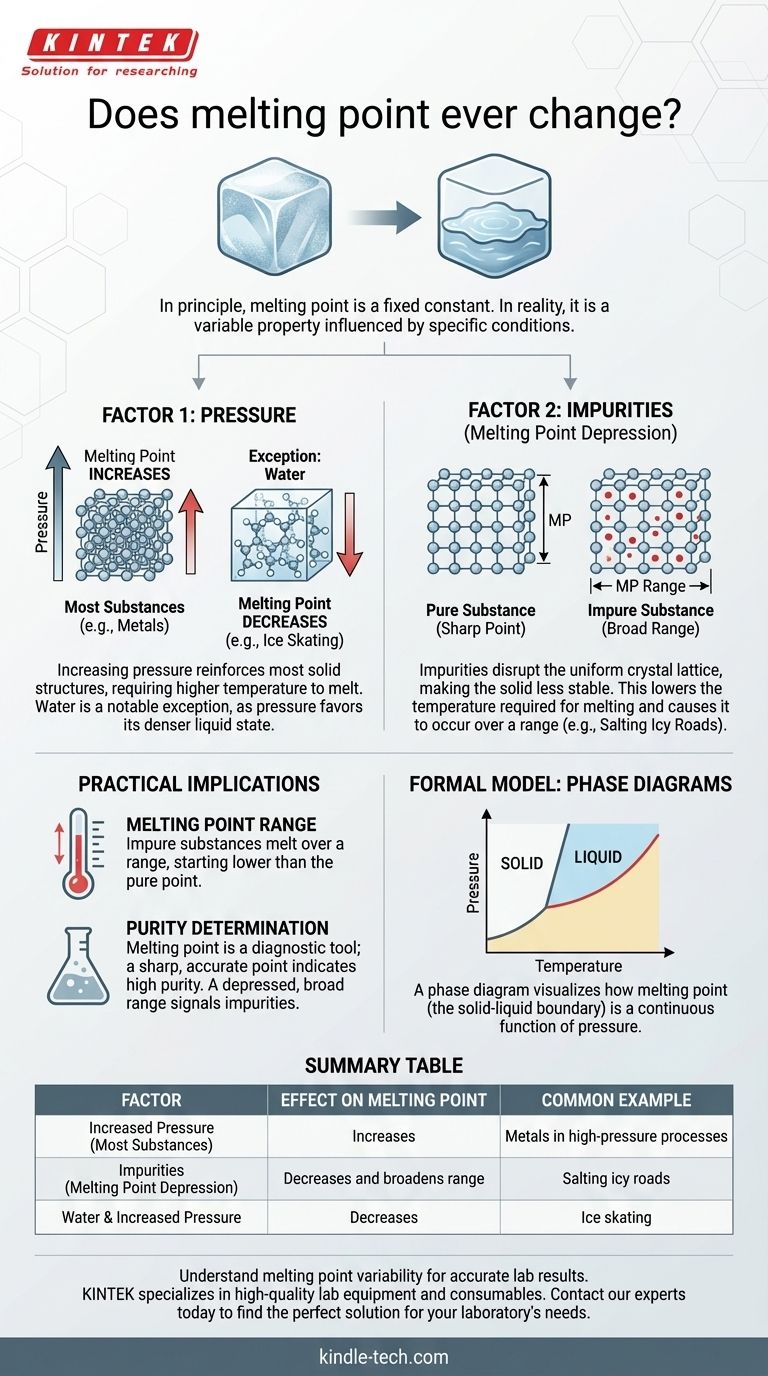
Im Prinzip ist der Schmelzpunkt einer reinen Substanz eine feste physikalische Konstante. In der realen Welt kann sich die beobachtete Temperatur, bei der eine Substanz schmilzt, jedoch absolut ändern. Dies ist keine willkürliche Verschiebung; es ist eine vorhersagbare Reaktion auf zwei Hauptfaktoren: Änderungen des Umgebungsdrucks und das Einbringen von Verunreinigungen in die Substanz.
Obwohl Lehrbücher den Schmelzpunkt oft als eine statische Zahl darstellen, versteht man ihn genauer als eine Eigenschaft, die nur unter bestimmten Bedingungen konstant ist. Zu verstehen, wie Druck und Reinheit diese Eigenschaft beeinflussen, ist der Schlüssel zur Vorhersage und Steuerung ihres Verhaltens in jeder realen Anwendung.

Die beiden Faktoren, die den Schmelzpunkt verändern
Der „offizielle“ Schmelzpunkt einer Substanz, wie Wasser bei 0 °C (32 °F), wird unter Standardbedingungen gemessen – typischerweise bei einem Druck von einer Atmosphäre und wenn die Substanz in einem hochreinen Zustand vorliegt. Wenn diese Bedingungen nicht erfüllt sind, weicht der Schmelzpunkt ab.
Faktor 1: Der Einfluss des Drucks
Bei den meisten Substanzen zwingt eine Erhöhung des äußeren Drucks die Moleküle in eine dichtere Anordnung. Dies verstärkt die feste Struktur, sodass mehr Energie (eine höhere Temperatur) erforderlich ist, um die Bindungen zu brechen und in eine Flüssigkeit überzugehen.
Daher führt bei der überwiegenden Mehrheit der Materialien eine Druckerhöhung zu einer Erhöhung des Schmelzpunkts.
Es gibt jedoch eine kritische und berühmte Ausnahme: Wasser. Festes Wasser (Eis) ist weniger dicht als flüssiges Wasser, weshalb Eisberge schwimmen. Eine Druckerhöhung auf Eis begünstigt den dichteren Zustand – flüssiges Wasser. Das bedeutet, dass Eis unter höherem Druck bei einer niedrigeren Temperatur schmilzt. Deshalb kann die Klinge eines Schlittschuhs durch Ausübung hohen Drucks auf einer dünnen Linie eine mikroskopische Wasserschicht erzeugen, auf der sie gleiten kann.
Faktor 2: Die Rolle von Verunreinigungen
Dies ist der häufigste Grund für eine Änderung des Schmelzpunkts außerhalb eines Hochdrucklabors. Wenn Sie eine Verunreinigung (ein gelöstes Teilchen) in eine reine Substanz (ein Lösungsmittel) einbringen, stört dies das gleichmäßige, sich wiederholende Kristallgitter des Festkörpers.
Diese Störung macht die feste Struktur weniger stabil. Infolgedessen wird weniger Energie benötigt, um sie aufzubrechen und in eine Flüssigkeit umzuwandeln. Dieses Phänomen wird als Schmelzpunkterniedrigung bezeichnet.
Ein klassisches Beispiel ist das Salzen vereister Straßen. Das Salz vermischt sich mit dem Eis und senkt dessen Schmelzpunkt. Dadurch kann das Eis schmelzen, selbst wenn die Umgebungstemperatur noch unter dem normalen Gefrierpunkt von Wasser liegt.
Verständnis der praktischen Auswirkungen
Die Erkenntnis, dass sich der Schmelzpunkt ändern kann, ist nicht nur eine akademische Übung. Sie hat erhebliche Auswirkungen in wissenschaftlichen und industriellen Umgebungen, wo sie oft als Diagnosewerkzeug eingesetzt wird.
Von einem „Punkt“ zu einem „Bereich“
Ein reiner kristalliner Feststoff schmilzt typischerweise bei einer sehr scharfen, spezifischen Temperatur. Wenn Sie beginnen, ihn zu erhitzen, steigt die Temperatur, bis sie den Schmelzpunkt erreicht, wo sie konstant bleibt, bis das gesamte Feststoff in Flüssigkeit übergegangen ist.
Eine unreine Substanz verhält sich anders. Sie schmilzt nicht bei einer einzigen Temperatur, sondern über einen Schmelzpunktbereich. Das Schmelzen beginnt bei einer niedrigeren Temperatur als bei der reinen Substanz und endet bei einer Temperatur, die näher am Schmelzpunkt der reinen Substanz liegt, aber oft immer noch darunter.
Verwendung des Schmelzpunkts zur Bestimmung der Reinheit
Dieser „Fehler“ ist tatsächlich ein unglaublich nützliches Merkmal. In einem Chemielabor ist eine der ersten und schnellsten Methoden zur Beurteilung der Reinheit einer synthetisierten kristallinen Verbindung die Messung ihres Schmelzpunkts.
Wenn die Verbindung über einen weiten Bereich und bei einer niedrigeren Temperatur als dem Literaturwert schmilzt, ist dies ein klares Zeichen dafür, dass Verunreinigungen vorhanden sind und eine weitere Reinigung erforderlich ist. Ein scharfer Schmelzpunkt, der mit dem etablierten Wert übereinstimmt, ist ein starker Indikator für hohe Reinheit.
Das formale Modell: Phasendiagramme
Die Beziehung zwischen Druck, Temperatur und dem Zustand einer Substanz (fest, flüssig, gasförmig) wird formal in einem Phasendiagramm erfasst.
Eine Karte der Aggregatzustände
Ein Phasendiagramm ist ein Diagramm mit dem Druck auf der y-Achse und der Temperatur auf der x-Achse. Linien im Diagramm grenzen die Grenzen ab, an denen die Substanz zwischen verschiedenen Phasen übergeht.
Die Fest-Flüssig-Grenze
Die Linie, die die feste Phase von der flüssigen Phase in diesem Diagramm trennt, stellt den Schmelzpunkt bei jedem möglichen Druck dar. Die Betrachtung dieses Diagramms macht sofort klar, dass der Schmelzpunkt keine einzelne Zahl ist, sondern eine kontinuierliche Funktion des Drucks. Dieses visuelle Modell vereint die Konzepte und beweist, dass der Schmelzpunkt von Natur aus variabel ist.
Die richtige Wahl für Ihr Ziel treffen
Ihre Sichtweise auf den Schmelzpunkt sollte von Ihrem Ziel bestimmt werden.
- Wenn Ihr Hauptaugenmerk auf chemischer Synthese oder Analyse liegt: Betrachten Sie den Schmelzpunkt als ein entscheidendes Diagnosewerkzeug für die Reinheit. Ein scharfer, genauer Schmelzpunkt bestätigt den Erfolg, während ein erniedrigter, breiter Bereich auf die Notwendigkeit einer Reinigung hinweist.
- Wenn Ihr Hauptaugenmerk auf Materialwissenschaft oder Ingenieurwesen liegt: Sie müssen Druckschwankungen in Ihren Konstruktionen berücksichtigen. Der Schmelzpunkt eines Materials auf Meereshöhe ist möglicherweise nicht derselbe in einem Hochdruck-Industrieprozess oder bei Tiefenerdanwendungen.
- Wenn Ihr Hauptaugenmerk auf dem Verständnis alltäglicher Phänomene liegt: Nutzen Sie das Prinzip der Schmelzpunkterniedrigung, um zu erklären, warum wir im Winter Straßen salzen oder warum das Hinzufügen von Salz zu einem Eis-Wasser-Bad es kälter macht, um Eiscreme zu kurbeln.
Letztendlich verwandelt die Erkenntnis, dass der Schmelzpunkt eine dynamische Eigenschaft und keine statische Zahl ist, ihn von einer einfachen Tatsache in ein mächtiges Vorhersagewerkzeug.
Zusammenfassungstabelle:
| Faktor | Auswirkung auf den Schmelzpunkt | Häufiges Beispiel |
|---|---|---|
| Erhöhter Druck | Erhöht (für die meisten Substanzen) | Metalle in Hochdruckprozessen |
| Verunreinigungen (Schmelzpunkterniedrigung) | Verringert und verbreitert den Bereich | Salzen von vereisten Straßen |
| Wasser & Erhöhter Druck | Verringert | Schlittschuhlaufen |
Benötigen Sie eine präzise Temperaturkontrolle für Ihre Laborarbeit?
Das Verständnis der Schmelzpunktvariabilität ist entscheidend für eine genaue Synthese und Analyse. KINTEK ist spezialisiert auf hochwertige Laborgeräte und Verbrauchsmaterialien, einschließlich Schmelzpunktapparate, die auf die Zuverlässigkeit und Präzision ausgelegt sind, die Ihr Labor erfordert.
Lassen Sie uns Ihnen helfen, konsistente, genaue Ergebnisse zu erzielen. Kontaktieren Sie noch heute unsere Experten, um die perfekte Lösung für die Bedürfnisse Ihres Labors zu finden.
Visuelle Anleitung