Kurz gesagt, die Kalzinierung von Kalkstein erzeugt zwei Schlüsselprodukte: Calciumoxid (CaO) und Kohlendioxid (CO₂). Dieser Prozess beinhaltet das Erhitzen von Kalkstein, der hauptsächlich aus Calciumcarbonat (CaCO₃) besteht, auf eine hohe Temperatur, wodurch er chemisch zersetzt wird, anstatt einfach zu schmelzen oder zu verbrennen.
Die Kalzinierung von Kalkstein ist ein grundlegender industrieller Prozess. Es handelt sich um eine thermische Zersetzungsreaktion, die ein stabiles, natürliches Gestein in einen hochreaktiven chemischen Baustein (Calciumoxid) umwandelt, indem Kohlendioxidgas ausgetrieben wird.

Die Chemie der Kalzinierung: Ein genauerer Blick
Um den Prozess vollständig zu verstehen, ist es unerlässlich, die zugrunde liegende chemische Umwandlung und die Bedingungen zu kennen, die für deren Ablauf erforderlich sind.
Die chemische Kernreaktion
Die Reaktion ist elegant einfach und ein Eckpfeiler der anorganischen Chemie. Es handelt sich um eine endotherme Reaktion, was bedeutet, dass sie einen kontinuierlichen Energieeintrag (Wärme) benötigt, um abzulaufen.
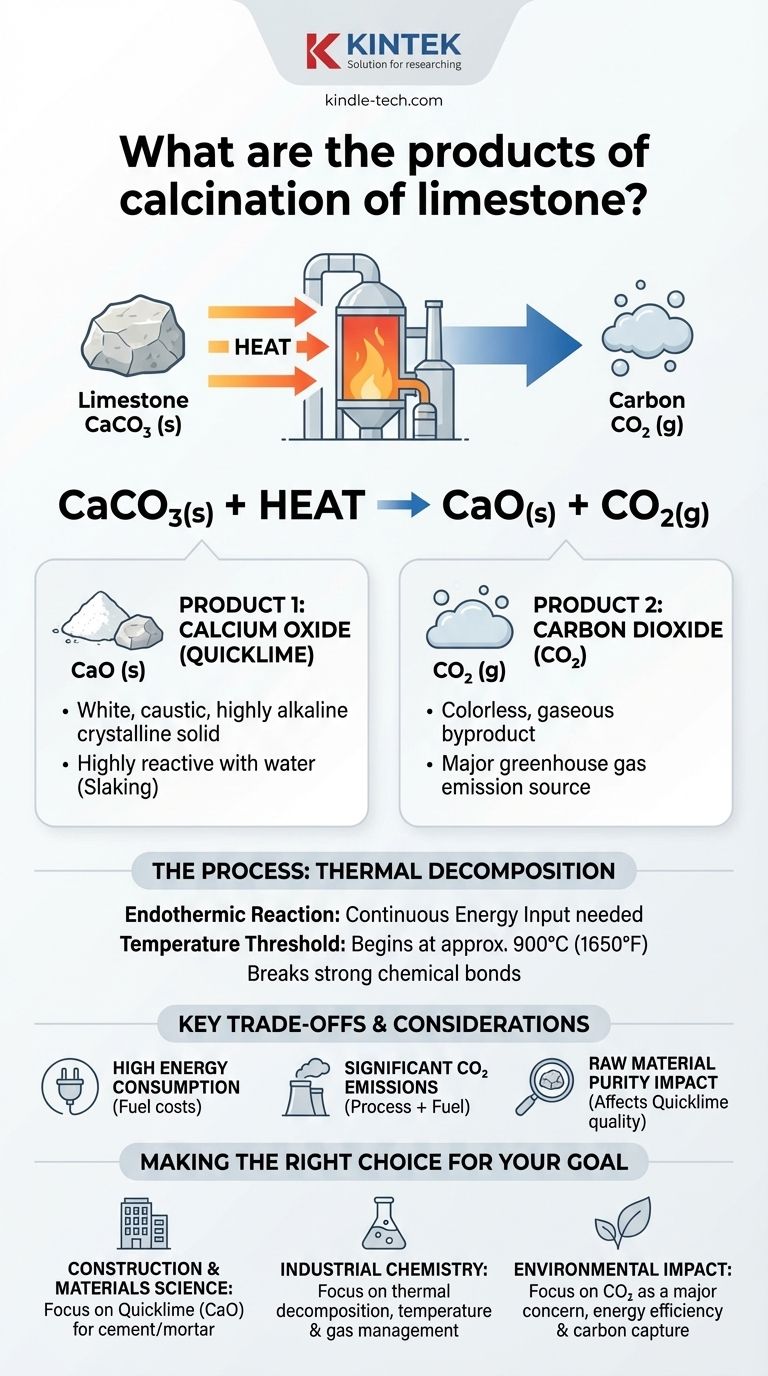
Die ausgeglichene Gleichung lautet: CaCO₃(s) + Wärme → CaO(s) + CO₂(g)
Dies zeigt, dass ein Molekül festes Calciumcarbonat in ein Molekül festes Calciumoxid und ein Molekül gasförmiges Kohlendioxid zerfällt.
Die Rolle der thermischen Zersetzung
Die Kalzinierung ist keine Reaktion mit Wärme; es ist eine Zersetzung, die durch Wärme verursacht wird. Die thermische Energie wird verwendet, um die starken chemischen Bindungen innerhalb der Calciumcarbonatstruktur aufzubrechen.
Kritische Temperaturschwelle
Die Zersetzung von Calciumcarbonat beginnt bei etwa 900°C (1650°F) unter normalem atmosphärischem Druck. In industriellen Öfen werden die Temperaturen oft höher gehalten, um sicherzustellen, dass die Reaktion effizient und vollständig abläuft.
Verständnis der Produkte und ihrer Eigenschaften
Die beiden Produkte dieser Reaktion haben sehr unterschiedliche Eigenschaften und Verwendungszwecke, weshalb der Prozess für die Industrie so grundlegend ist.
Produkt 1: Calciumoxid (Branntkalk)
Calciumoxid, allgemein bekannt als Branntkalk oder gebrannter Kalk, ist das primäre gewünschte Produkt. Es ist ein weißer, ätzender und stark alkalischer kristalliner Feststoff.
Seine wichtigste Eigenschaft ist seine hohe Reaktivität, insbesondere mit Wasser. Diese exotherme Reaktion, die als Löschen bezeichnet wird, erzeugt Calciumhydroxid oder gelöschten Kalk.
Produkt 2: Kohlendioxid (CO₂)
Kohlendioxid ist das gasförmige Nebenprodukt, das während des Prozesses aus dem Ofen ausgetrieben und entfernt wird.
Obwohl es manchmal für andere industrielle Zwecke aufgefangen wird, wird es häufiger als Abfallprodukt und als bedeutende Quelle von Treibhausgasemissionen betrachtet.
Verständnis der Kompromisse und wichtigen Überlegungen
Obwohl der Prozess chemisch einfach ist, birgt seine industrielle Anwendung erhebliche Herausforderungen und Auswirkungen, die bewältigt werden müssen.
Hoher Energieverbrauch
Das Erreichen und Halten von Temperaturen über 900°C ist ein extrem energieintensiver Prozess. Die Brennstoffkosten stellen einen Großteil der Betriebskosten bei der Herstellung von Branntkalk dar.
Erhebliche CO₂-Emissionen
Die Kalzinierung von Kalkstein ist eine der größten globalen Quellen für Kohlendioxidemissionen. Das CO₂ stammt aus zwei Quellen: der chemischen Zersetzung des Kalksteins selbst und den fossilen Brennstoffen, die typischerweise zum Beheizen der Öfen verbrannt werden.
Einfluss der Reinheit des Rohmaterials
Die Qualität des endgültigen Branntkalks hängt direkt von der Reinheit des ursprünglichen Kalksteins ab. Verunreinigungen wie Siliziumdioxid, Ton oder Magnesiumcarbonat können die Reaktivität und Eigenschaften des Endprodukts beeinflussen, was für Anwendungen wie die Stahl- und Zementherstellung entscheidend ist.
Die richtige Wahl für Ihr Ziel treffen
Das Verständnis dieses Prozesses ermöglicht es Ihnen, seine Rolle in verschiedenen Bereichen zu würdigen. Die Bedeutung der Produkte hängt vollständig von Ihrer spezifischen Anwendung ab.
- Wenn Ihr Hauptaugenmerk auf Bauwesen und Materialwissenschaft liegt: Das Schlüsselprodukt ist Calciumoxid (Branntkalk), da es der wesentliche Vorläufer für Zement und Mörtel ist.
- Wenn Ihr Hauptaugenmerk auf der industriellen Chemie liegt: Betrachten Sie dies als eine klassische thermische Zersetzungsreaktion, bei der die Steuerung von Temperatur, Energieeinträgen und Gasentfernung die kritischen Prozessvariablen sind.
- Wenn Ihr Hauptaugenmerk auf den Umweltauswirkungen liegt: Erkennen Sie, dass das Nebenprodukt, Kohlendioxid, ein großes Problem darstellt, was Energieeffizienz und Kohlenstoffabscheidungstechnologien für die Zukunft der Industrie unerlässlich macht.
Letztendlich ist das Verständnis der Produkte der Kalksteinkalzinierung der erste Schritt zur Beherrschung ihrer Anwendung in unzähligen wichtigen Industrien.
Zusammenfassungstabelle:
| Produkt | Chemische Formel | Gebräuchlicher Name | Schlüsseleigenschaften |
|---|---|---|---|
| Calciumoxid | CaO | Branntkalk | Weiß, ätzend, stark alkalisch, reaktiv mit Wasser |
| Kohlendioxid | CO₂ | - | Farbloses Gas, Treibhausgas, industrielles Nebenprodukt |
Optimieren Sie Ihren Kalzinierungsprozess mit der fortschrittlichen Laborausrüstung von KINTEK. Egal, ob Sie thermische Zersetzungsreaktionen erforschen oder die industrielle Produktion skalieren, unsere Hochtemperaturöfen und -brennöfen gewährleisten präzise Temperaturregelung und Energieeffizienz. Wir bieten die zuverlässigen Werkzeuge, die Sie benötigen, um hochreinen Branntkalk herzustellen und gleichzeitig den Energieverbrauch und die Emissionen zu kontrollieren. Kontaktieren Sie uns noch heute (#ContactForm), um zu besprechen, wie unsere Lösungen Ihre Materialwissenschafts- und Industriechemie-Workflows verbessern können.
Visuelle Anleitung
Ähnliche Produkte
- Elektrischer Drehrohrofen Kontinuierlicher Betrieb Kleine Drehrohrofen Heizpyrolyseanlage
- Elektrische Drehrohrofen-Pyrolyseofenanlage Kalzinator Kleiner Drehrohrofen Rotierender Ofen
Andere fragen auch
- Wie werden Drehrohröfen beheizt? Erklärung der direkten vs. indirekten Heizmethoden
- Welche Arten von Kalzinatoren gibt es? Ein Leitfaden zur Auswahl der richtigen thermischen Verarbeitungsanlage
- Ist ein Drehrohrofen ein Ofen? Entdecken Sie die Hauptunterschiede für die industrielle Verarbeitung
- Warum befinden sich Ketten in einem Drehrohrofen? Steigern Sie Effizienz & Kontrolle durch internen Wärmeaustausch
- Wie hoch ist die Temperatur eines Drehrohrofens? Es hängt von Ihrem Material und Prozessziel ab

