Im Grunde genommen ist eine Inertatmosphäre eine kontrollierte Umgebung, in der die normale, reaktive Luft absichtlich durch ein nicht reaktives (oder „inertes“) Gas ersetzt wurde. Dies geschieht, um unerwünschte chemische Reaktionen wie Oxidation oder Verbrennung zu verhindern, die sonst in Anwesenheit von Sauerstoff auftreten würden.
Der grundlegende Zweck einer Inertatmosphäre liegt nicht im Gas selbst, sondern darin, was es entfernt: den Sauerstoff und die Feuchtigkeit aus der Luft, die Materialien abbauen, verderben, rosten oder entzünden lassen.

Das Problem: Reaktive Luft
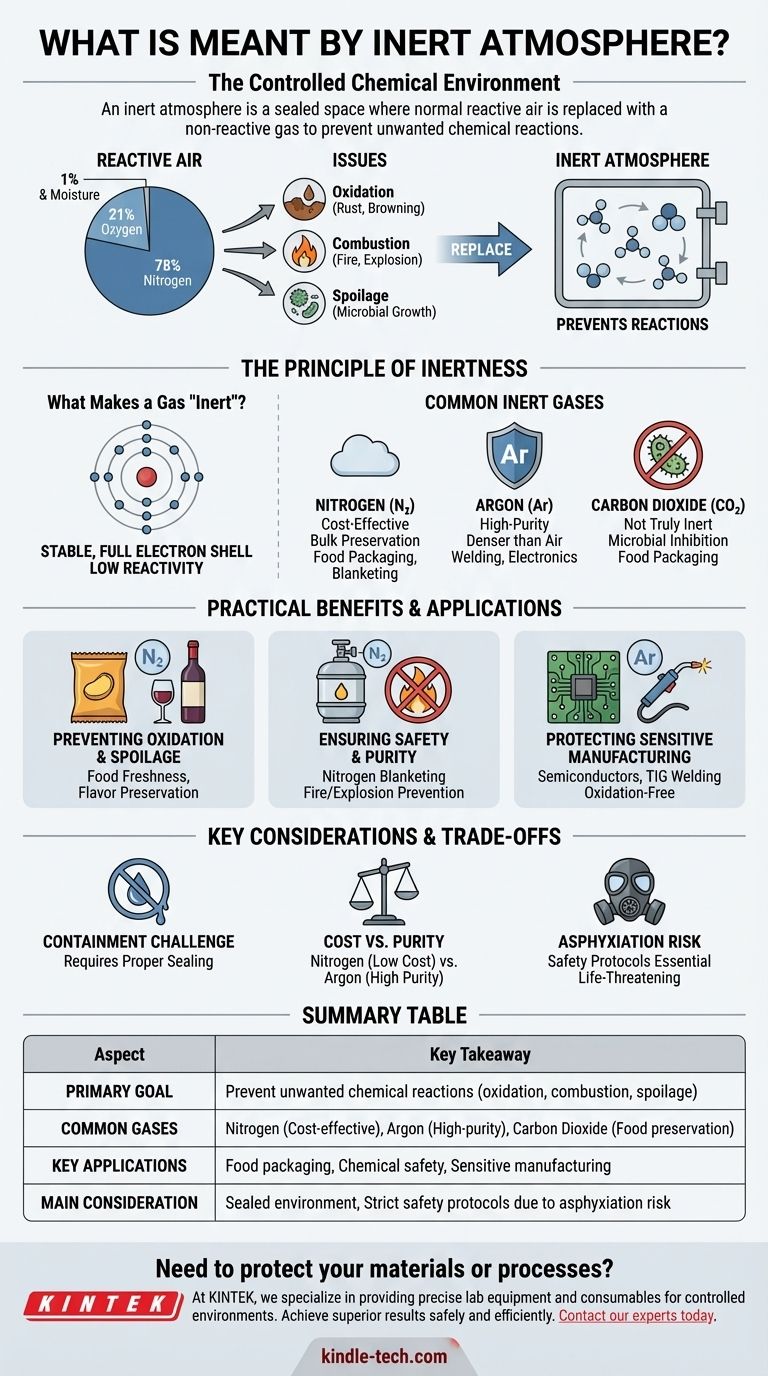
Die Luft, die wir atmen, besteht zu etwa 78 % aus Stickstoff, 21 % aus Sauerstoff und enthält geringe Mengen anderer Gase, einschließlich Wasserdampf. Für viele industrielle, wissenschaftliche und kommerzielle Prozesse stellt diese Zusammensetzung ein erhebliches Risiko dar.
Warum Sauerstoff oft ein Problem darstellt
Sauerstoff ist ein hochreaktives Element. Seine Neigung, sich mit anderen Substanzen zu verbinden, ist für alltägliche Prozesse wie das Rosten (Oxidation von Eisen) und das Braunwerden eines angeschnittenen Apfels verantwortlich. In volatileren Situationen ist er ein Hauptbestandteil von Feuer und Explosionen.
Die Rolle der Feuchtigkeit
Der in der Luft vorhandene Wasserdampf kann ebenfalls Korrosion beschleunigen und ein Umfeld für mikrobielles Wachstum schaffen, was zum Verderb von Lebensmitteln oder zur Kontamination empfindlicher Materialien führt.
Das Prinzip der Inertheit
Die Schaffung einer Inertatmosphäre beinhaltet das Spülen eines versiegelten Raumes mit Umgebungsluft und das erneute Füllen mit einem Gas, das das zu schützende Produkt oder den Prozess nicht beeinträchtigt.
Was macht ein Gas „inert“?
Inertgase sind chemisch stabil, da ihre äußerste Elektronenschale vollständig gefüllt ist, was bedeutet, dass sie nur eine sehr geringe Neigung haben, mit anderen Elementen zu reagieren. Während echte Edelgase wie Argon am inertesten sind, sind andere Gase wie Stickstoff für die meisten Anwendungen nicht reaktiv genug.
Häufig verwendete Gase
Die Wahl des Gases hängt vom erforderlichen Grad der Inertheit und dem Budget ab.
- Stickstoff (N₂): Mit Abstand am häufigsten, da es kostengünstig ist und den größten Teil unserer Atmosphäre ausmacht, was die Beschaffung erleichtert.
- Argon (Ar): Inert als Stickstoff und dichter als Luft. Es wird für empfindlichere Anwendungen wie hochwertiges Schweißen und Elektronikfertigung eingesetzt, bei denen selbst die leichte Reaktivität von Stickstoff nicht akzeptabel ist.
- Kohlendioxid (CO₂): Obwohl es nicht wirklich inert ist, wird es häufig in Lebensmittelverpackungen verwendet, da es Sauerstoff verdrängt und das Wachstum einiger Bakterien und Schimmelpilze hemmen kann.
Praktische Vorteile und Anwendungen
Der Wert einer Inertatmosphäre zeigt sich in einer Vielzahl von Bereichen, in denen die Kontrolle der chemischen Umgebung von entscheidender Bedeutung ist.
Verhinderung von Oxidation und Verderb
Dies ist eine der häufigsten Anwendungen. Die Luft in einer Tüte Kartoffelchips wird durch Stickstoff ersetzt, um zu verhindern, dass die Öle ranzig werden, und um das Produkt zu polstern. Ebenso verwenden Winzer Inertgase, um Wein während des Abfüllens vor Sauerstoff zu schützen.
Gewährleistung von Sicherheit und Reinheit
In Chemieanlagen wird die Luft in Behältern, die brennbare Flüssigkeiten oder Pulver enthalten, häufig durch Stickstoff ersetzt. Dieser als „Stickstoffüberlagerung“ (Nitrogen Blanketing) bekannte Prozess entfernt den für Feuer oder Explosionen erforderlichen Sauerstoff und verbessert die Sicherheit drastisch.
Schutz der empfindlichen Fertigung
Bei der Herstellung von Halbleitern und Elektronik können selbst mikroskopische Oxidationsspuren eine Komponente ruinieren. Diese Prozesse werden oft in Kammern durchgeführt, die mit einem hochreinen Inertgas wie Argon gefüllt sind. Schweißer verwenden ebenfalls einen Schutzschild aus Inertgas, um das geschmolzene Schweißbad vor Sauerstoff zu schützen, der die endgültige Verbindung schwächen würde.
Wichtige Überlegungen und Kompromisse
Obwohl die Implementierung einer Inertatmosphäre wirkungsvoll ist, erfordert sie eine sorgfältige Planung und das Verständnis ihrer Grenzen.
Die Herausforderung der Eindämmung
Eine Inertatmosphäre ist nur wirksam, wenn der Behälter oder Raum ordnungsgemäß abgedichtet ist. Jede Leckage lässt Sauerstoff und Feuchtigkeit wieder eindringen, was den Zweck des Systems zunichtemacht.
Kosten vs. Reinheit
Es besteht ein direkter Kompromiss zwischen den Kosten des Gases und seinem Grad an Inertheit. Stickstoff ist für die meisten Massenanwendungen ausreichend, aber Prozesse, die absolute chemische Reinheit erfordern, verlangen nach teureren Gasen wie Argon.
Erhebliches Erstickungsrisiko
Eine Atmosphäre, die zur Verhinderung von Verbrennung entwickelt wurde, ist auch eine Atmosphäre, die kein Leben erhalten kann. Jeder Bereich, der mit einem Inertgas geflutet wird, stellt eine extreme Erstickungsgefahr dar, da er wenig bis keinen Sauerstoff enthält. Strikte Sicherheitsprotokolle sind für alle Mitarbeiter, die in oder in der Nähe dieser Umgebungen arbeiten, unerlässlich.
Die richtige Wahl für Ihr Ziel treffen
Die Auswahl und Anwendung einer Inertatmosphäre wird vollständig durch das gewünschte Ergebnis bestimmt.
- Wenn Ihr Hauptaugenmerk auf kostengünstiger Konservierung liegt: Stickstoff ist die Standardwahl für groß angelegte Anwendungen wie Lebensmittelverpackungen, Getreidesilos und die Überlagerung von Chemikalientanks.
- Wenn Ihr Hauptaugenmerk auf hochreinen Prozessen liegt: Argon ist die überlegene Option für empfindliche Arbeiten wie WIG-Schweißen, wissenschaftliche Forschung und die Herstellung von Siliziumwafern, bei denen absolute Nichtreaktivität entscheidend ist.
- Wenn Ihr Hauptaugenmerk auf der aktiven Hemmung von Mikroben liegt: Eine modifizierte Atmosphäre, die Kohlendioxid enthält, wird häufig bei der Verpackung von Fleisch und Produkten verwendet, um die Haltbarkeit über die reine Verhinderung der Oxidation hinaus zu verlängern.
Letztendlich ist eine Inertatmosphäre ein mächtiges Werkzeug, um die chemische Umgebung zu kontrollieren, um empfindliche Materialien und Prozesse zu schützen und zu konservieren.
Zusammenfassungstabelle:
| Aspekt | Wichtigste Erkenntnis |
|---|---|
| Hauptziel | Verhinderung unerwünschter chemischer Reaktionen (Oxidation, Verbrennung, Verderb). |
| Häufige Gase | Stickstoff (kosteneffizient), Argon (hohe Reinheit), Kohlendioxid (Lebensmittelkonservierung). |
| Wichtige Anwendungen | Lebensmittelverpackung, chemische Sicherheit (Überlagerung), empfindliche Fertigung (Schweißen, Elektronik). |
| Hauptüberlegung | Erfordert eine abgedichtete Umgebung und strenge Sicherheitsprotokolle aufgrund der Erstickungsgefahr. |
Müssen Sie Ihre Materialien oder Prozesse vor Sauerstoff und Feuchtigkeit schützen?
Bei KINTEK sind wir spezialisiert auf die Bereitstellung der präzisen Laborgeräte und Verbrauchsmaterialien, die zur Schaffung und Aufrechterhaltung kontrollierter Umgebungen für Ihr Labor erforderlich sind. Ob Ihr Ziel kosteneffiziente Konservierung oder hochreine Verarbeitung ist, unsere Lösungen können Ihnen helfen, überlegene Ergebnisse sicher und effizient zu erzielen.
Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie wir Ihre spezifische Anwendung mit zuverlässigen Inertatmosphärenlösungen unterstützen können.
Visuelle Anleitung
Ähnliche Produkte
- 1200℃ Schutzgasofen Stickstoff-Inertgas-Atmosphärenofen
- 1700℃ Kontrollierte Atmosphäre Ofen Stickstoff Inertgas Ofen
- 1400℃ Kammerofen mit kontrollierter Atmosphäre und Stickstoff- und Inertgasatmosphäre
- Kontrollierter Hochtemperatur-Wasserstoff-Ofen
- Kammerofen mit Bandförderer für kontrollierte Atmosphäre
Andere fragen auch
- Was ist die Funktion eines Schutzgasofens? Nitrierhärten für AISI 52100 & 1010 Stahl meistern
- Was ist die Funktion eines hochpräzisen Schutzgasofens für die Legierung 617? Simulation extremer VHTR-Bedingungen
- Was ist die Rolle der Ofenatmosphäre? Beherrschen Sie die präzise metallurgische Kontrolle für Ihre Wärmebehandlung
- Wie wird Sauerstoff (O2) in kontrollierten Ofenatmosphären eingesetzt? Beherrschen der Oberflächentechnik für Metalle
- Was ist ein Schutzgasofen? Reinheit und Präzision bei der Hochtemperaturverarbeitung erreichen




