Kurz gesagt, Schutzatmosphären sind beim Sintern notwendig, um zerstörerische chemische Reaktionen, hauptsächlich Oxidation, zu verhindern, die bei hohen Temperaturen auftreten. Diese kontrollierte Umgebung stellt sicher, dass sich Metallpulverpartikel effektiv miteinander verbinden können, was das gesamte Ziel des Prozesses ist.
Das Sintern erfordert immense Hitze, um Materialpartikel zu verschmelzen, aber dieselbe Hitze macht diese Partikel sehr anfällig für chemische Angriffe aus der Umgebungsluft. Eine Schutzatmosphäre ersetzt die reaktive Luft durch ein kontrolliertes Gas, das als chemischer Schild wirkt, der diese Reaktionen entweder verhindert oder sie zu einem gewünschten Ergebnis führt.

Die grundlegende Herausforderung: Reaktivität bei hohen Temperaturen
Das Sintern basiert auf einem einfachen Prinzip: Ein verdichtetes Pulver wird erhitzt, bis sich die Partikel verbinden und verdichten. Die erforderlichen hohen Temperaturen beschleunigen jedoch auch chemische Reaktionen dramatisch, was eine erhebliche technische Herausforderung darstellt.
Der Hauptfeind: Oxidation
Die meisten industriellen Sinterprozesse umfassen Metallpulver. Beim Erhitzen reagieren diese Metalle leicht mit jedem in der Atmosphäre vorhandenen Sauerstoff.
Diese Reaktion, genannt Oxidation, bildet eine dünne, harte, keramikähnliche Schicht (ein Oxid) auf der Oberfläche jedes Pulverpartikels.
Diese Oxidschicht wirkt als Barriere und verhindert physisch, dass die Metalloberflächen direkten Kontakt aufnehmen und verschmelzen. Das Ergebnis ist ein schwaches, sprödes Teil, das nicht richtig gesintert wurde.
Jenseits von Sauerstoff: Andere Verunreinigungen
Während Sauerstoff das Hauptproblem ist, können auch andere Bestandteile der Luft schädlich sein. Wasserdampf (Luftfeuchtigkeit) und Kohlendioxid sind beides starke Oxidationsmittel bei Sintertemperaturen und müssen entfernt oder verdrängt werden, um das Material zu schützen.
Wie Schutzatmosphären das Problem lösen
Eine Schutzatmosphäre ersetzt die umgebende, reaktive Luft im Ofen durch ein Gas oder eine Gasmischung, die entweder nicht reaktiv ist oder eine spezifische, wünschenswerte Reaktivität aufweist.
Das Prinzip der Inertheit: Einen Schild schaffen
Der einfachste Ansatz ist die Verwendung eines inerten Gases, am häufigsten Stickstoff (N₂) oder Argon (Ar).
Diese Gase reagieren auch bei hohen Temperaturen nicht chemisch mit dem zu sinternden Material. Sie wirken, indem sie einfach den Sauerstoff und die Feuchtigkeit verdrängen und einen neutralen „Schild“ um die Teile bilden.
Das Prinzip der Reduktion: Oberflächen aktiv reinigen
Ein leistungsfähigerer Ansatz beinhaltet eine reduzierende Atmosphäre, die typischerweise Wasserstoff (H₂) enthält.
Wasserstoff verhindert nicht nur neue Oxidation, sondern kann diese auch aktiv umkehren. Er entzieht vorhandenen Oxidschichten auf den Pulveroberflächen chemisch Sauerstoffatome und wandelt sie in Wasserdampf (H₂O) um, der dann aus dem Ofen gespült wird.
Diese „Reinigungsaktion“ gewährleistet eine makellose metallische Oberfläche, die entscheidend ist, um maximale Dichte und Festigkeit im Endteil zu erreichen, insbesondere bei leicht oxidierbaren Materialien.
Gezielte Reaktionen: Die Oberfläche modifizieren
Manchmal geht es nicht nur darum, die Oberfläche zu schützen, sondern sie gezielt zu verändern. Spezifische Gasmischungen können verwendet werden, um Elemente in die Materialoberfläche zu diffundieren.
Zum Beispiel kann eine kohlenstoffreiche Atmosphäre (eine Aufkohlungsatmosphäre) verwendet werden, um eine harte, verschleißfeste Stahloberfläche an einem Teil zu erzeugen. Ähnlich kann eine stickstoffreiche Atmosphäre zum Nitrieren verwendet werden. In diesen Fällen wird die Atmosphäre zu einem wichtigen Bestandteil des Materialdesigns.
Die Kompromisse verstehen
Die Wahl der richtigen Atmosphäre ist ein Gleichgewicht aus technischen Anforderungen, Sicherheit und Kosten. Es gibt keine einzige „beste“ Atmosphäre für alle Anwendungen.
Inerte vs. reduzierende Atmosphären
Eine inerte Atmosphäre wie reiner Stickstoff ist sicher, relativ kostengünstig und wirksam zur Verhinderung von Oxidation bei weniger empfindlichen Materialien.
Eine reduzierende Atmosphäre, die Wasserstoff enthält, ist effektiver für die Herstellung hochreiner, hochdichter Teile, bringt aber die Kosten- und Sicherheitskomplexität des Umgangs mit einem brennbaren Gas mit sich.
Die entscheidende Rolle von Reinheit und Taupunkt
Die Wirksamkeit jeder Schutzatmosphäre hängt von ihrer Reinheit ab. Selbst eine Stickstoffatmosphäre kann oxidierend werden, wenn sie zu viel Feuchtigkeit oder Spuren von Sauerstoff enthält.
Der Taupunkt des Gases ist ein kritisches Maß für seinen Feuchtigkeitsgehalt. Ein niedriger Taupunkt weist auf ein sehr trockenes Gas hin, was für die Verhinderung unerwünschter Reaktionen während des Hochtemperatur-Sinterzyklus unerlässlich ist.
Kosten und Systemkomplexität
Reines Argon bietet den inertesten Schutz, ist aber deutlich teurer als Stickstoff. Wasserstoffsysteme erfordern ausgeklügelte Durchflussregelungen, Sicherheitsverriegelungen und Abfackelsysteme, was die Anfangsinvestition und die Betriebskomplexität des Ofens erhöht.
Die richtige Atmosphäre für Ihr Ziel auswählen
Ihre Wahl der Atmosphäre hängt direkt von dem Material ab, mit dem Sie arbeiten, und den endgültigen Eigenschaften, die Sie erreichen müssen.
- Wenn Ihr Hauptaugenmerk auf der grundlegenden Oxidationsverhinderung bei robusten Materialien liegt (wie einigen Kupferlegierungen): Eine inerte Stickstoffatmosphäre ist oft die kostengünstigste und ausreichende Wahl.
- Wenn Ihr Hauptaugenmerk auf maximaler Dichte und Festigkeit bei empfindlichen Materialien liegt (wie Edelstählen oder Wolfram): Eine reduzierende Atmosphäre, die Wasserstoff enthält, ist notwendig, um Oberflächenoxide zu entfernen und eine starke metallische Bindung zu gewährleisten.
- Wenn Ihr Hauptaugenmerk auf der Verbesserung der Oberflächenhärte und Verschleißfestigkeit liegt: Eine reaktive Atmosphäre, die für das Aufkohlen oder Nitrieren ausgelegt ist, ist erforderlich, um die gewünschte Oberflächenchemie zu erreichen.
Letztendlich ist die Kontrolle der Ofenatmosphäre gleichbedeutend mit der Kontrolle der grundlegenden Chemie Ihres Prozesses, wodurch Sie die direkte Kontrolle über die endgültige Qualität des gesinterten Bauteils erhalten.
Zusammenfassungstabelle:
| Funktion | Häufig verwendete Gase | Hauptvorteil |
|---|---|---|
| Inerte Abschirmung | Stickstoff (N₂), Argon (Ar) | Verhindert Oxidation, kostengünstig |
| Aktive Reduktion | Wasserstoff (H₂)-Mischungen | Entfernt vorhandene Oxide für maximale Festigkeit |
| Oberflächenmodifikation | Kohlenstoff-/Stickstoffreiche Gase | Erhöht die Härte durch Aufkohlen/Nitrieren |
Erzielen Sie eine präzise Kontrolle über Ihre Sinterergebnisse. Die richtige Schutzatmosphäre ist entscheidend für Teiledichte, Festigkeit und Oberflächeneigenschaften. KINTEK ist spezialisiert auf Laborgeräte und Verbrauchsmaterialien und bietet Lösungen für alle Ihre Labor-Sinteranforderungen. Lassen Sie sich von unseren Experten bei der Auswahl der idealen Atmosphäre für Ihr Material und Ihre Ziele unterstützen. Kontaktieren Sie uns noch heute, um zu besprechen, wie wir Ihren Prozess verbessern und hochwertige Ergebnisse sicherstellen können.
Visuelle Anleitung
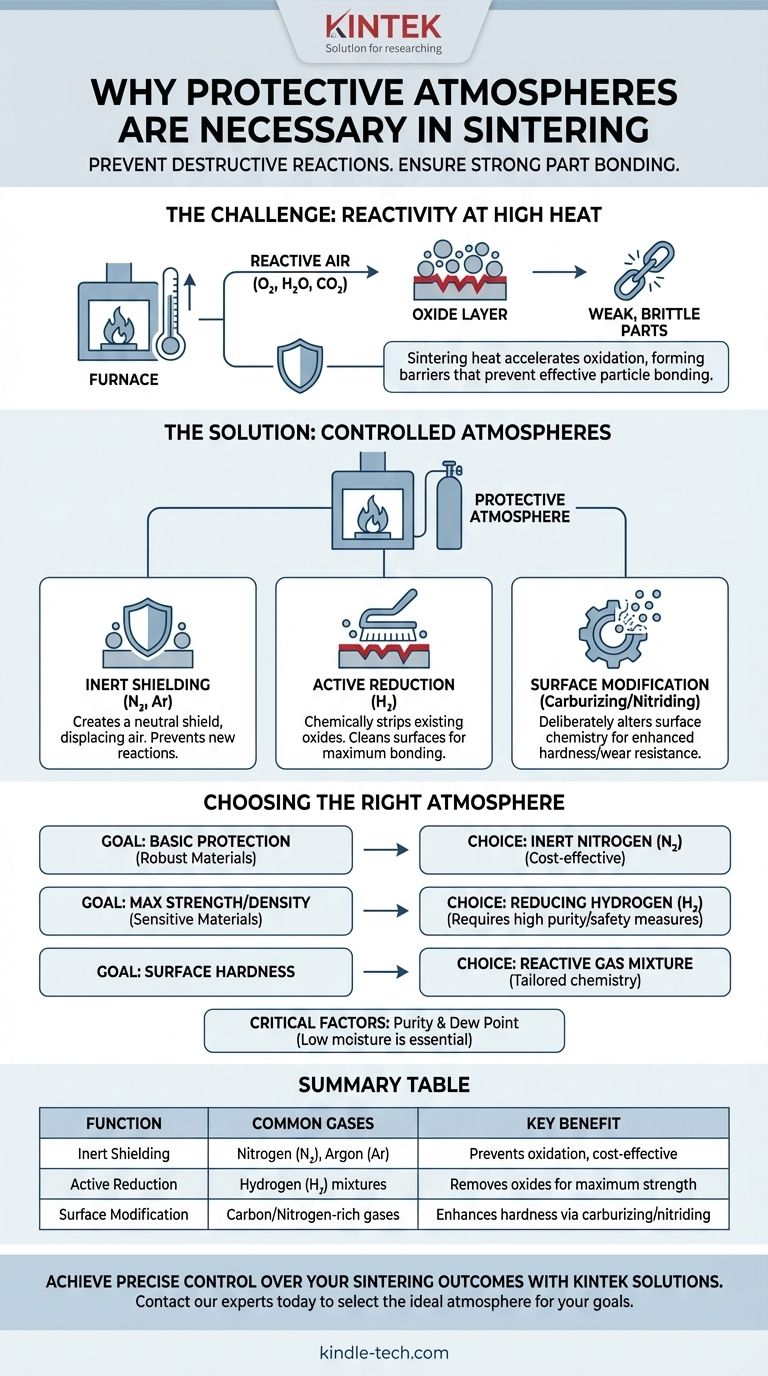
Ähnliche Produkte
- Kammerofen mit Bandförderer für kontrollierte Atmosphäre
- Kontrollierter Hochtemperatur-Wasserstoff-Ofen
- 1200℃ Schutzgasofen Stickstoff-Inertgas-Atmosphärenofen
- 1700℃ Kontrollierte Atmosphäre Ofen Stickstoff Inertgas Ofen
- 1400℃ Kammerofen mit kontrollierter Atmosphäre und Stickstoff- und Inertgasatmosphäre
Andere fragen auch
- Warum ist ein Ofen mit kontrollierter Atmosphäre für die Herstellung von aktiven Metallkatalysatoren notwendig?
- Warum ist die Kontrolle der Sinteratmosphäre unerlässlich? Optimale Materialeigenschaften erzielen
- Wie wird Sauerstoff (O2) in kontrollierten Ofenatmosphären eingesetzt? Beherrschen der Oberflächentechnik für Metalle
- Was sind einige der Gründe, warum ein Schutzgasofen beim Sintern wünschenswert ist? Erzielen Sie überlegene Sinterergebnisse
- Wie funktioniert ein Durchlaufofen mit Bandförderer? Erreichen Sie eine hochvolumige, reproduzierbare Wärmebehandlung



















