Das direkte Ergebnis der Kalzinierung ist ein fester Stoff, der thermisch gereinigt oder chemisch verändert wurde. Der Prozess verwendet hohe Hitze in einer sauerstoffarmen Umgebung, um flüchtige Substanzen wie Wasser und Kohlendioxid auszutreiben, Verbindungen zu zersetzen oder die kristalline Struktur des Materials zu verändern, ohne es zu schmelzen.
Die Kalzinierung ist kein letzter Fertigungsschritt, sondern ein entscheidender vorbereitender Prozess. Ihr Hauptzweck ist es, einen rohen, unreinen Feststoff in ein konzentrierteres, stabileres oder reaktiveres Material umzuwandeln, das für einen nachfolgenden Prozess wie das Schmelzen oder die chemische Synthese optimiert ist.

Was ändert sich während der Kalzinierung?
Die Kalzinierung erreicht ihr Ziel, indem sie durch sorgfältig kontrolliertes Erhitzen spezifische physikalische und chemische Veränderungen in einem Material hervorruft. Das Ergebnis wird durch die Art dieser Transformationen definiert.
Thermische Zersetzung
Dies ist das häufigste Ziel der Kalzinierung. Die Hitze zerlegt eine chemische Verbindung in zwei oder mehr einfachere Substanzen.
Ein klassisches Beispiel ist die Herstellung von Kalk aus Kalkstein. Das Erhitzen von Calciumcarbonat (CaCO3) treibt Kohlendioxid (CO2) aus und hinterlässt Calciumoxid (CaO) oder Branntkalk.
Entfernung flüchtiger Bestandteile
Die Kalzinierung ist sehr effektiv bei der Entfernung flüchtiger Verunreinigungen, die im Feststoff eingeschlossen sind. Dies reinigt und konzentriert das gewünschte Material.
Dazu gehört die Entfernung von physikalisch absorbiertem Wasser (Trocknung) und, was noch wichtiger ist, chemisch gebundenen Wassermolekülen aus hydratisierten Mineralien, ein Prozess, der als Dehydratisierung bekannt ist.
Induzierung eines Phasenübergangs
Manchmal besteht das Ziel nicht darin, die chemische Zusammensetzung zu ändern, sondern die interne Kristallstruktur oder Phase des Materials zu verändern.
Das Erhitzen eines Materials kann dazu führen, dass sich seine Atome zu einer anderen, oft stabileren oder nützlicheren, kristallinen Form neu anordnen. Dies ist ein häufiger Schritt bei der Herstellung spezifischer Keramiktypen und Katalysatoren.
Das Ziel: Materialien für den nächsten Schritt vorbereiten
Das Verständnis des Ergebnisses der Kalzinierung erfordert, es als Mittel zum Zweck zu betrachten. Der resultierende Feststoff ist selten das Endprodukt, aber er ist nun bereit für eine anspruchsvollere industrielle Anwendung.
Erhöhung der Erzkonzentration
In der Metallurgie wird die Kalzinierung verwendet, um Erze vor dem Schmelzen zu verarbeiten. Durch das Austreiben von Wasser aus hydratisierten Oxiden oder Kohlendioxid aus Karbonaterzen entfernt der Prozess totes Gewicht.
Dies erhöht den Metallanteil im Erz erheblich, wodurch der nachfolgende, energieintensive Schmelzprozess effizienter und kostengünstiger wird.
Erzeugung eines reaktiveren Materials
Das kalzinierte Produkt ist oft chemisch reaktiver als das ursprüngliche Rohmaterial.
Der aus der Kalzinierung von Kalkstein gewonnene Kalk (Calciumoxid) ist ein wichtiger Bestandteil bei der Zementherstellung, gerade weil er leicht mit anderen Komponenten reagiert. Der ursprüngliche Kalkstein tut dies nicht.
Die wichtigsten Unterscheidungen verstehen
Um wirklich zu verstehen, was die Kalzinierung produziert, ist es entscheidend, sie von ähnlichen Hochtemperaturprozessen zu unterscheiden, die andere Ziele und Ergebnisse haben.
Kalzinierung vs. Rösten
Der Hauptunterschied ist das Vorhandensein von Luft. Kalzinierung findet in Abwesenheit oder begrenzter Zufuhr von Luft statt, um eine thermische Zersetzung zu bewirken.
Rösten hingegen ist das Erhitzen in einem Überschuss an Luft. Sein Zweck ist es, Oxidation zu induzieren, typischerweise die Umwandlung von Metallsulfiderzen in Metalloxide.
Kalzinierung vs. Sintern
Diese Prozesse haben gegensätzliche physikalische Ziele. Kalzinierung zielt darauf ab, ein Material zu reinigen oder zu zersetzen, wodurch es oft poröser oder pulverförmiger wird.
Sintern verwendet Hitze, um kleine Partikel zu einem einzigen, festen Stück zu verschmelzen, wodurch dessen Festigkeit und Dichte erhöht werden, ohne es zu schmelzen.
Kalzinierung effektiv anwenden
Das gewünschte Ergebnis bestimmt, wie und wann Sie diesen Prozess anwenden sollten. Ihre Wahl hängt vollständig vom Ausgangsmaterial und Ihrem Endziel ab.
- Wenn Ihr Hauptaugenmerk auf der Herstellung von Kalk oder Zement liegt: Verwenden Sie die Kalzinierung zur thermischen Zersetzung von Kalkstein (Calciumcarbonat) zu Kalk (Calciumoxid).
- Wenn Ihr Hauptaugenmerk auf der Vorbereitung eines Metallerzes zum Schmelzen liegt: Wenden Sie die Kalzinierung an, um Wasser oder Kohlendioxid zu entfernen und dadurch das gewünschte Metalloxid zu konzentrieren.
- Wenn Ihr Hauptaugenmerk auf der Entwicklung spezifischer Materialeigenschaften liegt: Verwenden Sie die Kalzinierung, um den Phasenübergang und die Kristallstruktur Ihres Rohmaterials präzise zu steuern, eine gängige Praxis in der Keramik- und Katalysatorproduktion.
Letztendlich ist die Kalzinierung der grundlegende Wärmebehandlungsprozess zur Reinigung und Vorbereitung fester Materialien für ihre Endanwendung.
Zusammenfassungstabelle:
| Prozessziel | Ausgangsmaterial | Endmaterial | Wesentliche Änderung |
|---|---|---|---|
| Thermische Zersetzung | Kalkstein (CaCO₃) | Branntkalk (CaO) | Treibt CO₂ aus |
| Entfernung von flüchtigen Stoffen | Hydratisiertes Erz | Konzentriertes Erz | Entfernt Wasser/Verunreinigungen |
| Phasenübergang | Keramikvorläufer | Stabile Keramik | Verändert die Kristallstruktur |
Benötigen Sie eine präzise thermische Verarbeitung für Ihre Materialien? Die fortschrittlichen Kalzinierungsanlagen von KINTEK sind für Labor- und Industrieanwendungen konzipiert und gewährleisten optimale Reinheit, Reaktivität und Phasensteuerung für Erze, Keramiken und chemische Vorläufer. Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie unsere Lösungen Ihren Materialvorbereitungsprozess verbessern können.
Visuelle Anleitung
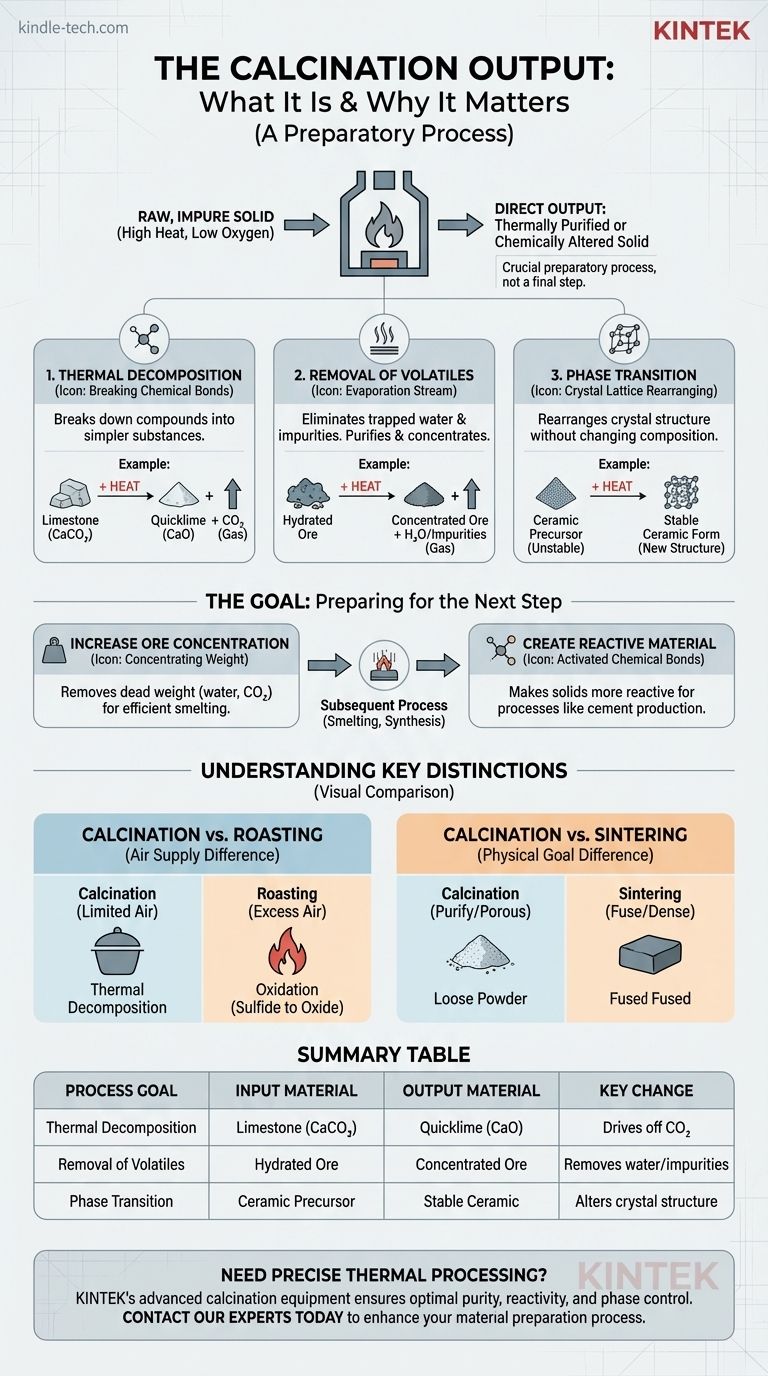
Ähnliche Produkte
- Elektrische Drehrohrofen-Pyrolyseofenanlage Kalzinator Kleiner Drehrohrofen Rotierender Ofen
- Elektrischer Drehrohrofen Kontinuierlicher Betrieb Kleine Drehrohrofen Heizpyrolyseanlage
- Nicht verzehrender Vakuumlichtbogen-Induktionsofen
- Vertikaler Hochtemperatur-Graphit-Vakuum-Graphitierungs-Ofen
- Graphitierungs-Vakuumofen für ultrahohe Temperaturen
Andere fragen auch
- Was ist ein elektrischer Drehrohrofen? Erzielen Sie eine überlegene gleichmäßige Erwärmung Ihrer Materialien
- Wie hoch ist die Temperatur eines Drehrohrofens? Es hängt von Ihrem Material und Prozessziel ab
- Wie hoch ist der Wirkungsgrad eines Drehrohrofens? Erreichen Sie einen thermischen Wirkungsgrad von über 95 %
- Was sind die Vorteile von Drehrohrofen? Erreichen Sie überlegene Gleichmäßigkeit & Effizienz
- Welche Arten von Kalzinatoren gibt es? Ein Leitfaden zur Auswahl der richtigen thermischen Verarbeitungsanlage



















