Im Kern ist das Prinzip der Galvanik der Prozess der Verwendung eines Gleichstroms, um gelöste Metallionen aus einer Lösung zu reduzieren und eine dünne, feste Metallschicht auf einem leitfähigen Objekt zu bilden. Diese kontrollierte elektrochemische Reaktion ermöglicht es Ihnen, ein Metall auf ein anderes zu „plattieren“ und so die Oberflächeneigenschaften des Grundmaterials grundlegend zu verändern.
Der gesamte Prozess hängt von der Erzeugung eines Elektrolysekreislaufs ab. In diesem Kreislauf treibt Elektrizität eine nicht-spontane chemische Reaktion an und zwingt positiv geladene Metallionen in einem flüssigen Bad, Elektronen aufzunehmen und sich als neutrale Metallschicht auf einer Zieloberfläche abzuscheiden.
Die Kernkomponenten eines galvanischen Systems
Um das Prinzip in der Praxis zu verstehen, müssen Sie zunächst seine vier wesentlichen Komponenten kennen, die innerhalb einer Elektrolysezelle zusammenwirken.
Der Elektrolyt (Das Bad)
Der Elektrolyt ist eine Lösung, die eine hohe Konzentration der abzuscheidenden Metallionen enthält. Diese wird typischerweise durch Auflösen von Metallsalzen (wie Kupfersulfat oder Nickelchlorid) in Wasser hergestellt. Das Bad enthält auch andere Zusätze, um die Qualität der Endbeschichtung zu steuern.
Die Kathode (Das Substrat)
Die Kathode ist das Objekt, das beschichtet werden soll. Sie ist mit dem Minuspol der Stromquelle verbunden. Diese negative Ladung zieht die positiv geladenen Metallionen aus dem Elektrolyten an.
Die Anode (Die Metallquelle)
Die Anode ist mit dem Pluspol der Stromquelle verbunden. Sie kann zwei Arten sein:
- Aktive Anode: Hergestellt aus dem gleichen Metall, das abgeschieden wird. Sie löst sich langsam auf und füllt die Metallionen im Elektrolyten wieder auf, während sie auf der Kathode abgeschieden werden.
- Inerte Anode: Hergestellt aus einem nicht reaktiven Material (wie Platin oder Kohlenstoff). Sie löst sich nicht auf, sondern dient dazu, den Stromkreis zu schließen. In diesem Fall werden die Metallionen im Bad mit der Zeit verbraucht.
Die Stromquelle
Eine Gleichstromquelle (DC) fungiert als Motor für den gesamten Prozess. Sie liefert das elektrische Potenzial, das erforderlich ist, um Elektronen zur Kathode zu treiben und sie von der Anode wegzuziehen, wodurch die Abscheidungsreaktion erzwungen wird.
Der elektrochemische Prozess, Schritt für Schritt
Der Abscheidungsprozess ist ein kontinuierlicher Kreislauf von Oxidation und Reduktion, der durch die externe Stromquelle angetrieben wird.
Schritt 1: Oxidation an der Anode
An der positiven Anode findet eine Oxidationsreaktion statt. Wenn die Anode aktiv ist, verlieren ihre Metallatome Elektronen und werden zu positiv geladenen Ionen, die sich im Elektrolyten lösen. Dies hält die Zufuhr von Metallionen konstant.
Schritt 2: Ionenwanderung im Elektrolyten
Die positiv geladenen Metallionen (Kationen) im Elektrolyten werden durch die Lösung zur negativ geladenen Kathode gezogen. Gleichzeitig wandern negative Ionen (Anionen) zur positiven Anode, um die Lösung elektrisch neutral zu halten.
Schritt 3: Reduktion an der Kathode
Dies ist der Abscheidungsschritt. Wenn die Metallionen die Kathode erreichen, nehmen sie Elektronen auf, die von der Stromquelle geliefert werden. Diese Reduktionsreaktion neutralisiert ihre Ladung, wodurch sie aus der Lösung ausfallen und sich als feste Metallatome an der Oberfläche anlagern, wodurch die Schicht Schicht für Schicht aufgebaut wird.
Wichtige Faktoren, die die Abscheidungsqualität beeinflussen
Die Qualität, Dicke und das Aussehen der Endbeschichtung erfolgen nicht automatisch. Sie hängen von der sorgfältigen Steuerung mehrerer Schlüsselfaktoren ab.
Stromdichte
Dies ist die Strommenge pro Flächeneinheit der Kathode (gemessen in Ampere/m²).
- Eine niedrige Stromdichte führt zu einer langsamen, aber oft glatteren und gleichmäßigeren Beschichtung.
- Eine hohe Stromdichte beschleunigt die Abscheidung, kann aber bei unsachgemäßer Handhabung zu rauen, porösen oder verbrannten Ablagerungen führen.
Zusammensetzung des Elektrolyten
Die Konzentration der Metallionen, der pH-Wert und das Vorhandensein von Zusätzen (wie Glanzbildner und Einebner) haben einen enormen Einfluss. Diese Zusätze können die Kristallstruktur des abgeschiedenen Metalls verändern und sein Finish von matt zu spiegelglänzend verändern.
Temperatur
Höhere Badtemperaturen erhöhen im Allgemeinen die Leitfähigkeit des Elektrolyten und die Abscheidungsrate. Übermäßig hohe Temperaturen können jedoch unerwünschte Nebenreaktionen oder die Zersetzung von Zusätzen verursachen.
Bewegung (Agitation)
Das Rühren oder sonstige Bewegen des Bades ist entscheidend. Es stellt sicher, dass ein frischer Nachschub an Metallionen die Kathodenoberfläche erreicht und verhindert eine lokale Verarmung, die zu ungleichmäßiger Beschichtung führt, insbesondere bei komplexen Formen.
Verständnis der Kompromisse und Herausforderungen
Obwohl die Galvanik wirkungsvoll ist, handelt es sich um einen präzisen Prozess mit häufigen Fehlerquellen.
Haftung und Gleichmäßigkeit der Beschichtung
Der kritischste Erfolgsfaktor ist die Vorbereitung des Substrats. Eine unreine oder oxidierte Oberfläche führt zu schlechter Haftung, wodurch sich die Beschichtung ablöst oder abblättert. Darüber hinaus konzentriert sich der elektrische Strom natürlich an scharfen Kanten und Ecken, was dort zu dickeren Ablagerungen und in Vertiefungen zu dünneren Ablagerungen führt – ein Problem, das als „Dog-Boning“-Effekt bekannt ist.
Konkurrierende Reaktionen
Die primäre konkurrierende Reaktion, insbesondere in wässrigen Elektrolyten, ist die Reduktion von Wasser, die an der Kathode Wasserstoffgas erzeugt. Dieser Prozess verbraucht elektrischen Strom, der sonst für die Metallabscheidung verwendet würde, was die Gesamteffizienz verringert. In einigen Fällen kann absorbierter Wasserstoff das Substrat auch spröde machen.
Badwartung und Sicherheit
Galvanische Bäder sind komplexe chemische Systeme, die eine ständige Überwachung und Anpassung von pH-Wert, Temperatur und chemischen Konzentrationen erfordern. Viele industrielle Galvaniklösungen, wie solche, die Cyanid oder sechswertiges Chrom enthalten, sind hochgiftig und stellen erhebliche Risiken für die Umwelt und die Sicherheit des Bedieners dar.
Die richtige Wahl für Ihre Anwendung treffen
Das Verständnis des Grundprinzips ermöglicht es Ihnen, den Prozess auf Ihr spezifisches Ziel zuzuschneiden.
- Wenn Ihr Hauptaugenmerk auf Korrosionsschutz liegt: Ihr Ziel ist eine dichte, nicht poröse Schicht, oft unter Verwendung eines opfernden Metalls wie Zink auf Stahl (Galvanisierung) oder eines Edelmetalls wie Gold.
- Wenn Ihr Hauptaugenmerk auf Ästhetik liegt: Sie müssen die Stromdichte sorgfältig steuern und spezielle Zusätze wie Glanzbildner verwenden, um eine glatte, reflektierende Oberfläche zu erzielen, wie bei Chrom- oder Nickelbeschichtungen.
- Wenn Ihr Hauptaugenmerk auf technischer Leistung liegt (z. B. Verschleißfestigkeit): Sie benötigen eine präzise Kontrolle über Dicke und Härte, was oft bei Hartchrom- oder chemisch abgeschiedenen Nickelbeschichtungen erreicht wird, bei denen eine starke Haftung von größter Bedeutung ist.
Durch die Steuerung des Ionen- und Elektronenflusses können Sie die Oberfläche eines Materials verändern, um spezifische technische oder ästhetische Anforderungen zu erfüllen.

Zusammenfassungstabelle:
| Schlüsselkomponente | Rolle bei der Galvanik |
|---|---|
| Elektrolyt (Bad) | Lösung, die die abgeschiedenen Metallionen enthält. |
| Kathode (Substrat) | Das zu beschichtende Objekt; zieht positive Metallionen an. |
| Anode (Metallquelle) | Quelle der Metallionen (aktiv) oder inerte Elektrode. |
| Stromquelle (DC) | Liefert den Strom, um die nicht-spontane Reaktion anzutreiben. |
| Stromdichte | Steuert die Abscheidungsgeschwindigkeit und die Beschichtungsqualität (Glätte). |
| Badzusätze | Beeinflussen die Eigenschaften der Endbeschichtung (z. B. Glanz, Härte). |
Bereit für überlegene Metallbeschichtungen in Ihrem Labor?
Das Verständnis der Prinzipien der Galvanik ist der erste Schritt. Die effektive Umsetzung erfordert die richtige Ausrüstung und Verbrauchsmaterialien. KINTEK ist spezialisiert auf hochwertige Laborgeräte für die Galvanik und andere Oberflächentechnikprozesse und hilft Ihnen, präzise, zuverlässige und reproduzierbare Ergebnisse zu erzielen.
Ganz gleich, ob Sie sich auf Forschung, Qualitätskontrolle oder die Entwicklung neuer Beschichtungen konzentrieren, unsere Expertise kann die Bedürfnisse Ihres Labors unterstützen.
Kontaktieren Sie noch heute unsere Experten, um zu besprechen, wie wir Ihnen bei der Optimierung Ihres galvanischen Prozesses helfen können!
Visuelle Anleitung
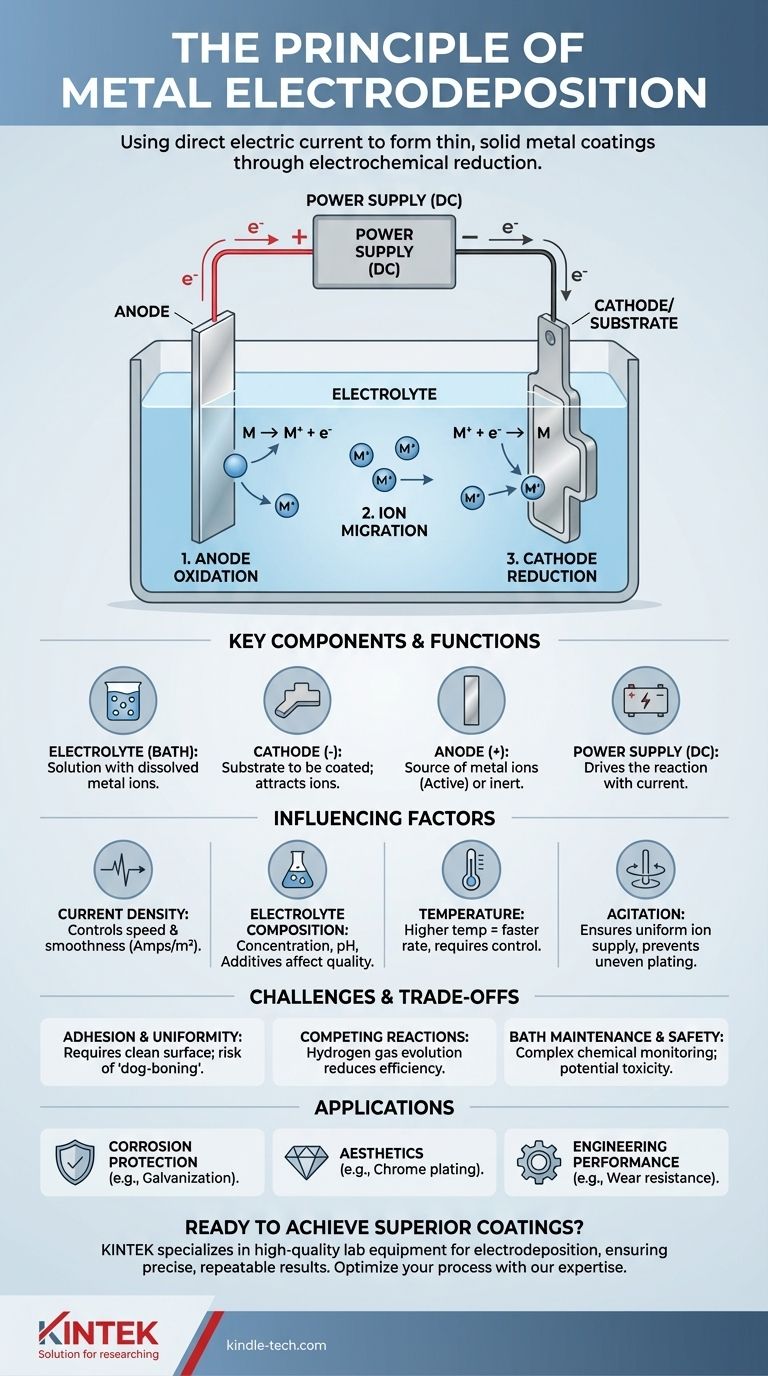
Ähnliche Produkte
- Metall-Scheibenelektrode Elektrochemische Elektrode
- Elektronenstrahlverdampferbeschichtung Sauerstofffreier Kupfertiegel und Verdampferschiffchen
- Kupfer-Nickel-Schaummetallblech
- Hochreine Gold-, Platin-, Kupfer- und Eisenmetallbleche
- Gold-Elektrodenblech Gold-Elektrode
Andere fragen auch
- Was ist die Hauptfunktion von Metallelektroden bei der Elektrokoagulation? Optimieren Sie Ihre Strategie zur Sanierung von Mikroplastik
- Wie sollte eine Metallscheibenelektrode gewartet werden? Ein Leitfaden für konsistente, zuverlässige elektrochemische Daten
- Was ist die erwartete Lebensdauer einer Metallscheibenelektrode? Verlängern Sie ihre Lebensdauer durch richtige Pflege
- Welche Vorsichtsmaßnahmen sollten bei der Verwendung von Metallscheibenelektroden getroffen werden? Genauigkeit und Langlebigkeit gewährleisten
- Welche Materialien können für Metallscheibenelektroden verwendet werden? Die Wahl des richtigen Metalls für Ihr elektrochemisches Experiment



















