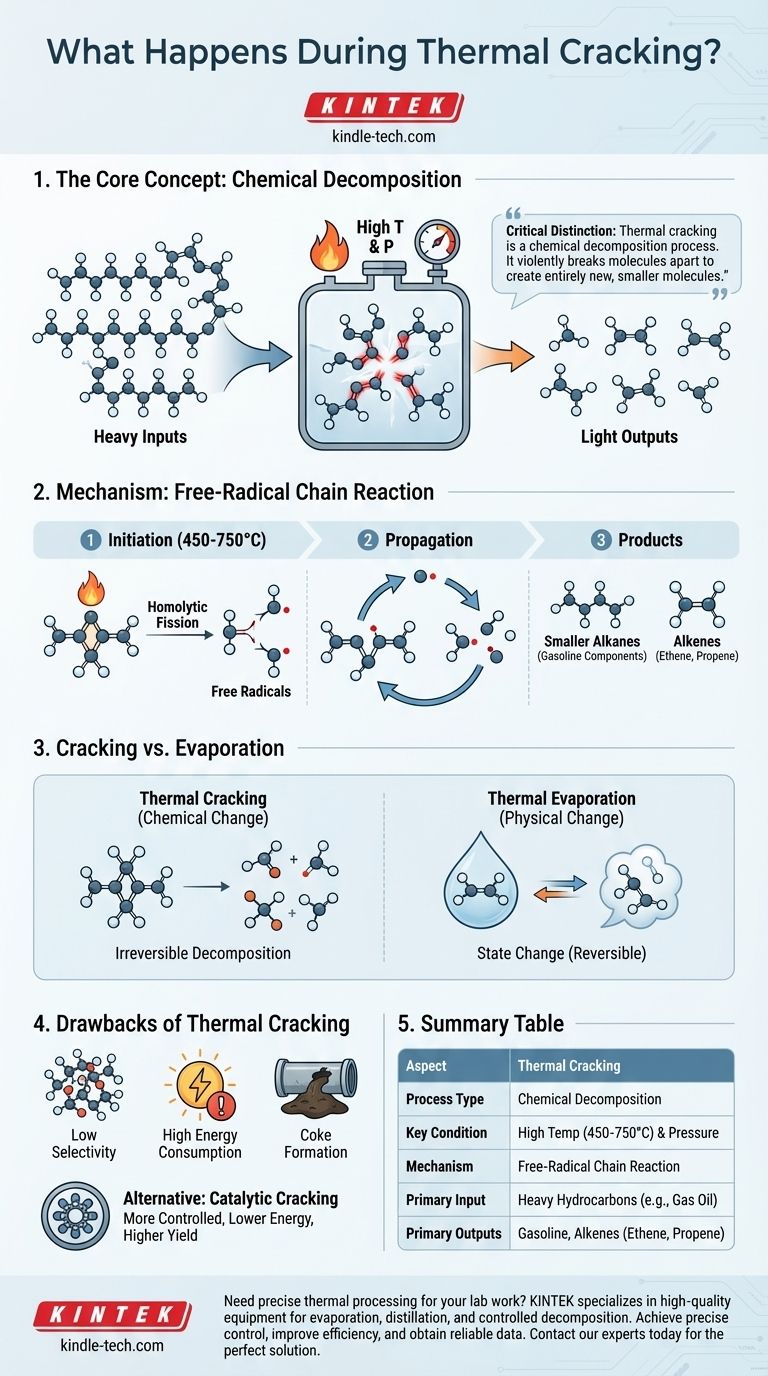
Im Wesentlichen ist thermisches Cracken ein chemischer Prozess, der hohe Temperaturen und Drücke nutzt, um große, komplexe Kohlenwasserstoffmoleküle in kleinere, wertvollere zu zerlegen. Im Gegensatz zu einer einfachen Phasenänderung wie dem Sieden verändert dieser Prozess die chemische Struktur der Moleküle grundlegend, indem er ihre Kohlenstoff-Kohlenstoff-Bindungen spaltet. Die primären Ausgangsstoffe sind schwere, minderwertige Kohlenwasserstofffraktionen, und die Produkte sind leichtere, nützlichere Produkte wie Benzinkomponenten und Alkene.
Der entscheidende Unterschied, den es zu verstehen gilt, ist, dass thermisches Cracken ein chemischer Zersetzungsprozess ist. Es verändert nicht nur den Zustand einer Substanz (wie Schmelzen oder Sieden); es zerbricht Moleküle gewaltsam, um völlig neue, kleinere Moleküle zu erzeugen.

Der Kernmechanismus des molekularen Abbaus
Thermisches Cracken ist kein sanfter Prozess. Es beruht auf roher Gewalt – in Form von thermischer Energie –, um eine Kettenreaktion auszulösen, die langkettige Kohlenwasserstoffe zerschlägt.
Initiierung der Reaktion
Der Prozess beginnt mit dem Erhitzen schwerer Kohlenwasserstoff-Einsatzstoffe wie Gasöl oder Naphtha auf sehr hohe Temperaturen, typischerweise zwischen 450 °C und 750 °C (842 °F und 1382 °F), unter hohem Druck. Diese intensive thermische Energie liefert die Aktivierungsenergie, die erforderlich ist, um die starken Kohlenstoff-Kohlenstoff-Einfachbindungen innerhalb der großen Moleküle zu brechen.
Die freie radikalische Kettenreaktion
Das anfängliche Brechen einer Kohlenstoff-Kohlenstoff-Bindung wird als homolytische Spaltung bezeichnet. Dieses Ereignis spaltet die Bindung gleichmäßig und erzeugt zwei hochreaktive Fragmente, jedes mit einem ungepaarten Elektron. Diese Fragmente werden als freie Radikale bezeichnet.
Diese instabilen freien Radikale greifen sofort andere große Kohlenwasserstoffmoleküle an und lösen eine Kettenreaktion aus, die sie in eine Vielzahl kleinerer Moleküle und weitere freie Radikale zerlegt, wodurch der Kreislauf fortgesetzt wird.
Gebildete Schlüsselprodukte
Dieser Prozess führt zu einer Mischung kleinerer, wertvollerer Produkte. Die primären Produkte sind typischerweise:
- Kleinere Alkane: Diese werden verwendet, um die Ausbeute an hochoktanigem Benzin zu erhöhen.
- Alkene: Moleküle wie Ethen (Ethylen) und Propen (Propylen) sind entscheidende Bausteine für die petrochemische Industrie und werden zur Herstellung von Polymeren und Kunststoffen verwendet.
Abgrenzung des Crackens von anderen thermischen Prozessen
Der Begriff „thermisch“ kann Verwirrung stiften, da er für viele verschiedene wissenschaftliche Prozesse gilt. Das Verständnis des grundlegenden Unterschieds zwischen einer chemischen und einer physikalischen Veränderung ist entscheidend.
Thermisches Cracken vs. thermische Verdampfung
Thermisches Cracken bewirkt eine chemische Veränderung. Sein Zweck ist es, molekulare Bindungen zu brechen und völlig neue Substanzen zu erzeugen. Dies ist eine irreversible Zersetzung.
Thermische Verdampfung hingegen ist eine physikalische Veränderung. Sie nutzt Wärme, um einen Feststoff oder eine Flüssigkeit in einen Dampf umzuwandeln, beispielsweise für Dünnschichtabscheidungen. Die Moleküle selbst bleiben intakt; sie gehen lediglich in einen gasförmigen Zustand über.
Katalytisches Cracken: Eine kontrolliertere Alternative
Moderne Raffinerien bevorzugen oft das katalytische Cracken. Dieser Prozess erreicht den gleichen molekularen Abbau, verwendet aber einen Katalysator, um die erforderliche Temperatur und den Druck zu senken. Dies ermöglicht eine bessere Kontrolle über die Reaktion, was zu einer höheren Ausbeute an gewünschten Produkten und einem geringeren Energieverbrauch führt.
Verständnis der Kompromisse und Einschränkungen
Obwohl effektiv, weist das traditionelle thermische Cracken mehrere erhebliche Nachteile auf, die zur Einführung fortschrittlicherer Methoden geführt haben.
Mangelnde Selektivität
Der freie radikalische Mechanismus ist schwer zu kontrollieren. Er erzeugt eine breite Mischung von Kohlenwasserstoffen, und die Ausbeute des spezifisch gewünschten Produkts kann geringer sein als bei gezielteren Methoden.
Hoher Energieverbrauch
Das Erreichen und Aufrechterhalten der extremen Temperaturen und Drücke, die für das thermische Cracken erforderlich sind, ist ein sehr energieintensiver und kostspieliger Prozess.
Koksbildung
Eine häufige und problematische Nebenwirkung ist die Bildung eines festen, kohlenstoffreichen Rückstands, der als Koks bekannt ist. Dieses Material lagert sich an den Reaktorwänden ab, wodurch die Effizienz verringert wird und regelmäßige Abschaltungen zur Entfernung erforderlich sind.
Wie dies in der Praxis angewendet wird
Die Wahl oder das Verständnis eines thermischen Prozesses hängt vollständig von Ihrem Ziel ab – ob Sie Moleküle zerlegen oder einfach ihren Zustand ändern müssen.
- Wenn Ihr Hauptaugenmerk auf der effizienten Produktion von hochoktanigem Benzin liegt: Moderne Raffinerien verwenden fast ausschließlich das Fluid Catalytic Cracking (FCC) wegen seiner überlegenen Kontrolle und höheren Produktqualität.
- Wenn Ihr Hauptaugenmerk auf der Produktion grundlegender Alkene (Ethen/Propen) liegt: Eine spezifische Hochtemperaturform des thermischen Crackens, das sogenannte „Steam Cracking“, bleibt die dominierende industrielle Methode für diesen Zweck.
- Wenn Ihr Hauptaugenmerk auf der Zustandsänderung eines Materials ohne Änderung seiner Chemie liegt: Sie suchen nach einem physikalischen Prozess wie thermischer Verdampfung oder Destillation, nicht nach einem chemischen Prozess wie dem Cracken.
Das Verständnis des grundlegenden Unterschieds zwischen dem Brechen chemischer Bindungen und dem Ändern physikalischer Zustände ist der Schlüssel zur Beherrschung dieser wesentlichen industriellen Prozesse.
Zusammenfassungstabelle:
| Aspekt | Thermisches Cracken |
|---|---|
| Prozesstyp | Chemische Zersetzung |
| Schlüsselbedingung | Hohe Temperatur (450-750°C) & Druck |
| Mechanismus | Freie radikalische Kettenreaktion |
| Primärer Input | Schwere Kohlenwasserstoffe (z.B. Gasöl) |
| Primäre Outputs | Benzin, Alkene (z.B. Ethen, Propen) |
Benötigen Sie präzise thermische Verarbeitung für Ihre Laborarbeit?
Ob Sie neue Materialien entwickeln oder Kohlenwasserstoffproben analysieren, die richtige Ausrüstung ist entscheidend für genaue und wiederholbare Ergebnisse. Thermische Prozesse wie Verdampfung, Destillation und kontrollierte Zersetzung sind grundlegend für den Erfolg im Labor.
Bei KINTEK sind wir auf hochwertige Laborgeräte und Verbrauchsmaterialien spezialisiert, die den strengen Anforderungen moderner Labore gerecht werden. Unser Sortiment an thermischen Verarbeitungsgeräten kann Ihnen helfen:
- Präzise Temperaturkontrolle für Ihre Experimente zu erreichen.
- Die Effizienz und Sicherheit Ihrer Prozesse zu verbessern.
- Zuverlässige und konsistente Daten zu erhalten.
Lassen Sie KINTEK Ihr Partner für Innovation sein. Kontaktieren Sie noch heute unsere Experten, um die perfekte Lösung für Ihre spezifischen Anforderungen an thermische Anwendungen zu finden.
Visuelle Anleitung
Ähnliche Produkte
- Doppelplatten-Heizpresse für Labor
- Siliziumkarbid (SiC) Keramikplatte Flachwelliger Kühlkörper für technische fortschrittliche Fein-Keramik
- Verdampferschale für organische Materie
- 50L Heiz-Kühl-Umwälzgerät Kühlwasserbad-Umwälzgerät für Hoch- und Niedertemperatur-Konstanttemperaturreaktion
- Labor-Schnelltemperatur-Prozess (RTP) Quarzrohr-Ofen
Andere fragen auch
- Was ist der Zweck von speziellen Druckvorrichtungen in Sulfid-Festkörperbatterien? Sicherstellung der chemo-mechanischen Stabilität
- Was ist die Pressform-Methode? Ein Leitfaden für konsistente, detaillierte Keramikformen
- Was ist die Hauptfunktion des Pressens von LAGP-Pulvern? Hochleistungsfähige Festelektrolyte erzielen
- Warum werden Druckformen mit nicht leitenden Harz-Innenwänden für Batterietests benötigt? Gewährleistung der Datengenauigkeit
- Wie verwendet man eine Pressform? Meistern Sie die Kunst, konsistente Keramikformen zu schaffen







